
【题目】标准状况下,某同学向 100 mL H2S 饱和溶液中通入SO2, 所得溶液 pH 变化如图所示。下列分析中,正确的是( )

A. ab 段反应是:SO2+ 2 H2S="3S↓+2" H2O
B. 亚硫酸是比氢硫酸更弱的酸
C. 原H2S溶液的物质的量浓度为0.05 molL-1
D. b 点对应的溶液导电性最强
【答案】A
【解析】
试题A.ab段pH在增大,由酸性到中性,则发生的反应是SO2+2H2S=3S↓+2H2O,A正确;B.由图象可知恰好反应时消耗二氧化硫112mL,n(SO2)=0.112L÷22.4L/mol=0.005mol,由SO2+2H2S=3S↓+2H2O可知原溶液中硫化氢为0.01mol,通入336mL二氧化硫时,溶液中亚硫酸为0.01mol,亚硫酸的浓度与原氢硫酸浓度相等,二者都是二元酸,溶液中亚硫酸pH值更小,故亚硫酸的酸性比氢硫酸更强,B错误;C.由图可知,112mLSO2与硫化氢恰好完全反应,则n(SO2)=0.005mol,由方程式可知n(H2S)=0.01mol,则原H2S溶液的物质的量浓度为0.01mol÷0.1L=0.1mol/L,C错误;D.b点为中性,只有水,导电性最差,D错误;答案选A。


科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究苯与液溴之间的反应,进行实验,装置如图所示,请根据要求回答相关问题。(已知苯的沸点为80.1 ℃,密度为0.9 g/mL )

(1)写出苯与液溴反应的化学方程式_____________________,反应类型为___________
(2)锥形瓶中有淡黄色浑浊生成,该组同学经过讨论后认为,依据该现象不能确定发生了以上反应,理由是:______________________________________,因此有必要对实验进行改进。
(3)请依据下面的实验流程图选取合适的装置和试剂对上述实验进行改进:
![]()
I _____________(填字母,下同), II _______________
A.装有NaOH溶液的洗气瓶 B.装有CC14的洗气瓶
C.装有KI溶液的洗气瓶 D.装有湿润淀粉KI试纸的集气瓶
①小组同学对改进实验后的B装置中产生的淡黄色沉淀,进行过滤、洗涤、干燥、称量。在以上步骤中:洗涤沉淀的操作为___________________________________________________
②若实验中取用的苯为17.3 mL,液溴稍过量,最终测得的沉淀质量为18.8 g,则苯在该反应中的转化率为 ____________(保留两位有效数字),该组同学认为转化率过低,除了可能发生副反应和反应可能进行不完全外,你分析还可能的原因是__________________________,__________________(请答出2条)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A~F是中学化学中常见物质,其中A、C、E为气体,且A能使品红溶液褪色;B、D为液体,D的浓溶液在常温下能使铁钝化;F的浓溶液与X共热通常用于实验室制备单质C;X是一种黑色粉末,B分子中有18个电子。(反应中部分生成物已略去)
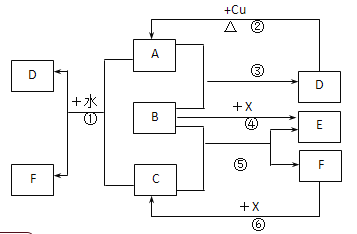
(1)写出反应②的化学方程式:___________________。
(2)写出反应①、⑤的离子方程式:①____________;⑤________________.
(3)根据图中信息,B、C、D、X氧化性从强到弱的顺序是_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:

回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____________________________,基态S原子电子占据最高能级的电子云轮廓图为________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________________。

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为________形,其中共价键的类型有________种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为anm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______________________________g·cm-3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为________nm。
所形成的正八面体的体心,该正八面体的边长为________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液由Na+、Cu2+、Ba2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成,取适量该溶液进行如下实验:下列说法正确的是
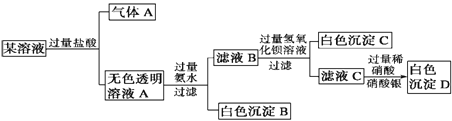
A. 原溶液中一定只存在AlO2-、CO32-、SO42-、Cl- 四种离子
B. 气体A的化学式是CO
C. 原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+
D. 生成沉淀B的离子方程式为:Al3++ 3OH- = Al(OH)3 ↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com