
����Ŀ�����顢��ϩ���л����ڹ�ҵ���й㷺��Ӧ�ã��ش��������⣺
��1����֪����C3H8��g��+5O2��g��= 3CO2��g��+4H2O��l�� ��H1
��C��ʯī��s��+O2��g��= CO2��g�� ��H2
��2H2��g��+O2��g��= 2H2O��l�� ��H3
д���������壨C3H8���ֽ�õ�ʯī��C�����������Ȼ�ѧ����ʽ��___��
��2��ú����ϩ�����ϳ����Ʊ����ϳ����Ƽ״����״��ֽ���������
�������ϳ����ķ�Ӧ��C(s)+H2O(g)=CO(g)+H2(g)�ڸ��������Է����У���÷�Ӧ��___����ѡ���
a����H>0 ��S>0 b����H>0 ��S<0
c����H<0 ��S>0 d����H>0 ��S<0
���úϳ����Ʊ��״��ķ�ӦΪ��CO(g)+ 2H2(g)![]() CH3OH(g)��������������Ӧ�����ĸ���������ʼʱѹǿ���ݻ�����ͬ��ά�ֺ��£������������±���
CH3OH(g)��������������Ӧ�����ĸ���������ʼʱѹǿ���ݻ�����ͬ��ά�ֺ��£������������±���
��� | �������� | CO(g)/moL | H2(g)/moL | CH3OH(g)/moL |
A | ά�ֺ��� | 0.2 | 0.4 | 0 |
B | ά�ֺ��� | 0.1 | 0.2 | 0.1 |
C | ά�ֺ��� | 0.4 | 0.8 | 0 |
D | ά�ֺ�ѹ | 0.4 | 0.8 | 0 |
�ﵽƽ��ʱ���ĸ������м״�����������ɴ�С�Ĺ�ϵ��___������ĸ��ʾ����
��3���������ݻ���Ϊ1L���ܱ��������Բ�ͬ����̼��[n��H2��/n(CO2)]����H/span>2��CO2����һ�������·�����Ӧ��2CO2��g��+ 6H2��g��![]() C2H4��g��+ 4H2O��g����H��CO2��ƽ��ת��������CO2�����¶ȵĹ�ϵ��ͼ��ʾ��
C2H4��g��+ 4H2O��g����H��CO2��ƽ��ת��������CO2�����¶ȵĹ�ϵ��ͼ��ʾ��
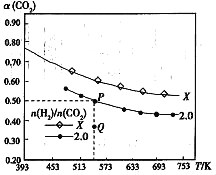
�ٴ˷�Ӧ��ƽ�ⳣ������ʽK=___��P���Ӧ�¶��£�K��ֵΪ___��
�ڸ÷�Ӧ�ġ�H___0������>����<������=�������жϵ�������___��
����̼�ȣ�X___2.0������>����<������=������
������̼��Ϊ2.0ʱ��Q��v���棩___P���v���棩������>����<������=������
���𰸡�C3H8��g��=3C��ʯī��s��+ 4H2��g�� ��H=��H1-3��H2-2��H3 a D>C>A=B ![]() 64 < ������������ʱ�������¶ȣ�CO2ת���ʼ�С����ѧƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ������H<0 > <
64 < ������������ʱ�������¶ȣ�CO2ת���ʼ�С����ѧƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ������H<0 > <
��������
(1)��������C3H8��g��+5O2��g��= 3CO2��g��+4H2O��l�� ��H1
��C��ʯī��s��+O2��g��= CO2��g�� ��H2
��2H2��g��+O2��g��= 2H2O��l�� ��H3
���ݸ�˹���ɿ�֪�������� (C3H8)�ֽ�õ�ʯī(C)���������Ȼ�ѧ����ʽΪ��C3H8��g��=3C��ʯī��s��+ 4H2��g�� ��H=��H1-3��H2-2��H3���ʴ�ΪC3H8��g��=3C��ʯī��s��+ 4H2��g�� ��H=��H1-3��H2-2��H3 ��
(2)�����ɷ�Ӧ��֪����S>0��Ҫʹ��Ӧ���Է����У�����G=��H-T��S��0�����÷�Ӧ��Ҫ�ڸ��²����Է����У�������H>0����ѡa��
��A. B����ת������ʼ����ͬ��C��Ͷ����ΪA��2����D�� C��ȣ�D�к�ѹ����Ӧ����ʱ���ʵļ�С�������С��D�൱�ڼ�ѹ��ƽ��������еij̶ȱ�C��ƽ��������еij̶�Խ�״����������Խ����ƽ��ʱ���ĸ������м״�����������Ĺ�ϵ��D> C>A=B��
�ʴ�Ϊ�� D> C> A=B��
(3)����2CO2��g��+ 6H2��g��![]() C2H4��g��+ 4H2O��g��������ƽ�ⳣ��K=
C2H4��g��+ 4H2O��g��������ƽ�ⳣ��K=![]() ��
��
��ͼ��֪��P��ƽ��ʱ������̼ת����Ϊ0.5����̼��=2������ʼʱ����Ϊ2mol/L��������̼Ϊ1mol/L���������̼Ũ�ȱ仯��Ϊ0.5mol/L����
2CO2��g��+ 6H2��g��![]() C2H4��g��+ 4H2O��g��
C2H4��g��+ 4H2O��g��
��ʼŨ��(mol/L)�� 1 2 0 0
�仯Ũ��(mol/L)�� 0.5 1.5 0.25 1
ƽ��Ũ��(mol/L)�� 0.5 0.5 0.25 1
����ƽ�ⳣ������ʽK=![]() = 64��
= 64��
�ʴ�Ϊ��![]() ��64��
��64��
������ͼ��֪�����¶�����CO2��ƽ��ת���ʼ�С��˵�������¶�ƽ�������ƶ��������¶�ƽ�������ȷ�ӦԽ��������ӦΪ���ȷ�Ӧ������H<0��
�ʴ�Ϊ��<���¶�����CO2��ƽ��ת���ʼ�С��ƽ�������ƶ������淴Ӧ�����ȷ�Ӧ������ӦΪ���ȷ�Ӧ��
����ͼ���֪X��̼��Ȳ�����2������ͬ�����·�Ӧ��ƽ��ʱ��������̼��ת���������ˣ�˵����������������������߶���̼��ת���ʣ���̼���Խ������̼ת����Խ��
�ʴ�Ϊ��> ��
������̼��Ϊ2.0ʱ��P���ƽ�⣬Q��δ��ƽ�⣬��ʱ������̼��ת���ʱ�ƽ��ʱС��˵����ʱҪ����ת������Ķ�����̼����Ӧ��Ũ���ڼ�С��������Ũ������������Ӧ�����ڼ�С���淴Ӧ�������������Դ�ʱ�淴Ӧ���ʱ�ƽ��ʱ�淴Ӧ����С��
�ʴ�Ϊ�� <��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п��Һ�������һ�����͵绯ѧ����װ��(��ͼ��ʾ)�����ҺΪ�廯пˮ��Һ���������Һ�ڵ������Һ�ڵ���ʴ��͵�ؼ䲻��ѭ��������˵������ȷ����
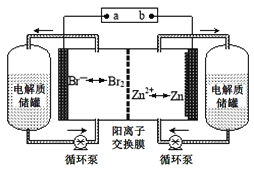
A.�����ӽ���Ĥ����ֹBr2��Znֱ�ӷ�����Ӧ
B.�ŵ�ʱ�����ĵ缫��ӦʽΪBr2+2e-=2Br-
C.���ʱ�缫b���ӵ�Դ������
D.�ŵ�ʱ������ʴ����е�������Ũ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CH4��Ƴ�ȼ�ϵ�أ��������ʸ��ߣ�װ����ͼ��ʾ(A��BΪ�����̼��)����ͨ����飬�ڱ�״���£����ļ������VL��������˵����ȷ���ǣ� ��

A��OH-��A������B��
B��0��V��22.4Lʱ������ܷ�Ӧ�Ļ�ѧ����ʽΪ��CH4 + 2O2 + KOH = KHCO3 + 2H2O
C��22.4L��V��44.8Lʱ�������缫��ӦΪ��CH4 - 8e- + 9CO32- + 3H2O = 10HCO3-
D��V=33.6Lʱ����Һ��������Ũ�ȴ�С��ϵΪ��c(CO32- )��c(HCO3- )��c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ױ�(![]() )��һ����Ҫ�Ļ���ԭ�ϣ���������������ȩ(
)��һ����Ҫ�Ļ���ԭ�ϣ���������������ȩ(![]() )��������(
)��������(![]() )�Ȳ�Ʒ���±��г����й����ʵIJ����������ʣ���ش�
)�Ȳ�Ʒ���±��г����й����ʵIJ����������ʣ���ش�
���� | ��״ | �۵�(��) | �е�(��) | ����ܶ�(��ˮ=1g��cm��3) | �ܽ��� | |
ˮ | �Ҵ� | |||||
�ױ� | ��ɫҺ����ȼ�ӷ� | ��95 | 110.6 | 0.8660 | ���� | ���� |
����ȩ | ��ɫҺ�� | ��26 | 179 | 1.0440 | �� | ���� |
������ | ��ɫƬ״����״���� | 122.1 | 249 | 1.2659 | �� | ���� |
ע���ױ�������ȩ�������������ܡ�
ʵ���ҿ�����ͼװ��ģ���Ʊ�����ȩ��ʵ��ʱ��������ƿ�м���0.5g��̬�����Դ������ټ���15mL������(��Ϊ�ܼ�)��2mL�ױ�������������70�棬ͬʱ��������12mL�������⣬�ڴ��¶��½��跴Ӧ3Сʱ��

(1)װ��a��������___��
(2)����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ___��
(3)д������ȩ��������Һ��һ���������·�����Ӧ�Ļ�ѧ����ʽ��___��
(4)��Ӧ��Ϻ�Ӧ���Һ������Ȼ��ȴ������ʱ����Ӧ����___��___(���������)�Ȳ��������ܵõ�����ȩ�ֲ�Ʒ��
(5)ʵ���м���������������ҷ�Ӧʱ��ϳ�����ʹ����ȩ��Ʒ�в����϶�ı����ᡣ����ӻ��б�����ı���ȩ�з���������ᣬ��ȷ�IJ���������___(������˳������ĸ)��
a���Ի��Һ���з�Һ
b�����ˡ�ϴ�ӡ�����
c��ˮ���м����������pH=2
d����������̼��������Һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����д����������Ҫ���3���û���Ӧ�Ļ�ѧ����ʽ��___��
�����漰��Ԫ�ص�ԭ��������С��20����6�ֵ��ʷ���6����ͬ�����塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þ�Ͻ��Ƿɻ����졢������������ҵ����Ҫ���ϡ��о���ѧϰС���ͬѧ��Ϊ�ⶨij��þ3%��5%����þ�Ͻ�(��������Ԫ��)��þ������������������������ֲ�ͬʵ�鷽������̽������д���пհף�
������һ��
��ʵ�鷽��������þ�Ͻ�������NaOH��Һ��Ӧ���ⶨʣ�����������
ʵ���з�����Ӧ�Ļ�ѧ����ʽ��_____________________________��
��ʵ�鲽�裩
(1)��ȡ10.8 g��þ�Ͻ��ĩ��Ʒ���������ΪV���ʵ���Ũ��Ϊ4.0 mol��L��1NaOH��Һ�У���ַ�Ӧ����NaOH��Һ�����V��_________mL��
(2)���ˡ�ϴ�ӡ�����������塣�ò�������δϴ�ӹ��壬���þ������������________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
����������
��ʵ�鷽��������þ�Ͻ�������ϡ������Һ��Ӧ���ⶨ��������������
��ʵ�鲽�裩
(1)ͬѧ����ѡ������ʵ��װ�����ʵ�飺
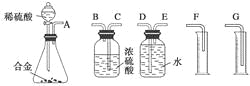
����Ϊ�����װ��������˳����A����_____��(��)��(��)(��)��(��)(��ӿ���ĸ���ɲ�����)��
(2)��ϸ����ʵ��װ�ú�ͬѧ�Ǿ�������Ϊ�������������ϴ���ϡ���������ƿ�У���ʹ������������Ҳ�Ὣƿ�ڿ����ų���ʹ�����������ƫ��ʵ�����ʱ�����ӹ��ƿ����Ͳ�ĵ�����������ˮ���ڣ�ʹ�����������ƫС�����������������ͼ��ʾ��ʵ��װ�á�
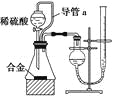
��װ���е���a��������_______________��
��ʵ��ǰ����������Һ������ֱ�ΪV1 mL��V2mL����������������Ϊ___mL��
������ȷ��������������������ⶨ��������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
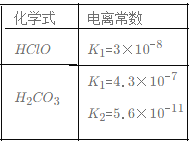
����Ŀ����֪����298KʱK(HF)=3.5��10-4��Ksp(CaF2)=1.8��10-7
��HF(aq)![]() H+(aq)+F-(aq)��H<0
H+(aq)+F-(aq)��H<0
����������֪��Ϣ�ж�����˵����ȷ���ǣ� ��
A. 298Kʱ��������ˮϡ��HF��Һ�� ![]() ���ֲ���
���ֲ���
B. 308Kʱ��HF�ĵ��볣��Ka>3.5��10-4
C. 298Kʱ����CaF2��Һ�м�������CaCl2��Ksp(CaF2)���С
D. 2HF(aq)+Ca2+(aq)![]() CaF2(s)+2H+(aq)K��0.68
CaF2(s)+2H+(aq)K��0.68
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A.����������MgCl2��6H2O�ķ�Ӧʽ MgCl2��6H2O![]() MgCl2��6H2O
MgCl2��6H2O
B.�����±��ṩ�����ݣ������ʵ���Ũ�ȵ�NaClO��NaHCO3�����Һ�У���c(HCO3��)��c(ClO��)��c(OH��) ��
C.�����£���pH=2��ϡ����ϡ��10�������и����ӵ����ʵ���Ũ�ȶ���Ϊԭ����ʮ��֮һ��
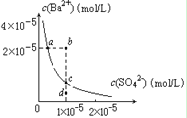
D.ij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ���ܶȻ�����Ksp=c(Ba2+)��c(SO42��)������� Na2SO4��ʹ��Һ��a��䵽b�㣻ͨ����������ʹ��Һ��d ��䵽c �㡣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���Cl2ͨ��NaOH��Һ�У���Ӧ�õ�NaCl��NaClO��NaClO3�Ļ��Һ�����ⶨNaClO��NaClO3�����ʵ���֮��Ϊ1��3����Cl2��NaOH��Һ��Ӧʱ����ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��Ϊ![]()
![]()
A.3��11B.11��3C.1��4D.4��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com