
【题目】常温下,分别取未知浓度的MOH和HA溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如下图所示。下列叙述正确的是

A. MOH为弱碱,HA为强酸
B. 水的电离程度:X=Z>Y
C. 若升高温度,Y、Z点对应溶液的pH均不变
D. 将X点溶液与Z点溶液等体积混合,所得溶液呈碱性
【答案】B
【解析】A.纵坐标为物质的量的倍数取对数,HA从pH=4到pH=5稀释了100倍,所以HA为弱酸,MOH的pH从10到9稀释了10倍,所以MOH为强碱,故A错误;B.水的电离度受溶液中酸电离出的H+浓度或者碱电离出的OH-浓度影响,X点pH=5时,c(H+)水=10-14/10-5=10-9mol/L,Z点c(H+)水=10-9mol/L,Y点c(H+)水=10-10mol/L,所以水的电离度X=Z>Y,故B正确;C.升温水的离子积会增大,溶液的pH值会发生变化,故C错误;D.HA为弱酸,MOH为强碱,X点和Z点相比,HA的溶液浓度大于MOH,所以等体积混合后溶液应该呈酸性,故D错误。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.电解饱和食盐水时,若生成11.2LCl2,则生成H2分子的数目为0.5NA
B.28g分子式为CnH2n的链烃中含有的共用电子对数目为6NA
C.1mol晶体硅中含有的共价键数目为4NA
D.87gMnO2与100mL12mol·L-1的浓盐酸共热,转移电子数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s) + 4CO(g) ![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
C.80℃达到平衡时,测得![]() ,则Ni(CO)4的平衡浓度为2mol/L
,则Ni(CO)4的平衡浓度为2mol/L
D.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时反应向正向进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的FuNvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂lmolNN吸收167kJ热量,生成1molN≡N放出945kJ热量。根据以上信息,下列说法正确的是( )
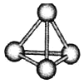
A.N4属于由非极性键构成的极性分子
B.氮元素非金属性比磷强,可知N4沸点比P4高
C.1molN4气体转变为N2气体放出888kJ热量
D.N4与N2互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了强化安全管理,某油库引进一台测空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液作电解质溶液)。下列说法不正确的是
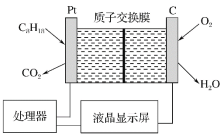
A.石墨电极作正极,发生还原反应
B.铂电极的电极反应式:C8H18+16H2O-50e-===8CO2↑+50H+
C.H+由质子交换膜左侧向右侧迁移
D.每消耗 5.6 L O2,电路中通过 1 mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中通入 H2 和 I2,发生反应:H2(g)+I2(g)![]() 2HI(g)。反应体系中各物质浓度的有关数据如下。
2HI(g)。反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/molL-1 | c(I2)/molL-1 | c(HI)/molL-1 | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | — |
下列判断正确的是
A.HI 的平衡浓度:a=b>0.004
B.平衡时,H2 的平衡转化率:丁>甲
C.平衡时,乙中 H2 的平衡转化率等于 20%
D.丙中条件下,该反应的平衡常数 K=4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 在NH![]() 和[Cu(NH3)4]2+中都存在配位键
和[Cu(NH3)4]2+中都存在配位键
B. H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央
C. SO2、SO3、BF3、NCl3都是极性分子
D. 向含有0.1 mol [Co(NH3)4Cl2]Cl的水溶液中加入足量AgNO3溶液只能生成0.1 mol AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素A、B、C、D、E、F的原子序数依次增大。A原子的阴离子的电子排布式与基态锂离子的相同,A和E位于同主族,基态B原子核外有3个能级且各能级上容纳的电子数相等,基态D原子有2个未成对电子,最外能层符号为L。+1价F离子的3d能级达到全充满结构。
回答下列问题:
(1)基态C原子价电子排布图为_____。
(2)B、C、D三种元素第一电离能由大到小排序为_____(填元素符号,下同),它们的电负性由小到大排序为_____。
(3)C、F组成的晶体的晶胞如图1所示。已知该晶体密度为ρg·cm-3,NA代表阿伏加德罗常数,则C、F最近的核间距为_____cm。
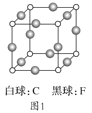
(4)A和E组成晶体,其晶胞如图2所示。E粒子周围有_____个E紧密相邻且最近;连接与E等距离且最近的A粒子构成的形状是_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)二氧化硫一空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如图:

①质子的流动方向为________________(“从A到B”或“从B到A”)。
②负极的电极反应式为________________。
(2)工业上吸收和转化SO2的电解装置示意图如下(A.B均为惰性电极):
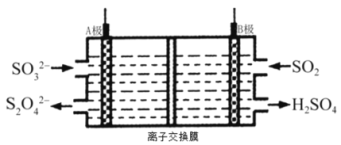
①B极接电源的________________极(“负”或“正”)。
②A极的电极反应式是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com