
【题目】氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )
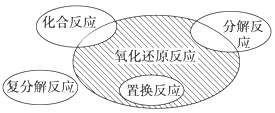
A.Cl2+2KBr=Br2+2KClB.2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O=4Fe(OH)3D.2Na2O2+2CO2=2Na2CO3+O2
科目:高中化学 来源: 题型:
【题目】在无土栽培中需用浓度为0.5mol/L NH4Cl、0.16mol/L KCl、0.24mol/L K2SO4的培养液,若用KCl、NH4Cl和(NH4)2SO4三种物质来配制1.00L上述营养液,所需三种盐的物质的量正确的是( )
A.0.4mol、0.5mol、0.12molB.0.66mol、0.5mol、0.24mol
C.0.64mol、0.5mol、0.24molD.0.64mol、0.02mol、0.24mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )

A. 在t℃时,Ag2CrO4的Ksp为1×10-8
B. 在饱和溶液中加入K2CrO4可使溶液由Y点到Z点
C. 在t℃时,Ag2CrO4(s)+2Cl-(aq)![]() 2AgCl(s)+CrO42-(aq)平衡常数K=6.25×107
2AgCl(s)+CrO42-(aq)平衡常数K=6.25×107
D. 在t℃时,以0.001mol/L AgNO3溶液滴定20mL 0.001mol/L KCl和0.001mol/L的K2CrO4的混合溶液,Cl-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 可用
可用![]() 来检验呈蓝色
来检验呈蓝色![]() 将图I装置中的铁棒末段分别联上一块锌片和铜片,并静置于含有
将图I装置中的铁棒末段分别联上一块锌片和铜片,并静置于含有![]() 及酚酞的混合凝胶上.一段时间后发现凝胶的某些区域(如图)II示发生了变化.则下列说法正确的是
及酚酞的混合凝胶上.一段时间后发现凝胶的某些区域(如图)II示发生了变化.则下列说法正确的是
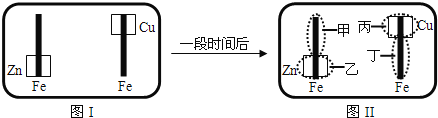
A.甲区不变色B.乙区呈现蓝色
C.丙区产生![]() 离子D.丁区产生
离子D.丁区产生![]() 离子
离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.1871 年门捷列夫最早预言了类硅元素锗,1886 年德国化学家温克勒发现和分离了锗元素,并以其祖国的名字命名为“Ge”。锗是重要的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。下图为工业上利用锗锌矿(主要成分GeO2和ZnS)来制备高纯度锗的流程。
已知:
1.丹宁是一种有机沉淀剂,可与四价锗络合形成沉淀;
2.GeCl4易水解,在浓盐酸中溶解度低。
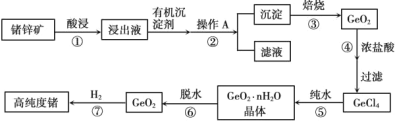
(1)锗元素在周期表中的位置:_____。
(2)步骤②操作A方法是_____。
(3)步骤③中的物质在_____(填仪器名称)中加热。
(4)步骤④不能用稀盐酸,原因可能是_____。
(5)写出步骤⑦的化学方程式_____。
Ⅱ.将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出晶体Cu(NH3)4SO4·H2O。
(1)Cu2+基态核外电子排布式为 _________;1mol [Cu(NH3)4]2+中![]() 键的数目为_______。
键的数目为_______。
(2)SO42-的S原子轨道杂化类型_______________。
(3)NH3极易溶于H2O中,原因为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物a和苯通过反应合成b的过程可表示为下图(无机小分子产物略去)。则下列说法错误的是( )

A.该反应是取代反应
B.若R为—CH3时,b中所有碳原子共面
C.若R为—C4H9时,则b中苯环上的一氯代物可能的结构共有12种
D.若R为—C4H5时,1mol b最多可以与4molH2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚酞为常用的酸碱指示剂,其结构如图所示,下列有关酚酞的说法正确的是
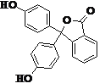
A.含有 3 种官能团
B.可以发生取代反应、消去反应、加成反应、氧化反应
C.分子式为 C20H14O4
D.1 mol 酚酞分别与 NaOH、溴水和 H2 发生反应时,消耗 NaOH、Br2 和 H2 的物质的量的最大值分别为2 mol、4 mol 和10 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用高分子吸附树脂提取卤水中的碘(主要以I -形式存在)的工艺流程如下:
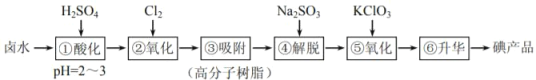
下列说法不正确的是
A.经①和④所得溶液中,c(I-)后者大于前者
B.④的作用是将吸附的碘氧化而脱离高分子树脂
C.若②和⑤中分别得到等量I2,则消耗的n(Cl2):n(KClO3) =3:1
D.由⑥得到碘产品的过程,主要发生的是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六氟合铝酸钠(Na3AlF6)俗称冰晶石,微溶于水,可用作陶瓷乳白剂、树脂橡胶的耐磨填充剂等。实验室以萤石(CaF2,难溶于水)、石英和纯碱等为原料可制备Na3AlF6,实验步骤如下:
Ⅰ.将萤石(CaF2)、石英和纯碱按一定比例混合后煅烧并释放出CO2;
Ⅱ.……
Ⅲ.在浸取液中加入稀硫酸调节pH,再加入硫酸铝,充分反应后过滤,洗涤烘干后得到六氟合铝酸钠。
回答下列问题:
(1)Na3AlF6中铝元素的化合价为__________。
(2)步骤Ⅰ中煅烧原料混合物时,盛装原料混合物的仪器名称为___________;混合物煅烧后除生成CO2、CaSiO3外还有一种产物(二元化合物),该物质的化学式为______________。
(3)步骤Ⅱ的具体内容是__________________。
(4)通过实验探究不同pH时氟离子的去除率,即对多份相同量的浸取液调节至不同pH后,再分别加入等量硫酸铝,得到了溶液中残留氟浓度和氟去除率随溶液pH的变化关系如图所示。则步骤Ⅲ中最佳pH为_________;图中当pH增大时,氟去除率下降的原因是_______________________________________。
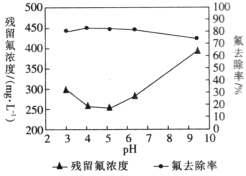
(5)步骤Ⅲ中检验过滤后的固体已洗涤干净的方法是_______________________________。
(6)写出一种能将含氟废水中氟离子去除的可行方法:______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com