
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.12.4 g白磷(P4)中所含的P-P键数目为0.6 NA
B.40 g SiC晶体中含有SiC分子的数目为NA个
C.1 mol麦芽糖完全水解后产生的葡萄糖分子数目为NA
D.标准状况下,2 mol Na2O2与44.8 L SO2完全反应,转移的电子数目为2NA
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol/LKOH溶液滴定10.00mL 0.10 mol/L某二元弱酸H2R溶液,滴定曲线如图(混合溶液总体积看作混合前两种溶液体积之和),下列关系正确的是
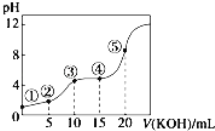
A. 点②所示溶液中:c(K+)+c(H+)=c(HR﹣)+c(R2﹣)+c(OH﹣)
B. 点③所示溶液中:c(K+)>c(HR﹣)>c(H2R)>c(R2﹣)
C. 点④所示溶液中:c(H2R)+c(HR﹣)+c(R2﹣)=0.04 mol.L-1
D. 点⑤所示溶液中:c(H+)=c(HR﹣)+2c(H2R)+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的位置关系如图所示,已知在同周期元素的常见简单离子中,W的简单离子半径最小,X、Y、Z、W的单质及其化合物在日常生活中用途极其广泛.
X | Y | Z | |
W |
(1)X元素在元素周期表中的位置_____________________.
(2)X 、Y、Z元素的氢化物均有两种或两种以上,其中一定条件下,液态YH3与液态H2Z可以发生类似方式电离,则液态YH3中阴离子的电子式为____________.
(3)超细WY粉末被应用于大规模集成电路领域.其制作原理为W2Z3、Y2、X在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:1;其反应的化学方程式为______.
(4)以W为材料制成的容器在空气中具有自我保护作用,这种容器______![]() 填“能”或“不能”
填“能”或“不能”![]() 用来腌制咸菜,原因是______.
用来腌制咸菜,原因是______.
(5)某汽车尾气分析仪以燃料电池为工作原理测定XZ的浓度,其装置如图所示,该电池中电解质为氧化钇![]() 氧化钠,其中Z2-可以在固体介质NASICON中自由移动.则负极的反应式______
氧化钠,其中Z2-可以在固体介质NASICON中自由移动.则负极的反应式______![]() 关于该电池的下列说法,正确的是______
关于该电池的下列说法,正确的是______
A 工作时电极b作正极,Z2-通过固体介质NASICON由电极b流向电极a
B 工作时电流由电极a通过传感器流向电极b
C 传感器中通过的电流越大,尾气中XZ的含量越高
(6)由元素X与元素Z组成的某种阴离子具有还原性,能被酸性KMnO4氧化,请填写相应的离子,并给予配平:____________![]() ______
______![]() ______
______![]() ______
______![]() ______
______![]() ______
______![]()

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)简称三盐,白色或微黄色粉末,稍带甜味、有毒。200℃以上开始失去结晶水,不溶于水及有机溶剂。可用作聚氯乙烯的热稳定剂。以100.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。
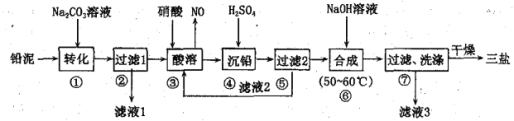
已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13。请回答下列问题
(1)步骤①转化的目的是将PbSO4转化为PbCO3,反应的离子方程式为___________________。
(2)滤液3中的主要溶质为_____________(填化学式)。
(3)步骤③酸溶时,铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为____________________。
(4)滤液2中可循环利用的溶质为___________(填化学式)。若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)为___________mol·L-1
(5)步骤⑥合成三盐的化学方程式为____________________________。若得到纯净干燥的三盐49.50 t,假设铅泥中的铅元素有80.00%转化为三盐,则铅泥中铅元素的质量分数为_____。[已知:三盐(3PbO·PbSO4·H2O)的相对分子质量为990,注意保留正确的有效数字]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成A2C和A2C2两种常见的液态化合物。请回答下列问题:
(1)D在周期表中的位置_____,E的简单阴离子结构示意图______。
(2)C、D、E三种元素简单离子的离子半径由大到小的顺序是_____。
(3)用电子式来表示BA3的形成过程:__________ 。
(4)用含A元素最简单的有机化合物与炽热的氧化铜反应生成一种单质、液态氧化物和一种可以使澄清石灰水变浑浊的气体,其化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的恒容密闭容器中,加人4mol A和2mol B进行反应:3A(g)+2B(g) ![]() 4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K=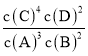
B.此时,B的平衡转化率是20%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加C,B的平衡转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
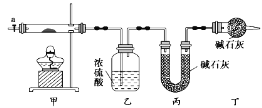
【题目】碱式碳酸钴[Cox(OH)y(CO3)z]常用作电子材料,磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示装置进行实验。
(1)请完成下列实验步骤:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中________________________(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是_________________________________________。
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的____(填字母)连接在装置______之前(填“甲”或“乙”或“丙”或“丁”)。
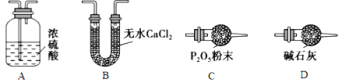
(4)若按正确装置进行实验,测得如下数据:则该碱式碳酸钴的化学式为______________。
乙装置的质量/g | 丙装置的质量/g | |
加热前 | 80.00 | 62.00 |
加热后 | 80.36 | 62.88 |
(5)CoCl2·6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种工艺如下:
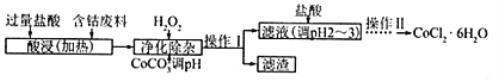
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净化除杂质时,加入H2O2发生反应的离子方程式为__________________________________。
②加入CoCO3调pH除杂得到滤渣Al(OH)3、Fe(OH)3,则pH应调节至_____。(填pH值的范围)
③加盐酸调整pH为2~3的目的为_____________________________________。
④操作Ⅱ过程为_________________________________(填操作名称)、过滤。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A.煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏得到
B.C4H8Cl2的同分异构体有9种(不含立体异构)
C.苯乙烯(![]() )分子中所有原子不可能共平面
)分子中所有原子不可能共平面
D.乙醇和乙酸均能与酸性KMnO4溶液发生氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com