
【题目】生活中的一些问题常涉及到化学知识,下列叙述不正确的是( )
A.糯米中的淀粉一经发生水解反应,就酿造成酒
B.福尔马林是一种良好的杀菌剂,但不可用来消毒饮用水
C.棉花和人造丝的主要成分都是纤维素
D.室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染空气
科目:高中化学 来源: 题型:
【题目】锌锰干电池是很古老的一次性电池,它的生产原料主要有软锰矿和闪锌矿。已知闪锌矿中含ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分;软锰矿中含MnO2约a%,SiO2约20%,Al2O3约4%,其余为水分。科研人员开发了综合利用软锰矿和闪锌矿的同槽酸浸工艺,工艺流程如下图所示。
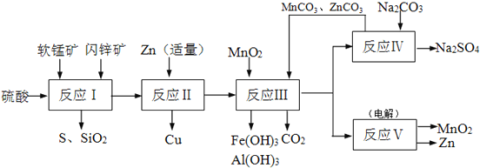
请回答下列问题:
(1)反应I需不断搅拌,目的是____________________________。
(2)检验反应I的滤液中含有Fe3+的试剂为____________;写出反应I中由FeS生成Fe3+的离子方程式____________________________________。
(3)反应Ⅱ加入适量锌的作用是__________________;反应III中MnO2的作用是________________。
(4)已知ZnCO3、MnCO3的Ksp分别为1.4×10-10、2.2×10-11;要使反应IV之后的溶液中Zn2+、Mn2+浓度均降到1.0×10-6mol/L,则溶液中残留的CO32-浓度至少为__________mol/L。
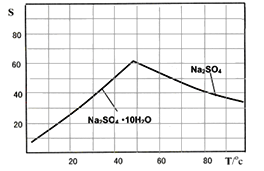
(5)图是Na2SO4和Na2SO410H2O的溶解 度曲线(g/100g水),则Ⅳ中得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液________→__________→ 用乙醇洗涤→干燥。用乙醇洗涤而不用水洗的原因是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液体积比为3:2:1时,三种溶液中Cl﹣的物质的量之比为
A. 3:4:3B. 1:2:3C. 3:2:1D. 1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )

A. 微生物促进了反应中电子的转移
B. 正极反应中有CO2生成
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示。下列有关叙述中正确的是
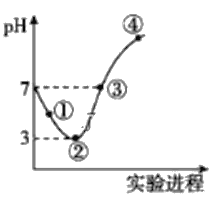
A. 曲线③④段有离子反应:HClO+OH-=ClO-+H2O
B. 可依据②处数据计算所溶解的n(Cl2)
C. ③处表示氯水与氢氧化钠溶液恰好反应完全
D. ①处c(H+)约为②处c(H+)的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 44gCO2与C3H8的混合物中含有共用电子对数为9NA
B. 将标准状况下2.24LSO2通入水中完全溶解,溶液中HSO32-与SO32-总数为0.1NA
C. 硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA
D. 标准状况下,8.96L的平均相对分子质量为3.5的H2与D2混合物中含中子数0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
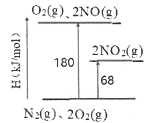
I.(1)已知氮氧化物转化过程中的能量变化如图(图中表示生成2 moI NO2的能量变化)。1 moI NO氧化为NO2的焓变△H=___________kJ/mol。
(2)某温度下,反应的平衡常数如下:
a.2NO2(g)![]() N2(g)+2O2(g) K=6.7×1016
N2(g)+2O2(g) K=6.7×1016
b.2NO(g)![]() N2(g)+O2(g) K=2.2×1030
N2(g)+O2(g) K=2.2×1030
分解反应趋势较大的反应是___________(填“a”或“b”);反应2NO(g)+O2(g)![]() 2NO2(g)的K=___________。
2NO2(g)的K=___________。
(3)已知反应2NO(g)+O2(g)![]() 2NO2(g)的正反应速率v正=k1cm(NO)cn(O2),其中k为速率常数,该反应的历程为:
2NO2(g)的正反应速率v正=k1cm(NO)cn(O2),其中k为速率常数,该反应的历程为:
第一步:NO+NO=N2O2 快速平衡
第二步:N2O2+O2![]() 2NO2 慢反应
2NO2 慢反应
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v(正)=k1c2(NO),ν(逆)=k-1c(N2O2)。下列叙述正确的是___________(填字母)。
A.第一步反应的平衡常数K=![]()
B.v(第一步的正反应)<v(第二步的反应)
C.第二步的活化能比第一步的活化能高
D.第二步中N2O2与O2的碰撞100%有效
II.氯氨是氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯氨、二氯氨和三氯氨(NH2Cl、NHCl2和NCl3),副产物少于其它水消毒剂。工业上可利用反应2C12(g)+NH3(g)![]() NHCl2(l)+HCl(g)制备二氯胺。
NHCl2(l)+HCl(g)制备二氯胺。
(1)二氯氨在中性、酸性环境中会发生强烈水解,生成具有强杀菌作用的物质,写出具有强杀菌作用的物质的电子式______________________。
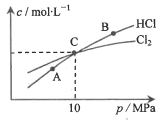
(2)在恒温条件下,将2 mol Cl2和1 moI NH3充入某密闭容器中发生上述反应,测得平衡时Cl2和HC1的物质的量浓度与平衡总压的关系如图所示。则A、B、C三点中Cl2转化率最高的是___________点(填“A”“B”或“C”);计算C点时该反应的压强平衡常数Kp(C)=___________(Kp是平衡分压代替平衡浓度计算,分压=总压×物质的量分数。)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com