
ЁОЬтФПЁПгУ NA БэЪОАЂЗќйЄЕТТоГЃЪ§ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
A. БъзМзДПіЯТЃЌ 22.4LCCl4 жаКЌгаЕФЗжзгЪ§ЮЊ NA
B. 1 mol/L FeCl3 ШмвКжаКЌга 3NA Иі Cl-
C. CO КЭ N2зщГЩЕФЛьКЯЮя 28g ЙВКЌгадзгЪ§ЮЊ 2 NA
D. 0.5molKClO3жаКЌгаClЃЕФЪ§ФПЮЊ0.5 NA
ЁОД№АИЁПC
ЁОНтЮіЁП
A. БъзМзДПіЯТЃЌCCl4ВЛЪЧЦјЬхЃЛ
B. ШмвКЬхЛ§ЮДжЊЃЌВЛФмМЦЫуРызгИіЪ§ЃЛ
C. CO КЭ N2ОљЮЊЫЋдзгЗжзгЃЌЧвФІЖћжЪСПОљЮЊ28 g/molЃЛ
D. KClO3гЩK+КЭClO3-ЙЙГЩЃЌВЛКЌCl-ЁЃ
A. БъзМзДПіЯТЃЌCCl4ЪЧвКЬхЃЌЮоЗЈАДееЦјЬхЕФФІЖћЬхЛ§МЦЫуЦфЮяжЪЕФСПЃЌЙЪAЯюДэЮѓЃЛ
B. ИљОнЙЋЪНn = ![]() = cVПЩвдПДГіЃЌШмвКЬхЛ§ЮДжЊЃЌВЛФмИљОнЮяжЪЕФСПХЈЖШМЦЫуРызгИіЪ§ЃЌЙЪBЯюДэЮѓЃЛ
= cVПЩвдПДГіЃЌШмвКЬхЛ§ЮДжЊЃЌВЛФмИљОнЮяжЪЕФСПХЈЖШМЦЫуРызгИіЪ§ЃЌЙЪBЯюДэЮѓЃЛ
C. CO КЭ N2ФІЖћжЪСПОљЮЊ28 g/molЃЌЙЪЛьКЯЮяЕФЮяжЪЕФСПЮЊn = ![]() =1 molЃЌСНепОљЮЊЫЋдзгЗжзгЃЌдђ1 molИУЛьКЯЮяЫљКЌдзгЪ§ЮЊ 2 NAЃЌЙЪCЯюе§ШЗЃЛ
=1 molЃЌСНепОљЮЊЫЋдзгЗжзгЃЌдђ1 molИУЛьКЯЮяЫљКЌдзгЪ§ЮЊ 2 NAЃЌЙЪCЯюе§ШЗЃЛ
D. KClO3ЪЧРызгЛЏКЯЮяЃЌ1 molИУЛЏКЯЮягЩ1 mol K+КЭ1 mol ClO3-ЙЙГЩЃЌВЛКЌCl-ЃЌВЛЗћКЯЪТЪЕЃЌЙЪDЯюДэЮѓЃЛ
Д№АИбЁCЁЃ


 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯђвЛЖЈСПЕФFeЁЂFeOЁЂ![]() ЕФЛьКЯЮяжаМгШы100 mLХЈЖШЮЊ
ЕФЛьКЯЮяжаМгШы100 mLХЈЖШЮЊ![]() ЕФбЮЫсЃЌЖўепЧЁКУЭъШЋЗДгІЃЌЗХГі224 mLЕФЦјЬх
ЕФбЮЫсЃЌЖўепЧЁКУЭъШЋЗДгІЃЌЗХГі224 mLЕФЦјЬх![]() БъзМзДПі
БъзМзДПі![]() ЃЌЫљЕУШмвКжаМгШыKSCNШмвККѓЮобЊКьЩЋГіЯжЁЃШєгУзуСПЕФCOдкИпЮТЯТЛЙдЯрЭЌжЪСПЕФДЫЛьКЯЮяЃЌФмЕУЕНЬњЕФжЪСПЪЧ
ЃЌЫљЕУШмвКжаМгШыKSCNШмвККѓЮобЊКьЩЋГіЯжЁЃШєгУзуСПЕФCOдкИпЮТЯТЛЙдЯрЭЌжЪСПЕФДЫЛьКЯЮяЃЌФмЕУЕНЬњЕФжЪСПЪЧ![]() ЁЁ
ЁЁ![]()
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбѕЛЏЬњбљЦЗжаКЌгаЩйСПЕФСђЫсбЧЬњЁЃФГЭЌбЇвЊВтЖЈЦфжаЬњдЊЫиЕФжЪСПЗжЪ§ЃЌЩшМЦСЫШчЯТЪЕбщЗНАИЁЃ

(1)ВйзїЂёжаХфжЦШмвКЪБЃЌЫљгУЕНЕФВЃСЇвЧЦїГ§ЩеБЁЂСПЭВЁЂВЃСЇАєЁЂНКЭЗЕЮЙмвдЭтЃЌЛЙБиаыга__________(ЬювЧЦїУћГЦ)ЁЃ
(2)ЗДгІЂйжаМгШызуСПH2O2ШмвКЃЌЗДгІЕФРызгЗНГЬЪНЃК_______________________________ЁЃ
(3)МьбщГСЕэжа![]() ЪЧЗёЯДЕгИЩОЛЕФВйзїЪЧ_______________________________________ЁЃ
ЪЧЗёЯДЕгИЩОЛЕФВйзїЪЧ_______________________________________ЁЃ
(4)НЋГСЕэМгШШЃЌРфШДжСЪвЮТЃЌгУЬьЦНГЦСПлслігыМгШШКѓЙЬЬхЕФзмжЪСПЮЊb1gЃЌдйДЮМгШШВЂРфШДжСЪвЮТГЦЦфжЪСПЮЊb2gЃЌШєb1Ѓb2ЃН0.3ЃЌЛЙгІНјааЕФВйзїЪЧ_____________________ЁЃ
(5)лсліЕФжЪСПЮЊ42.6 gЃЌзюжелслігыМгШШКѓЕФЙЬЬхЕФзмжЪСПЮЊ45.8 gЃЌдђбљЦЗжаЬњдЊЫиЕФжЪСПЗжЪ§ЮЊ________________ЁЃ
(6)гаЭЌбЇШЯЮЊЩЯЪіЗНАИЕФЪЕбщВНжшЬЋЗБЫіЃЌЫћШЯЮЊЃЌжЛвЊНЋбљЦЗШмгкЫЎГфЗжНСАшЃЌМгШШЁЂеєИЩЁЂзЦЩеГЦСПМДПЩВтЕУбљЦЗжаЬњдЊЫиЕФжЪСПЗжЪ§ЃЌФуШЯЮЊЫћЕФетИіЗНАИЪЧЗёПЩааЃП__________(ЬюЁАПЩааЁБЛђЁАВЛПЩааЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕЊдЊЫиМАЦфЛЏКЯЮяЕФзЊЛЏЙиЯЕШчЯТЭМЫљЪОЃК

ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЪЕбщЪвГЃгУЯТЭМзАжУжЦШЁВЂЪеМЏАБЦјЃЌЪдЙмжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ_____________ЁЃ
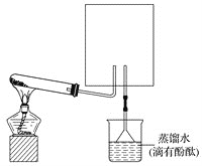
ЃЈ2ЃЉЩЯЭМжаЕФЗНПђФкЪеМЏАБЦјЕФзАжУЪЧ________(ЬюЯТЭМжаЕФзжФИ)ЁЃ
ЃЈ3ЃЉгУNH3жЦШЁNOЕФЛЏбЇЗНГЬЪНЪЧ__________________ЁЃ
ЃЈ4ЃЉЙЄвЕЩЯНЋNO2ЭЈШыNa2CO3ШмвКжаНјааЮќЪеДІРэЃЌЭъГЩЯргІЕФЛЏбЇЗНГЬЪНЃК2NO2ЃЋNa2CO3===NaNO2ЃЋ________ЃЋ________ЃЌ_______________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПI.ФГЛЏбЇПЮЭтаЁзщгУШчгвЭМвЛзАжУжЦШЁфхБНЁЃЯШЯђЗжвКТЉЖЗжа МгШыБНКЭвКфхЃЌдйНЋЛьКЯвКТ§Т§ЕЮШыЗДгІЦїAЃЈAЯТЖЫЛюШћЙиБеЃЉжаЁЃ

ЃЈ1ЃЉЙлВьЕНAжаЕФЯжЯѓЪЧ_________________________________ЁЃ
ЃЈ2ЃЉЪЕбщНсЪјЪБЃЌДђПЊAЯТЖЫЕФЛюШћЃЌШУЗДгІвКСїШыBжаЃЌГфЗжеёЕДЃЌ аДГігаЙиЗДгІЕФЛЏбЇЗНГЬЪН_____________________________ЁЃ
ЃЈ3ЃЉCжаЪЂЗХCCl4ЕФзїгУЪЧ________________________________ЁЃ
ЃЈ4ЃЉШєжЄУїБНКЭвКфхЗЂЩњЕФЪЧШЁДњЗДгІЃЌЖјВЛЪЧМгГЩЗДгІЃЌПЩЯђЪдЙмDжаМгШыAgNO3ШмвКЃЌШєВњЩњЕЛЦЩЋГСЕэЃЌдђФмжЄУїЁЃСэвЛжжбщжЄЕФЗНЗЈЪЧ________________________________________ЁЃ
II.ЪЕбщЪвгУЯТЭМЫљЪОЕФзАжУжЦШЁввЫсввѕЅЁЃ

ЃЈ1ЃЉдкДѓЪдЙмжаХфжЦвЛЖЈБШР§ЕФввДМЁЂввЫсКЭХЈСђЫсЕФЛьКЯвКЃЌВйзїВНжшШчЯТЃК__________ЃЌШЛКѓЧсеёЕДЪЙЦфЛьКЯОљдШЁЃ
ЃЈ2ЃЉХЈСђЫсЕФзїгУЪЧЃКЂй _______________ЃЛЂк ______________ЁЃ
ЃЈ3ЃЉгвБпзАжУжаЭЈеєЦјЕФЕМЙмвЊВхдквКУцЩЯЖјВЛФмВхШыШмвКжаЃЌФПЕФЪЧЗРжЙШмвКЕФЕЙЮќЁЃдьГЩЕЙЮќЕФдвђЪЧ___________________ЁЃ
ЃЈ4ЃЉЗжРыЕУЕНввЫсввѕЅЕФЗНЗЈЪЧ________________ЃЌЗжРыашвЊЕФВЃСЇвЧЦїЪЧ___________ЁЃ
ЃЈ5ЃЉШєМгЕФЪЧC2H518OHаДГіжЦввЫсввѕЅЕФЗНГЬЪН________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉЕїВщБэУїЃЌМЮСъНДѓЧХатЪДЫйЖШУПФъЮЊ0.16mmЃЌдЖдЖГЌЙ§Ш№ЕфЫЙЕТЖћИчЖћФІДѓЧХУПФъ0.03mmЕФатЪДЫйТЪЁЃ1982Фъ6дТ8ШеЃЌжиЧьЪаЯТСЫвЛГЁДѓгъЃЌЪаНМ1300ЖрЙЋЧъЫЎЕОЭЛШЛПнЛЦЃЌКУЯёЛ№ЩеЙ§вЛбљЃЌМИЬьКѓЃЌОжВППнЫРЁЃЩЯЪіВФСЯжаГіЯжЕФЯжЯѓЃЌВњЩњЕФжБНгдвђЪЧ_________________ЮлШОЮЪЬтЃЌдкЮвЙњЃЌаЮГЩИУЮлШОЕФЦјЬхжївЊЪЧ_________________ЁЃ
ЃЈ2ЃЉЦћГЕЮВЦјЃЈКЌгаЬўРрЁЂCOЁЂSO2гыNOЕШЮяжЪЃЉЪЧГЧЪаЕФЮлШОдДЁЃжЮРэЕФЗНЗЈжЎвЛЪЧдкЦћГЕЕФХХЦјЙмЩЯзАвЛИіЁАДпЛЏзЊЛЏЦїЁБЃЈгУВЌЁЂюйКЯН№зїДпЛЏМСЃЉЁЃЫќЕФЬиЕуЪЧЪЙCOКЭNOЗДгІЩњГЩCO2КЭN2ЁЃЧыЛиД№ЃК
Ђй COгыNOЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_____________________________ЁЃ
Ђк ПижЦГЧЪаПеЦјЮлШОдДЕФЗНЗЈПЩвдга_________________ЃЈЬюзжФИЃЉ
a.ПЊЗЂаТФмдД b.ЪЙгУЕчЖЏГЕ c.жВЪїдьСж d.ДјКєЮќУцОп
ЃЈ3ЃЉРЌЛјЪЧЗХДэСЫЮЛжУЕФзЪдДЃЌБиаыЖдРЌЛјНјааЗжРрЛиЪеЁЃФГзЁеЌаЁЧјЧхРэГівдЯТРЌЛјЃКa.ЗЯжН b.ЪЃВЫЪЃЗЙЁЂЙЯЙћЦЄ c.ЗЯОЩЕчГи d.ЗЯВЃСЇЦП e.ЗЯЯ№НКЪжЬз f.вЛДЮадЫмСЯЗЙКаЁЃЧыгУЯргІЕФзжФИЬюПеЁЃ
Ђй ЦфжаПЩЭЖШыга![]() БъжОРЌЛјЯфЕФЪЧ_________________ЃЛ
БъжОРЌЛјЯфЕФЪЧ_________________ЃЛ
Ђк ЦфжаЪЪвЫЖбЗЪДІРэЕФРЌЛјЪЧ_________________ЃЛ
Ђл НЋРЌЛјАДзщГЩВФСЯЗжРрЃЌЦфжаЪєгкЙшЫсбЮВФСЯЕФЪЧ____________ЃЛ
ЂмЫцвтЖЊЦњ_________________ЃЌЛсдьГЩАзЩЋЮлШОЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвжагУЯТСазАжУжЦFeCl3ЃЌПЩЙЉбЁдёЕФЪдМСгаЃКЂйMnO2ЁЁЂкNaOHШмвКЁЁЂлБЅКЭNaClШмвКЁЁЂмХЈСђЫсЁЁЂнХЈбЮЫсЁЃ

(1)АДЦјЬхСїЯђгЩзѓЕНгвХХСаЃЌИїзАжУЕФСЌНгЫГађЮЊ(ЬюаДAЁЋEађКХ)ЃК__Нг__Нг___Нг__Нг__ЁЃ
(2)зАжУСЌНгКУКѓЃЌгІИУЪзЯШНјааЕФЪЕбщВйзїЪЧ____________________________________________ЁЃ
(3)AзАжУЩеЦПжаЗДгІЕФРызгЗНГЬЪНЪЧ_________________________________________ЁЃ
(4)EжаЪЂзАЕФЪдМСЪЧ________ЃЌЦфзїгУЪЧ_________________________________________ЁЃ
(5)ЭЃжЙЗДгІКѓЃЌЛЙгаЬњЫПЪЃгрЁЃЮЊМьбщFeCl3ЕФЩњГЩЃЌВЂзюжеЕУЕНFeCl3ШмвКЃЌМзЭЌбЇЩшМЦвдЯТЪЕбщВНжшЃК
aЃЎД§BзАжУВЃСЇЙмРфШДКѓЃЌНЋЙмжаЮяжЪгУЫЎШмНтЃЌ________(ЬюВйзїЗНЗЈ)Г§ШЅВЛШмЮяЃЛ
bЃЎШЁЩйСПТЫвКЃЌЕЮМг________ШмвКЃЌШмвКГЪЯжКьЩЋЃЌвдДЫМьбщFe3ЃЋЃЛ
cЃЎШЁЩйСПТЫвКЃЌЕЮМгЯѕЫсЫсЛЏЕФAgNO3ШмвКЃЌМьбщClЃЁЃ
(6)ввЭЌбЇШЯЮЊМзЕФЪЕбщЩшМЦВЛФмзюжеЕУЕНFeCl3ШмвКЃЌЦфРэгЩЪЧ(аДГіЯргІЕФРызгЗДгІЗНГЬЪН)__________________________________________________________________ЁЃ
ФуШЯЮЊЛЙбЁдёЯТСаФФаЉЪдМСВХФмжЦЕУНЯЮЊДПОЛЕФFeCl3ШмвК________ЁЃ
AЃЎKMnO4(HЃЋ) BЃЎFeЁЁЁЁCЃЎH2O2 DЃЎCl2 ЁЁЁЁEЃЎбЮЫс
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПВнЫсОЇЬх (H2C2O4)КЭХЈСђЫсЛьКЯЛКТ§МгШШЪБЃЌПЩЗЂЩњШчЯТЗДгІЃКH2C2O4 = CO2Ёќ+COЁќ+H2O ФГПЮЭтЛюЖЏаЁзщЕФбЇЩњЩшМЦСЫШчЯТЪЕбщзАжУЃЌгУРДжЦШЁИЩдяДПОЛЕФ CO ЦјЬхЃЌВЂгУЩњГЩЕФ CO ЦјЬхЛЙд FexOy жЦШЁЬњЗлЁЃ

ЃЈ1ЃЉзАжУ B ЕФзїгУЪЧ_____ЁЃзАжУ E жаЕФЯжЯѓЪЧ_________ЁЃзАжУ F ЕФзїгУЪЧ_________ЁЃ
ЃЈ2ЃЉзАжУ D жаВЃСЇЙмжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_____ЁЃ
ЃЈ3ЃЉШє FexOy ЮЊ 0.4gЃЌЩњГЩЕФЦјЬхгыЙ§СПГЮЧхЪЏЛвЫЎЗДгІЩњГЩ 0.75g АзЩЋГСЕэЃЌдђ FexOy ЕФЛЏбЇЪНЮЊ_____ЁЃ
ЃЈ4ЃЉдкЪЕбщПЊЪМЪБЃЌЕуШМAЁЂD ОЦОЋЕЦЕФЯШКѓЫГађЪЧ_____ЃЌЪЕбщЭъБЯКѓЃЌЯЈУ№AЁЂ DОЦОЋЕЦЕФЯШКѓЫГађЪЧ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЭЕФЕчНтЪЕЯжСЫЭгыдгжЪЕФЗжРыЃЌвВдьГЩСЫвЛВПЗжзЪжиН№ЪєНјШыбєМЋФржаЃЌЭЈЙ§ЖдбєМЋФрЕФзлКЯДІРэПЩвдЛиЪеПЩЙлЕФБІЙѓН№ЪєЁЃЯЁЩЂдЊЫиЮјКЭэкЙуЗКгУгкжЮН№ЙЄвЕЁЂЕчзгЙЄвЕЁЂЙњЗРЙЄвЕЁЂвНбЇКЭХЉвЕЕШСьгђЃЌашЧѓСПдНРДдНДѓЁЃЕчНтОЋСЖЭЕФбєМЋФржївЊГЩЗжЮЊCu2SeЁЂCu2TeКЭЩйСПН№ЪєЕЅжЪAuЕШЃЌЙЄвЕЩЯДгЦфжаЭЌЪеэкЁЂЮјЕФвЛжжЙЄвеСїГЬШчЭМ:

вбжЊ:TeO2ЪЧСНадбѕЛЏЮяЃЌSeКЭTeO2ЕФЮяРэаджЪШчЯТБэ:
ЮяРэаджЪ | ШлЕу | ЗаЕу | ЫЎШмад |
Se | 221Ёц | 685Ёц | ФбШмгкЫЎ |
TeO2 | 733Ёц | 1260Ёц | ЮЂШмгкЫЎ |
(1)ЁАБКЩеЁБЪБЫљМгЕФСђЫсХЈЖШзюКУЮЊ_____(ЬюађКХ)ЁЃ
a.10% b.50% c.70% d.98%
(2)МгСђЫсБКЩеЙ§ГЬжаCu2SeВЮгыЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_________ЃЌбѕЛЏВњЮяКЭЛЙдВњЮяЕФЮяжЪЕФСПжЎБШЪЧ_______ЁЃ
(3)ТЫдќЕФжївЊГЩЗжЪЧ_______ (ЬюЛЏбЇЪН)ЁЃ
(4)ЁАЫсШмЁБКѓЃЌНЋTeO2ЯШШмгкбЮЫсЕУЕНЫФТШЛЏэкЃЌШЛКѓдйЭЈШыЖўбѕЛЏСђЕУЕНэкЕЅжЪЃЌКѓепЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ______________ ЁЃ
(5)ЁАГСэкЁБЪБПижЦШмвКЕФpHЮЊ4.5-5.0ЃЌЩњГЩTeO2ГСЕэЁЃШчЙћH2SO4Й§СПЃЌШмвКЫсЖШЙ§ДѓЃЌНЋЕМжТЁАГСэкЁБВЛЭъШЋЃЌдвђЪЧ______________ ЁЃ
(6)Й§ТЫЫљЕУДжЮјжаКЌгаNiЁЂFeЁЂCuЕШдгжЪЃЌПЩВЩгУецПееєСѓЕФЗНЗЈНјааЬсДПЃЌЛёЕУДПЮјЁЃецПееєСѓЕФЛгЗЂЮяжаЮјКЌСПгыЮТЖШЕФЙиЯЕШчЭМЫљЪОЁЃеєСѓВйзїжаПижЦЕФзюМбЮТЖШЪЧ_____(ЬюађКХ)

a. 455Ёц b.462Ёц c.475Ёц d.515Ёц
(7)ЙЄвЕЩЯЛЙПЩвдЭЈЙ§ЕчНтЭбєМЋФрМюНўЃЌЙ§ТЫКѓЕФТЫвКЕУЕНЕЅжЪэкЁЃМКжЊЕчНтЪБЕФЕчМЋОљЮЊЪЏФЋЃЌдђвѕМЋЕФЕчМЋЗДгІЪНЮЊ___________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com