
【题目】利用硫酸法钛白粉生产中的副产物(主要成分是绿矾、少量TiO2及重金属离子)制备高品质氧化铁红的工艺过程如图1: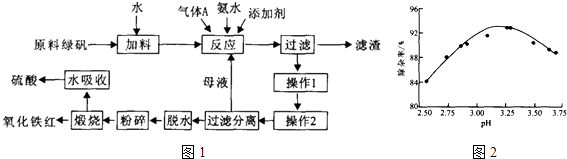
(1)原料绿矾需要加入铁粉进行预处理,其目的为(用离子方程式表示).
(2)利用氨水中和反应可以促进重金属离子水解,以便沉淀出去,如图为pH与除杂率的关系.气体A为(填化学式),调节pH适宜范围为 .
(3)操作1和操作2分别为
(4)绿矾通过脱水、锻烧等工序转化为氧化铁红.反应为:FeSO47H2O ![]() FeSO4H2O+6H2O↑:
FeSO4H2O+6H2O↑:
(5)该过程中可循环使用的物质为(填化学式).
(6)若生产1t钦白粉会产生3t含量为96.5%的绿矾原料,生产中损失5%,则高品质氧化铁红的产量为 t
(7)TiO2可用于制备海绵钛:
①已知:
(i)TiO2(g)+2C12(g)═TiC14(1)+O2(g)△H=+141kJmol﹣1
(ii)TiO2(g)+C(s)+2C12(g)═TiC14(1)+CO2(g)△H=﹣218kJmol﹣1
工业上采用(ii)制备TiC14 , 不能采用(i)的原因是 . 02Mg在高温下还原TiC14制备海绵钦的化学方程式 .
【答案】
(1)Fe+2Fe3+=3Fe2+
(2)N2;3.2﹣4.4
(3)加热浓缩、冷却结晶
(4)4FeSO4?H2O+O2 ![]() 2Fe2O3+4SO3↑+4H2O↑
2Fe2O3+4SO3↑+4H2O↑
(5)FeSO4
(6)0.791
(7)反应属于焓增、熵减的反应,标准状态下任何温度都难以自发反应;TiCl4+2Mg ![]() Ti+2MgCl2
Ti+2MgCl2
【解析】解:原料绿矾中(主要成分是绿矾、少量TiO2及重金属离子),加水溶解再用氨水调节PH值,促进重金属离子水解,以便沉淀出去,除去杂质,过滤后得硫酸亚铁溶液,滤液加热浓缩、冷却结晶,过滤得硫酸亚铁晶体,滤液可循环利用,硫酸亚铁晶体煅烧得氧化铁、三氧化硫,(1)原料绿矾中亚铁离子容易被氧化成铁离子,需要加入铁粉进行预处理,反应的离子方程式为Fe+2Fe3+=3Fe2+ ,
所以答案是:Fe+2Fe3+=3Fe2+;(2)空气中的氧气能氧化硫酸亚铁溶液中的亚铁离子,所以要用氮气隔绝空气,所以气体A为N2 , 根据图中pH与除杂率的关系,可知PH值为3.2﹣4.4之间除杂率最高,所以调节pH适宜范围为,
所以答案是:N2;3.2﹣4.4;(3)从硫酸亚铁溶液中获得硫酸亚铁晶体,可以用加热浓缩、冷却结晶方法获得晶体,
所以答案是:加热浓缩、冷却结晶;(4)绿矾通过脱水、锻烧等工序转化为氧化铁红的过程中FeSO47H2O生成FeSO4H2O,FeSO4H2O再被空气中氧化成氧化铁,反应的化学方程式为4FeSO4H2O+O2 ![]() 2Fe2O3+4SO3↑+4H2O↑,
2Fe2O3+4SO3↑+4H2O↑,
所以答案是:4FeSO4H2O+O2 ![]() 2Fe2O3+4SO3↑+4H2O↑;(5)根据流程分析可知循环的物质为 FeSO4 ,
2Fe2O3+4SO3↑+4H2O↑;(5)根据流程分析可知循环的物质为 FeSO4 ,
所以答案是:FeSO4;(6)3t含量为96.5%的绿矾原料中FeSO47H2O的质量为2895kg,所以含铁元素的质量为2895kg× ![]() ×100%=583.2kg,根据铁元素守恒可知氧化铁的质量为
×100%=583.2kg,根据铁元素守恒可知氧化铁的质量为 ![]() ×583.2×(1﹣5%)kg=0.791t,
×583.2×(1﹣5%)kg=0.791t,
所以答案是:0.791;(7)根据反应 (i)TiO2(g)+2C12(g)═TiC14(1)+O2(g)△H=+141kJmol﹣1 , (ii)TiO2(g)+C(s)+2C12(g)═TiC14(1)+CO2(g)△H=﹣218kJmol﹣1可知,(i)反应是吸热、熵减反应,(ii)是放热、熵增反应,所以采用(ii)制备TiC14 , 不能采用(i)的原因是反应(i)属于焓增、熵减的反应,标准状态下任何温度都难以自发反应,Mg在高温下还原TiC14 , 生成氯化镁和钛,反应的化学方程式为TiCl4+2Mg ![]() Ti+2MgCl2 ,
Ti+2MgCl2 ,
所以答案是:反应属于焓增、熵减的反应,标准状态下任何温度都难以自发反应;TiCl4+2Mg ![]() Ti+2MgCl2 .
Ti+2MgCl2 .


科目:高中化学 来源: 题型:
【题目】足量的锌加入100mL18mol/L的浓硫酸中充分反应,则被还原的H2SO4的物质的量为
A.1.8molB.﹤0.9mol
C.0.9molD.在0.9mol和1.8mol之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中,两种气体的分子数一定相等的是( )
A.温度相同,体积相同的O2和N2
B.温度相等,压强相等的N2和 C2H4
C.压强相同,质量相同的O3和O2
D.体积相同,密度相等的CO 和C2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜锌原电池(如图)工作时,回答下列问题: 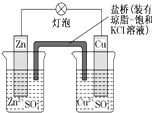
(1)(选填“Zn”或“Cu”)为原电池负极.
(2)在外电路中,电子从(选填“Zn”或“Cu”,下同)极流向极.
(3)正极反应式为
(4)电池反应的离子方程式为
(5)盐桥中的K+移向(选填“ZnSO4”或“CuSO4”)溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质转化中,A是一种酸式盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:A ![]() B
B ![]() C
C ![]() D
D ![]() E 当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素.请回答:
E 当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素.请回答:
(1)A是 , Z是 .
(2)当X是强酸时,写出B生成C的化学方程式: .
(3)当X是强碱时,E是 , 写出E和铜反应生成C的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2 .
完成下列填空:
(1)化合物X与异戊二烯具有相同的分子式,与Br2/CCl4反应后得到3﹣甲基﹣1,1,2,2﹣四溴丁烷.X的结构简式为 .
(2)异戊二烯的一种制备方法如图所示:
A能发生的反应有 . (填反应类型)
B的结构简式为 .
(3)设计一条由异戊二烯制得有机合成中间体 ![]() 的合成路线. (合成路线常用的表示方式为:A
的合成路线. (合成路线常用的表示方式为:A ![]() B…
B… ![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图的分子酷似企鹅,化学家 Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法不正确的是( ) 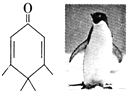
A.Penguinone的同分异构体中属于酚类只含有一个烃基侧链的物质共有4种
B.Penguinone的分子式为C10H14O,且能使溴水褪色
C.1 mol Penguinone完全燃烧消耗13mol O2
D.Penguinone分子中有碳原子不可能都在同一个平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠是活泼金属的代表,钠和钠的化合物是中学化学的基础知识.请回答下列问题.
(1)钠跟水剧烈反应,生成和氢气(H2),此实验说明钠的化学性质活泼;
(2)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是;
(3)固体碳酸钠中含有碳酸氢钠杂质,除去该杂质的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com