
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使pH试纸变蓝的溶液中:![]() 、Na+、Cl-、ClO-
、Na+、Cl-、ClO-
B.1.0 mol·L-1的HNO3溶液中:K+、[Ag(NH3)2]+、Cl-、![]()
C.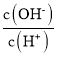 =1的溶液中:Fe2+、
=1的溶液中:Fe2+、![]() 、Al3+、I-
、Al3+、I-
D.0.1 mol·L-1的NH4HCO3溶液中:K+、Na+、![]() 、Cl-
、Cl-
 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入1L1mol/L食盐水中。下列说法正确的是( )
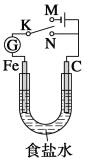
A.若电键K与N连接,铁被保护不会腐蚀
B.若电键K与N连接,正极反应式是4OH--4e-=2H2O+O2↑
C.若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜
D.若电键K与M连接,当两极共产生28L(标准状况)气体时,生成了1.25molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是重要的工业品,可用于制取卤代烃、丙醇及塑料等。回答下列问题:
(1)丙烯与HCl加成生成CH3CHClCH3或CH3CH2CH2Cl的能量与反应历程如图:
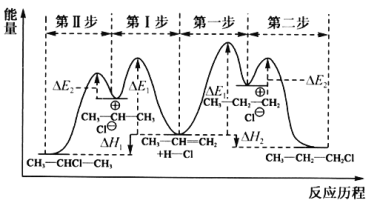
①从能量角度看,较稳定的产物是________(填“CH3CHClCH3”或“CH3CH2CH2Cl”)。
②制取CH3CHClCH3时,反应速率较慢的步骤是________(填“Ⅰ”或“Ⅱ”)。
(2)丙烷直接脱氢制丙烯的相关热化学反应如下:
主反应:C3H8(g)→C3H6(g)+H2 ΔH1=+124.27kJ·mol-1
副反应:C3H8(g)→CH4(g)+C2H4(g) ΔH2=+81.30kJ·mol-1
C3H8(g)+H2(g)→CH4(g)+C2H6(g) ΔH3=-55.64kJ·mol-1
C2H4(g)+H2(g)→C2H6(g) ΔH4
①ΔH4=_____________kJ·mol-1
②分别在0.1Mpa和0.01Mpa时,丙烷和丙烯的平衡物质的量分数如图所示:
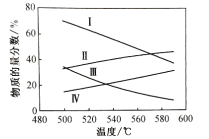
表示0.1Mpa时丙烷物质的量分数的是________(填罗马数字,下同);表示0.01Mpa时丙烯物质量的分数的是________。
(3)用二氧化碳氧化丙烷制丙烯主要反应如下:
Ⅰ.C3H8(g)![]() C3H6(g)+ H2 ΔH1>0平衡常数K1
C3H6(g)+ H2 ΔH1>0平衡常数K1
Ⅱ.CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH2>0平衡常数K2
CO(g)+H2O(g) ΔH2>0平衡常数K2
Ⅲ.耦合反应C3H8(g)+CO2(g)![]() C3H6(g)+CO(g)+H2O(g)
C3H6(g)+CO(g)+H2O(g)
当C3H8的物质的量一定时,按不同投料比Z[Z=![]() ]向密闭容器中充入C3H8和CO2,发生反应Ⅲ,C3H8平衡转化率随温度变化如图所示:
]向密闭容器中充入C3H8和CO2,发生反应Ⅲ,C3H8平衡转化率随温度变化如图所示:
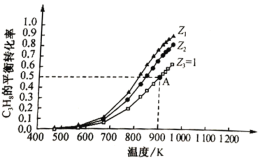
①反应Ⅲ的平衡常数K=________(用K1、K2表示)。
②Z1________(填“>”“<”“=”)Z2。原因是________
③若A点气体总压强为0.2Mpa,则丙烯的平衡分压为________MPa;900K时反应Ⅲ的平衡常数Kp=________MPa(Kp为用平衡分压表示的平衡常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要意义。
⑴ 将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) = 2Fe(s) + 3CO(g) ΔH 1 = +489.0 kJ·mol-1
C(石墨) + CO2(g) =2CO(g) ΔH 2 = +172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为___________________________________________。
⑵ 二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) ΔH
CH3OH(g) +H2O(g) ΔH
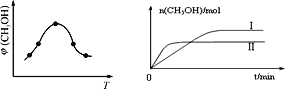
① 取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图所示,则该反应ΔH_______0(填“>”、“<”或“=”)。
② 在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图所示,曲线I、Ⅱ对应的平衡常数大小关系为:KⅠ______KⅡ(填“>” 或“<”)。
⑶ 以CO2为原料还可以合成多种物质。①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为_____________________________________。当氨碳比n(NH3 )/n(CO2 )=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.MnO2与浓盐酸混合加热:MnO2+4H++4Cl-![]() MnCl2+ Cl2↑+2H2O
MnCl2+ Cl2↑+2H2O
B.氢氧化钡溶液中加入硫酸铵:Ba2++OH-+![]() +
+![]() ===BaSO4↓+NH3·H2O
===BaSO4↓+NH3·H2O
C.FeSO4溶液中加入盐酸酸化的H2O2:Fe2++H2O2+2H+===Fe3++2H2O
D.0.01 mol·L-1 NH4Al(SO4)2溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合:![]() +Al3++2
+Al3++2![]() +2Ba2++4OH-===2BaSO4↓+Al(OH)3↓+NH3·H2O
+2Ba2++4OH-===2BaSO4↓+Al(OH)3↓+NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应与对应的图像相符合的是

A.I :N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
B.II : 2SO3(g) ![]() 2SO2(g)+O2(g)ΔH>0
2SO2(g)+O2(g)ΔH>0
C.III : 4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g)ΔH<0
4NO(g)+6H2O(g)ΔH<0
D.IV: H2(g)+CO(g) ![]() C(s)+H2O(g) ΔH>0
C(s)+H2O(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)关于反应H2(g)+![]() O2(g)===H2O(l),下列说法正确的是________(填字母)。
O2(g)===H2O(l),下列说法正确的是________(填字母)。
A.焓变ΔH<0,熵变ΔS<0
B.可以把反应设计成原电池,实现能量的转化
C.该反应在常温下不易被观察,因为具有较高的活化能,反应速率小
D.选用合适的催化剂,有可能使反应在常温常压下以较快的速率进行
(2)电渗析法淡化海水装置示意图如图所示,在电场中利用膜技术可以实现淡化海水和浓缩海水的分离。
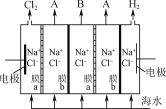
①图中膜a应选用________(填“阳离子”或“阴离子”)交换膜。
②各间隔室的排出液中,A为________(填“淡化海水”或“浓缩海水”)。
③电渗析法还可用来处理电镀废液,写出用该方法处理含AgNO3废液时所发生反应的化学反应方程式:______。
(3)水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2 ℃)、临界压强(22.1 MPa)时的水称为超临界水。
①如果超临界水的电离度变为常温下的100倍,则此时Kw的值为____。
②超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定实验条件下,测得乙醇的超临界水氧化结果如图,其中x为以碳元素计的物质的量分数,如xCO=![]() ,t为反应时间。 CO的分布分数先增后降的原因是___。
,t为反应时间。 CO的分布分数先增后降的原因是___。
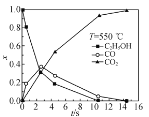
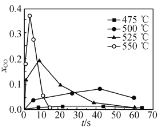
③不同温度下乙醇的超临界水氧化过程中CO的分布分数随时间变化如图所示,随着温度升高,CO分布分数峰值出现的时间提前且峰值更高的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,如图所示装置可实现有机物的电化学储氢,将10 mol由苯和环已烷组成的混合气体通入反应器中,下列说法不正确的是

A.N为电源的正极
B.H+从右向左移动
C.D电极上的电极反应式为![]()
D.苯的转化率为50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com