
【题目】用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:

(1)在实验室中由粗盐“重结晶”的操作包括溶解、过滤、蒸发、_________(填操作方法)、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是____________。
a. 蒸发的目的是得到热饱和溶液 b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液 d. 应蒸发至有较多晶体析出时为止
(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是_________。

a. 得到热饱和溶液 b. 析出晶体
(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:__________。
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____________________________________。
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和H2O,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a∶b为______________(取整数值)。
【答案】 过滤 ac a MgCl2·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑ 用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠(答“焰色反应”也可) 3∶1(或3)
Mg(OH)Cl+HCl↑+5H2O↑ 用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠(答“焰色反应”也可) 3∶1(或3)
【解析】贝壳中含有CaCO3,煅烧贝壳得到CaO,发生的反应为CaCO3![]() CO2↑+CaO,CaO和水发生反应CaO+H2O=Ca(OH)2得到石灰乳;海水通过蒸发得到粗盐和母液,粗盐通过溶解、重结晶得到精盐;将石灰乳加入母液中发生反应Ca(OH)2+MgCl2=Mg(OH)2+CaCl2,将Mg(OH)2加入稀盐酸中,发生反应 Mg(OH)2+2HCl=MgCl2+2H2O,然后浓缩得到MgCl2·6H2O,将MgCl2·6H2O在HCl氛围中加热得到MgCl2,则
CO2↑+CaO,CaO和水发生反应CaO+H2O=Ca(OH)2得到石灰乳;海水通过蒸发得到粗盐和母液,粗盐通过溶解、重结晶得到精盐;将石灰乳加入母液中发生反应Ca(OH)2+MgCl2=Mg(OH)2+CaCl2,将Mg(OH)2加入稀盐酸中,发生反应 Mg(OH)2+2HCl=MgCl2+2H2O,然后浓缩得到MgCl2·6H2O,将MgCl2·6H2O在HCl氛围中加热得到MgCl2,则
(1)在实验室中由粗盐“重结晶”制精盐的操作包括溶解、蒸发、过滤、洗涤等步骤;a.氯化钠的溶解度受温度影响不大,所以蒸发的目的是析出晶体,a错误;b.根据a知,蒸发的目的是析出晶体,b正确;c.因为溶液中含有大量杂质,所以不能蒸干溶液,c错误;d.应蒸发至有较多晶体析出时为止,因为溶液中含有大量杂质,所以不能蒸干溶液,否则得到的仍然是混合物,d正确;答案选ac;(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度如图2曲线,蒸发的目的是得到热的饱和溶液,然后冷却得到MgCl2·6H2O,答案选a;(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,根据反应物、生成物及反应条件知,该反应的化学方程式:MgCl2·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑;(4)根据焰色反应检验氯化钠,即用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠;(5)假设是1molMgCl26H2O发生反应,根据Mg原子守恒得a+b=1mol①,盐酸的质量=1mol×203g/mol-amol×40g/mol-bmol×95g/mol=(203-40a-95b)g,HCl的物质的量=(20340a95b)g×36.5%/36.5g/mol=[(203-40a-95b)×1%]mol,根据Cl原子守恒得2mol=[2b+0.01×(203-40a-95b)]mol②,联立①②得a=108/145、b=37/145,所以a:b=108/145:37/145=3:1。
Mg(OH)Cl+HCl↑+5H2O↑;(4)根据焰色反应检验氯化钠,即用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠;(5)假设是1molMgCl26H2O发生反应,根据Mg原子守恒得a+b=1mol①,盐酸的质量=1mol×203g/mol-amol×40g/mol-bmol×95g/mol=(203-40a-95b)g,HCl的物质的量=(20340a95b)g×36.5%/36.5g/mol=[(203-40a-95b)×1%]mol,根据Cl原子守恒得2mol=[2b+0.01×(203-40a-95b)]mol②,联立①②得a=108/145、b=37/145,所以a:b=108/145:37/145=3:1。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 聚乙烯是无毒高分子化合物,可用作食品包装
B. 醋和蔗糖的主要成分均为有机物
C. 蜜蜂蜇人将蚁酸注入人体可涂抹肥皂缓解
D. 人造纤维、合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合碱式碳酸镁[4MgC03·Mg(OH)2·4H2O〕,又称轻质碳酸镁。常利用菱镁矿(质量含量为碳酸镁90% ,碳酸钙10%〕碳化法制取:
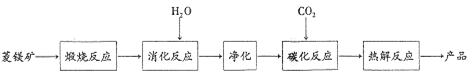
(1)根据下列表格数据,选择消化反应的最佳温度_____;理由是__________。

(2)碳化反应可生成Mg(HCO3)2,生成Mg(HCO3)2的化学方程式为_______。
(3)流程图中______和_____可以为碳化反应提供二氧化碳源。
(4)有工艺设计利用卤水碳化法制取轻质碳酸镁:
①卤水中含有Fe2+和Mn2+,当其浓度小于1×10-5时,可以认为完全除去。常温时当调节溶液pH为9.5时,此时Mn2+小于_____mol/L,不会沉淀出来。

②如果把Fe2+转化为Fe3+,从环境角度选择最合适的氧化剂为______。
A. Ca(C10)2 B. Cl2 C. H202 D. HNO3
③下列方案中,较好的为_______,理由是___________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.同系物一定符合同一通式
B.同分异构体一定具有相同的最简式
C.相对分子质量相等的两种有机物必定是同分异构体
D.同分异构体间不一定有相似的化学性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应 aA(g) ![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.7倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.7倍,下列叙述正确的是( )
A.A的转化率变小 B.平衡向正反应方向移动
C.D的物质的量变多 D.a>c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2016课标Ⅰ)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
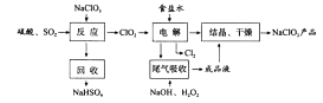
回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式_______。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于细胞中元素和化合物的叙述,正确的是
A. 蛋白质和核酸都主要在细胞核中合成
B. 除核糖体和中心体外,其他各种细胞器均含磷脂成分
C. 内质网和高尔基体的各种成分的含量相同
D. 能源物质都是糖类,所有的糖类都是能源物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的酒精溶液 ③碘的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.分液、蒸馏、萃取
C.萃取、蒸馏、分液
D.蒸馏、萃取、分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com