
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德。某种兴奋剂的结构简式如图示。有关该物质的说法中正确的是 ( )

A. 该物质与苯酚属于同系物,遇FeCl3溶液呈紫色
B. 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4mol和7mol
C. 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
D. 该分子中的所有碳原子不可能共平面
【答案】B
【解析】A.苯酚同系物中只含1个苯环,该物质含2个苯环,不是苯酚的同系物,但含酚-OH,遇FeCl3溶液呈紫色,故A错误;B.酚-OH的邻对位与溴水发生取代,碳碳双键与溴水发生加成,则1mol该物质与浓溴水反应,消耗溴为4mol;苯环与碳碳双键均与氢气发生加成,则1mol该物质与氢气反应时,消耗氢气为7mol,故B正确;C.碳碳双键、碳碳三键、酚-OH、醇-OH等均能被氧化,滴入酸性KMnO4溶液振荡,紫色褪去,只能说明其结构中碳碳双键、酚羟基两种基团至少存在一种,故C错误;D.苯环、碳碳双键均为平面结构,且直接相连的碳原子在同一平面内,则该分子中的所有碳原子可能共平面,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】某KCl、MgCl2,、Mg(NO3)2形成的混合中,c(K+) =" 0.1" mol/L ,c(Mg2+) =" 0.25" mol/L ,c (Cl-) =" 0.2" mol/L,则c(NO3-)为
A. 0.15mol/L B. 0.10mol/L C. 0.25mol/L D. 0.40mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)乙基香草醛( )是食品添加剂的增香原料,其香味比香草醛更浓郁。写出乙基香草醛分子中含氧官能团的名称:_____、_______、______,核磁共振氢谱显示该分子中有_____种不同类里的氢原子。
)是食品添加剂的增香原料,其香味比香草醛更浓郁。写出乙基香草醛分子中含氧官能团的名称:_____、_______、______,核磁共振氢谱显示该分子中有_____种不同类里的氢原子。
(2)乙基香草醛的同分异构体A是一种有机酸,A可发生以下变化:

已知:RCH2OH![]() RCHO
RCHO
b.与苯环直接相连的破原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧酸。根据以上信息,回答下列问题:
①由A→C的反应方程式_____,属于_____(填反应类型)。
②B的结构简式为_____________。
③写出在加热条件下C与NaOH醇溶液发生反应的化学方程式____________。
(3)乙基香草醛的另一种同分异构体D(![]() )是一种医药中间体,请设计合理方案,用茴香醛(
)是一种医药中间体,请设计合理方案,用茴香醛(![]() )合成D。(其他原料自选,用反应流程图表示并注明必要的反应条件)。
)合成D。(其他原料自选,用反应流程图表示并注明必要的反应条件)。
![]()
例如:_________。
(4)乙基香草醛的同分异构体有很多种,满足下列条件的同分异构体有_____种,其中有一种同分异构体的核磁共振氢谱中出现4组蜂,吸收峰的面权之比为1:1:2:6,该同分异构体的给构简式为___________。
①能与NaHCO3溶液反应 ②遇FeCl3溶液显紫色,且能与浓溴水反应
③苯环上的官能团处于对位 ④苯环上有两个甲基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】amolFeS与bmolFeO投入VLcmol/L的HNO3溶液(过量)中,充分反应,产生气体为NO,则反应后溶液中NO3-的量为
A. 62(a+b)g B. 186(a+b)g C. ![]() mol D.
mol D. ![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质所含的分子数(或原子数)等于阿伏加德罗常数的是
A. 0.5mo1 C2H4 B. 11.2L(标准状况) C2H2 气体
C. 23g Na D. 9g H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同主族,B和 D同主族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是_____(填元素符号)。
(2)写出与D同主族元素的氢化物中沸点最髙的物质电子式_______。
(3)单质E与水反应的产物中具有强氧化性物质的结构式_______。
(4)A和E形成的化合物与A和B形成的化合物反应,产物中存在的化学键类型为_______。
(5)C与氧气燃烧的产物投入到水中发生反应的离子方程式为_______。
(6)由A和B、D、E所形成的共价型化合物中,热稳定性最差的物质在足量氧气中燃烧,写出燃烧的化学方程式________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述的方法不正确的是( )
A.金属的电化学腐蚀比化学腐蚀更普遍
B.用铝质铆钉铆接铁板,铁板易被腐蚀
C.钢铁在干燥空气中不易被腐蚀
D.用牺牲锌块的方法来保护船身
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素。通常状况下,X与W元素均能形成-1价的气态氢化物,Y为同周期主族元素中原子半径最大的元素。X、Z和W的原子最外层电子教之和为20。回答下列问题:
(1)X在兀素周期表中的位置是______________。
(2)X和Y元素简单离子的半径较大的是_____(填离子符号);Z和W元素气态氢化物的稳定性较强的是______(填化学式)。
(3)Y的氧化物中既含离子键又含共价键的是_____(用电子式表示)。
(4)Z的最高价氧化物对应水化物的浓溶液(过量)和氧化亚铜共热,反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某种软锰矿(主要成分MnO2,同时含有FeCO3、Al2O3、SiO2等)为主要原料生产KMnO4的一种流程图如下:
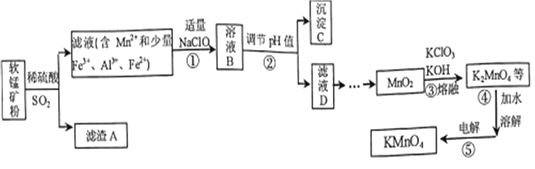
已知:Mn(OH)2极易被空气氧化;Fe(OH)3、Al(OH)3的溶度积常数依次为4.0×10-38、1.3×10-33。
(1)滤渣A的化学式是_________;溶液B中的主要阴离子有______________。
(2)为避免引入杂质,②步调节pH加入的物质是____________;调节pH除杂过程中,后析出的
沉淀是________________。
(3)浓硫酸与MnO2反应也能生成Mn2+,其化学方程式是___________________。
(4) K2MnO4在酸性、中性环境下都会歧化生成MnO4-和MnO2,则③步原料应保证_______________。
④步溶解水应煮沸的目的是_____________________。
(5)⑤步的阳极电极反应式是____________;该法电解时要产生污染,其原因是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com