
【题目】某实验小组在T1温度下,向容积为1L的恒容密闭容器中,同时通入0.1mol CO(g)和0.1mol H2O(g),发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=a kJ·mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
CO2(g)+H2(g)△H=a kJ·mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。

(1)0~10min内,CO的平均反应速率为_____________
(2)T1温度下,该反应的平衡常数K为_______________(用分数表示)。
(3)已知:I.H2的燃烧热 △H=-285.8 kJ·mol-1;
II.CO的燃烧热 △H=-283 kJ·mol-1;
III.H2O(g)![]() H2O(l) △H=-44 kJ·mol-1。则a=______________
H2O(l) △H=-44 kJ·mol-1。则a=______________
(4)T1温度下,某时刻另一实验小组测得反应容器中有关数据为c(CO)=0.6 mol·L-1、c(H2O)=1.6 mol·L-1、c(H2)=0.4 mol·L-1、c(CO2)=0.4 mol·L-1,则该反应在下一时刻将_______ (填“向正反应方向进行”“向逆反应方向进行”或“达到平衡”),判断依据是___________________。
【答案】0.003 mol/(L·min) ![]() -41.2 向正反应方向进行 Q=
-41.2 向正反应方向进行 Q=![]() ,所以该反应向正反应方向进行
,所以该反应向正反应方向进行
【解析】
(1)根据图中信息可知,0~10min内,CO2的平均反应速率为v(CO2)=![]() =0.003 mol/(L·min);根据反应CO(g)+H2O(g)
=0.003 mol/(L·min);根据反应CO(g)+H2O(g)![]() CO2(g)+H2(g)中化学反应速率之比等于计量数之比可知,v(CO)=v(CO2)=0.003 mol/(L·min);
CO2(g)+H2(g)中化学反应速率之比等于计量数之比可知,v(CO)=v(CO2)=0.003 mol/(L·min);
(2)T1温度下,根据三段式可知,
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
开始时的浓度(mol/L) 0.1 0.1 0 0
改变的浓度(mol/L) 0.03 0.03 0.03 0.03
平衡时的浓度(mol/L) 0.07 0.07 0.03 0.03
该反应的平衡常数K=![]() =
=![]() ;
;
(3)已知:I.H2(g)+ ![]() O2(g)=H2O(l) △H1=-285.8 kJ·mol-1;
O2(g)=H2O(l) △H1=-285.8 kJ·mol-1;
II.CO(g)+ ![]() O2(g)=CO2 (g) △H2=-283 kJ·mol-1;
O2(g)=CO2 (g) △H2=-283 kJ·mol-1;
III.H2O(g)![]() H2O(l) △H3=-44 kJ·mol-1
H2O(l) △H3=-44 kJ·mol-1
根据盖斯定律,由II- I + III得反应CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-283 kJ·mol-1-(-285.8 kJ·mol-1)-44 kJ·mol-1=a kJ·mol-1。则a=-41.2;
CO2(g)+H2(g) △H=-283 kJ·mol-1-(-285.8 kJ·mol-1)-44 kJ·mol-1=a kJ·mol-1。则a=-41.2;
(4)T1温度下,某时刻另一实验小组测得反应容器中有关数据为c(CO)=0.6 mol·L-1、c(H2O)=1.6 mol·L-1、c(H2)=0.4 mol·L-1、c(CO2)=0.4 mol·L-1,则该反应在下一时刻将向正反应方向进行,判断依据是Q=![]() ,所以该反应向正反应方向进行。
,所以该反应向正反应方向进行。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还含有一定量的SiO2)可用于制备FeCO3,其流程如下:
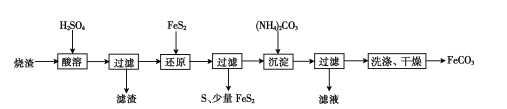
已知:“还原”时,FeS2与H2SO4不反应。
(l)“酸溶”时Fe2O3发生的化学反应方程式为________
(2)实验室“过滤”时所用的玻璃仪器有烧杯、________
(3)“还原”时生成S的离子方程式为________
(4)检验FeCO3是否洗净的方法是________
(5)“滤液”中的溶质可能有____(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列叙述中正确的是
A.常温常压下,11.2 LNH3所含的原子数为2NA
B.标准状况下,22.4 LCl2所含的原子数为NA
C.常温常压下,80 gSO3所含的氧原子数为3NA
D.一定条件下,56 g铁与足量HNO3完全反应,转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3极易溶于水,可用作喷泉试验。回答下列问题:
(l)实验室制取NH3通常有两种方法:i用固体氢氧化钙与氯化铵共热;ii在常温下用固体氢氧化钠与浓氨水混合。
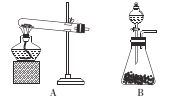
①方法i制取氨气的化学方程式为 ___。
②方法ii应选用的发生装置是 ___(填“A”或“B”),生成NH3的原因是____
(2)进行如图所示喷泉实验时,上部烧瓶中已充满干燥的NH3,引发喷泉的操作是____;若在烧杯内的水中滴加几滴无色酚酞试液,则形成喷泉后,烧瓶里的溶液呈____色。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)材料是人类赖以生存和发展的重要物质基础。
①水泥是最常用的建筑材料,它属于________(填字母)。
a. 金属材料 b. 无机非金属材料 c. 有机高分子材料
②下列硅酸盐产品的生产原料中不需要石灰石的是________(填字母)。
a. 陶瓷 b. 水泥 c. 玻璃
③高岭土是烧制瓷器的重要原料,其组成可以表示为Al2Si2Ox(OH)y,其中x,y的数值分别是________(填字母)。
a. 5、4 b. 6、3 c. 7、2
④下列物品的构成材料中主要是合成高分子材料的是________(填字母)。
a. 宣纸 b. 羊毛衫 c. 保鲜膜
⑤橡胶是制造轮胎的主要原料,天然橡胶是________结构(填“线型”或“体型”),需经过硫化处理改变其结构,增强其机械强度。
(2)某品牌果冻标签如图所示。回答下列问题:

①食品添加剂中,属于无机盐的是______(填化学式)。
②属于着色剂的是诱惑红和______;属于防腐剂的是______。
③配料表中白砂糖的成分是蔗糖,请写出蔗糖在人体内水解的化学方程式______。
(3)化学与科学技术、生产生活及环境保护等密切相关。
①2016年12月我省启动了保卫碧水蓝天的“263”行动,减少煤炭消费总量,减少雾霾天气的发生。形成硫酸型酸雨的主要气体是______;严格整治畜禽养殖场污染,主要是为减少______和P等元素及化学需氧量对水体的污染。
②目前正在推广用尿素水解液来消除柴油汽车尾气中的氮氧化物。写出尿素水解液中的NH3与NO在催化剂作用下,反应生成无污染物质的化学方程式____________________________________________________。
③阿司匹林作为一种药物,主要具有______作用;Mg2Si3O8·nH2O(三硅酸镁)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2 ·H2O等物质的化学方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某恒温密闭容器中,投入一定量的A发生可逆反应:A(s)![]() B(g)+C(g) △H=-QkJ·mol-1(Q>0)。一段时间后反应达到平衡,然后缩小容器体积,重新达到平衡。下列分析不正确的是
B(g)+C(g) △H=-QkJ·mol-1(Q>0)。一段时间后反应达到平衡,然后缩小容器体积,重新达到平衡。下列分析不正确的是
A. 两次平衡时,C(g)的浓度相等
B. 平衡时,单位时间内:n(B)生成:n(C)消耗=1:1
C. 若开始时向容器中加入1 mol B和1 mol C,则达到平衡时吸收Q kJ热量
D. 若再向平衡体系中加入少量A,平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 是中学化学中常见的三种物质,下表各组物质之间通过一步反应不能实现右图所示转化关系的是
X | Y | Z | 箭头上所标数字的反应条件 | ||
A. | NO | NO2 | HNO3 | ①常温遇氧气 |
|
B. | Cl2 | NaClO | HClO | ②通入CO2 | |
C. | Na2O2 | NaOH | NaCl | ③加入H2O2 | |
D. | Al2O3 | NaAlO2 | Al(OH)3 | ④加NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 向400mL某浓度的稀硝酸中加入Wg铁粉(还原产物只有NO),充分反应后,铁粉减少16.8 g且铁粉有剩余,继续向容器中加入足量的稀硫酸,会产生气体A。回答下列问题:
(1)稀硝酸的物质的量浓度是_____________ mol·L1
(2)气体A中若含有H2,则W的值一定要大于__________g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com