
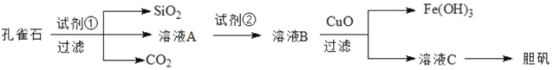
ΓΨΧβΡΩΓΩΩΉ»Η ·÷ς“ΣΚ§Cu2(OH)2CO3Θ§“‘ΦΑ…ΌΝΩFeΓΔSiΒΡΜ·ΚœΈοΘ§Ω…“‘”ΟΩΉ»Η ·ΈΣ‘≠Νœ÷Τ±ΗΒ®Ζ·( CuSO4ΓΛ5H2O)Θ§≤Ϋ÷η»γœ¬ΘΚ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1) ‘ΦΝΔΌ «“Μ÷÷≥ΘΦϊΒΡΥαΘ§ΤδΜ·―ß ΫΈΣ______ΓΘΙΐ¬ΥΥυ–η“ΣΒΡ≤ΘΝß“«Τς”–…’±≠ΓΔ__________ΓΘ
(2) Β―ι “Φλ―ι Fe3+ΒΡ≥Θ”ΟΖΫΖ® «_____________________________________ ΓΘ
(3)»τ»ή“ΚA÷–ΒΡΫπ τάκΉ””–Cu2+ΓΔFe2+ ΓΔFe3+Θ§…œ ωΝς≥Χ÷––η“Σ”Ο ‘ΦΝΔΎΫΪ»ή“ΚA÷–ΒΡFe2+»Ϊ≤ΩΉΣΜ·ΈΣFe3+Θ§¥”Εχ–Έ≥…»ή“Κ B,‘ρ ‘ΦΝΔΎΡήΖώ Ι”Ο¬»Υ°ΘΩΘ®ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±Θ§»τΧνΓΑ≤ΜΡήΓ±Θ§«κΫβ Ά‘≠“ρΘ©ΓΘ_________________
(4)”…»ή“ΚCΜώΒΟΒ®Ζ·Θ§–η“ΣΨ≠Ιΐ_______ΓΔ_____ΓΔΙΐ¬ΥΒ»≤ΌΉςΓΘ
(5)»Γ25.00mL»ή“ΚA,”Ο1.000ΓΝ10-2mol/LΒΡ KMnO4±ξΉΦ»ή“ΚΒΈΕ®ΓΘΖ¥”ΠάκΉ”ΖΫ≥Χ ΫΈΣΘΚ5Fe2++ MnO4-+8H+=5Fe3+ Mn2+ +4H2OΘ§»τœϊΚΡ±ξΉΦ»ή“Κ 20.00mLΘ§‘ρ»ή“ΚA ÷–Fe2+ΒΡ≈®Ε»ΈΣ_________mol/LΓΘ
ΓΨ¥πΑΗΓΩH2SO4 ¬©ΕΖΓΔ≤ΘΝßΑτ œρ»ή“Κ÷–ΒΈΦ”KSCN»ή“ΚΘ§»τ±δ―ΣΚλΘ§‘ρΚ§”–Fe3+ ≤ΜΡήΘ§Μα“ΐ»κ–¬‘”÷ ’τΖΔ≈®Υθ ά以ΫαΨß 0.040
ΓΨΫβΈωΓΩ
ΩΉ»Η ·÷ς“ΣΚ§Cu2(OH)2CO3Θ§“‘ΦΑ…ΌΝΩFeΓΔSiΒΡΜ·ΚœΈοΘ§œρΩΉ»Η ·÷–Φ”»κ ‘ΦΝΔΌΈΣœΓΝρΥαΘ§ΖΔ…ζΒΡΖ¥”Π”–Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2ΓϋΘ§ΧζΒΡ―θΜ·Έο»ή”ΎœΓΝρΥα…ζ≥…ΝρΥαΧζΓΔΝρΥα―«Χζ―ΈΚΆΥ°Θ§Ιΐ¬ΥΒΟΒΫΒΡ¬Υ‘ϋΈΣSiO2Θ§œρ»ή“ΚA÷–Φ”»κ ‘ΦΝΔΎΒΟΒΫ»ή“ΚBΘ§ ‘ΦΝΔΎ”Π «“Μ÷÷―θΜ·ΦΝΘ§ΫΪFe2+ΉΣΜ·ΈΣFe3+«“≤ΜΡή“ΐΫχ‘”÷ Θ§”ΠΗΟ―Γ»ΓΥΪ―θΥ°Θ§»ή“ΚB÷–Κ§ΝρΥαΧζΚΆΝρΥαΆ≠Θ§œρ»ή“ΚB÷–Φ”»κCuOΘ§ΒΟΒΫ»ή“ΚCΚΆFe(OH)3Θ§Ιΐ¬ΥΒΟΒΫ»ή“ΚCΈΣΝρΥαΆ≠»ή“ΚΘ§Ψ≠’τΖΔΫαΨßΩ…ΒΟΒΫΒ®Ζ·ΓΘ
Θ®1Θ© ‘ΦΝΔΌ «“Μ÷÷≥ΘΦϊΒΡΥαΘ§“‘±ήΟβ“ΐ»κ–¬‘”÷ Θ§”ΠΈΣœΓΝρΥαΘ§ΤδΜ·―ß ΫΈΣΘΚH2SO4Θ§Ιΐ¬ΥΥυ–η“ΣΒΡ≤ΘΝß“«Τς”–¬©ΕΖΓΔ…’±≠ΓΔ≤ΘΝßΑτΘ§Ι ¥πΑΗΈΣΘΚH2SO4ΘΜ¬©ΕΖΓΔ≤ΘΝßΑτΘΜ
Θ®2Θ©Φλ―ιΧζάκΉ”Θ§Ω…»Γ―υΘ§œρΤδ÷–ΒΈΦ”KSCN»ή“ΚΘ§»ή“Κ±δ―ΣΚλ…ΪΘ§‘ρΚ§”–Fe3+Θ§Ι ¥πΑΗΈΣΘΚœρ»ή“Κ÷–ΒΈΦ”KSCN»ή“ΚΘ§»τ±δ―ΣΚλΘ§‘ρΚ§”–Fe3+ΓΘ
Θ®3Θ©≤ΜΡήΦ”»κ¬»Υ°Θ§Μα…ζ≥…¬»Μ·Ά≠Εχ“ΐ»κ–¬‘”÷ Θ§Ι ¥πΑΗΈΣΘΚ≤ΜΡήΘ§Μα“ΐ»κ–¬‘”÷ ΓΘ
Θ®4Θ©”…»ή“ΚCΜώΒΟΒ®Ζ·Θ§–η“ΣΨ≠Ιΐ’τΖΔ≈®ΥθΓΔά以ΫαΨßΓΔΙΐ¬ΥΓΔœ¥Β”ΓΔΗ…‘οΘ§Ι ¥πΑΗΈΣΘΚ’τΖΔ≈®ΥθΘΜά以ΫαΨßΓΘ
Θ®5Θ©n(KMnO4)=1.000ΓΝ102mol/LΓΝ0.02L=2.000ΓΝ104molΘ§άκΉ”ΖΫ≥Χ ΫΈΣΘΚ5Fe2++ MnO4-+8H+=5Fe3+ Mn2+ +4H2OΩ…÷ΣΘ§n(Fe2+)=1.000ΓΝ103molΘ§‘ρ»ή“ΚA÷–Fe2+ΒΡ≈®Ε»ΈΣ0.001mol/0.025L=0.040mol/LΘ§Ι ¥πΑΗΈΣΘΚ0.040ΓΘ


 ≤Ι≥δœΑΧβΫ≠Υ’œΒΝ–¥πΑΗ
≤Ι≥δœΑΧβΫ≠Υ’œΒΝ–¥πΑΗ ―ßΝΖΩλ≥ΒΒάΩΎΥψ–ΡΥψΥΌΥψΧλΧλΝΖœΒΝ–¥πΑΗ
―ßΝΖΩλ≥ΒΒάΩΎΥψ–ΡΥψΥΌΥψΧλΧλΝΖœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡΈ±Ί¬εΕϊ «“Μ÷÷”Ο”Ύ―ΣΙήά©’≈ΒΡΫΒ―Σ―Ι“©ΈοΓΘ”Ο”ΎΚœ≥…ΡΈ±Ί¬εΕϊ÷–ΦδΧεGΒΡ≤ΩΖ÷Νς≥Χ»γΆΦΘΚ

“―÷ΣΘΚ““ΥατϊΒΡΫαΙΙΦρ ΫΈΣ![]()
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©GΈο÷ ÷–ΒΡΚ§―θΙΌΡήΆ≈ΒΡΟϊ≥Τ «___ΓΔ___ΓΘ
Θ®2Θ©Ζ¥”ΠAΓζBΒΡΜ·―ßΖΫ≥Χ ΫΈΣ___ΓΘ
Θ®3Θ©…œ ωΔήΓΔΔί±δΜ·Ιΐ≥ΧΒΡΖ¥”Πάύ–ΆΖ÷±π «___ΓΔ___ΓΘ
Θ®4Θ©–¥≥ω¬ζΉψœ¬Ν–ΧθΦΰΒΡCΒΡ“Μ÷÷Ά§Ζ÷“λΙΙΧεΒΡΫαΙΙΦρ ΫΘΚ___ΓΘ
Δώ.±ΫΜΖ…œ÷Μ”–ΝΫ÷÷»Γ¥ζΜυ
Δρ.Ζ÷Ή”÷–÷Μ”–4÷÷≤ΜΆ§Μ·―ßΜΖΨ≥ΒΡ«β
Δσ.Ρή”κNaHCO3Ζ¥”Π…ζ≥…CO2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ’αΧ«θΞ «ΝΣΚœΙζΙζΦ ΝΗ≈©Ήι÷·ΚΆ άΫγΈά…ζΉι÷·ΆΤΦω Ι”ΟΒΡ ≥ΤΖ»ιΜ·ΦΝΘ° Ρ≥’αΧ«θΞ”…’αΧ«”κ”≤÷§Υα““θΞΚœ≥…Θ§ Ζ¥”Π»γΆΦΥυ ΨΓΘ”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «

A.’αΧ«θΞ“≤ΗΏΦΕ÷§ΥαΒΡΗ ”ΆθΞ
B.Κœ≥…ΗΟ’αΧ«θΞΒΡΖ¥”Π τ”Ύ»Γ¥ζΖ¥”Π
C.’αΧ«Ζ÷Ή”÷–Κ§”–7Ηωτ«Μυ
D.ΗΟ’αΧ«θΞ‘ΎœΓΝρΥαΒΡΉς”Οœ¬Υ°ΫβΘ§Υ°ΫβΙΐ≥Χ÷–÷Μ”–”≤÷§ΥαΚΆΤœΧ―Χ«ΝΫ÷÷≤ζΈο
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ΘΈ¬œ¬Θ§œρ20.00 mL 0.100 0 molL©¹1 (NH4)2SO4»ή“Κ÷–÷πΒΈΦ”»κ0.200 0 molL©¹1 NaOH»ή“Κ ±Θ§»ή“ΚΒΡpH”κΥυΦ”NaOH»ή“ΚΧεΜΐΒΡΙΊœΒ»γΆΦΥυ Ψ(≤ΜΩΦ¬«Μ”ΖΔ)ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
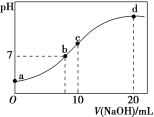
A. ΒψaΥυ Ψ»ή“Κ÷–ΘΚc(NH4+)ΘΨc(SO42-)ΘΨc(OHΘ≠)ΘΨc(HΘΪ)
B. ΒψbΥυ Ψ»ή“Κ÷–ΘΚc(NH4+)ΘΫc(NaΘΪ)ΘΨc(HΘΪ)ΘΫc(OHΘ≠)
C. ΒψcΥυ Ψ»ή“Κ÷–ΘΚc(SO42-)ΘΪc(HΘΪ)ΘΫc(NH3ΓΛH2O)ΘΪc(OHΘ≠)
D. ΒψdΥυ Ψ»ή“Κ÷–ΘΚc(SO42-)ΘΨc(NH3ΓΛH2O)ΘΨc(OHΘ≠)ΘΨc(NH4+)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩNA±μ ΨΑΔΖϋΦ”Β¬¬ό≥Θ ΐΘ§œ¬Ν––π ω’ΐ»ΖΒΡ «
A.32 g S8ΒΞ÷ Θ®”“ΆΦΘ©÷–Κ§”–ΒΡSΓΣSΦϋΗω ΐΈΣ8NA
B.≥ΘΈ¬œ¬Θ§16gO2ΚΆO3ΒΡΜλΚœΤχΧε÷–ΥυΚ§―θ‘≠Ή” ΐΈΣ2.5NA
C.1molMg‘ΎΩ’Τχ÷–Άξ»ΪΖ¥”Π…ζ≥…MgOΓΔMg3N2ΉΣ“ΤΒγΉ” ΐΈΣ2 NA
D.±ξΉΦΉ¥Ωωœ¬Θ§11.2 LΒΡ““œ©÷–Κ§”–ΒΡΙ≤”ΟΒγΉ”Ε‘ ΐΈΣNA
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΙΊ”Ύ”–ΜζΜ·ΚœΈο![]() ΚΆ
ΚΆ![]() ΒΡΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
ΒΡΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.Εΰ’ΏΒΡ“Μ¬»¥ζΈοΨυ”–6÷÷B.Εΰ’ΏΨυΡήΖΔ…ζ»Γ¥ζΖ¥”ΠΓΔΦ”≥…Ζ¥”ΠΚΆ―θΜ·Ζ¥”Π
C.Εΰ’ΏΩ…”ΟΥα–‘ΗΏΟΧΥαΦΊ»ή“Κ«χΖ÷D.![]() Ζ÷Ή”÷–Υυ”–ΧΦ‘≠Ή”“ΜΕ®‘ΎΆ§“ΜΤΫΟφ…œ
Ζ÷Ή”÷–Υυ”–ΧΦ‘≠Ή”“ΜΕ®‘ΎΆ§“ΜΤΫΟφ…œ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”–ΜζΜ·ΚœΈο‘Ύ»Υάύ…ζΜνΚΆ…ζ≤ζ÷–±Ί≤ΜΩ……ΌΘ§œ¬Ν–Ε‘”–ΜζΜ·ΚœΈοΒΡ–π ω≤Μ’ΐ»ΖΒΡ «( )
A.ΦΉΆι «Χλ»ΜΤχΒΡ÷ς“Σ≥…Ζ÷Θ§ «ΉνΦρΒΞΒΡΧΰΘ§ΤδΚ§ΧΦΝΩΈΣ75%
B.““¥ΦΒΡΖ÷Ή” ΫΈΣ![]() Θ§≥ΘΈ¬œ¬ «“Μ÷÷Έό…Ϊ“ΚΧεΘ§ΟήΕ»±»Υ°–Γ
Θ§≥ΘΈ¬œ¬ «“Μ÷÷Έό…Ϊ“ΚΧεΘ§ΟήΕ»±»Υ°–Γ
C.““ΥαΒΡΫαΙΙΦρ Ϋ «![]() Θ§“Ή»ή”ΎΥ°Θ§Υα–‘±»
Θ§“Ή»ή”ΎΥ°Θ§Υα–‘±»![]() ΒΡ«Ω
ΒΡ«Ω
D.““œ© «÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΘ§Ρή ΙδεΥ°ΚΆΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΘ§Τδ‘≠άμΨυ «““œ©ΨΏ”–Τ·ΑΉΉς”Ο
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΖœΨ…νήΫπ τΤ§÷–ΒΡνή”–ΘΪ2 ΦέΚΆΘΪ3 ΦέΘ§ΜΙΚ§”–ΟΧΓΔΧζΓΔΗΤΓΔΟΨΓΔ¬ΝΒ»Ϋπ τ‘ΣΥΊΦΑΧΦΖέΒ»Θ§ΜΊ ’νήΒΡΙΛ“’Νς≥ΧΘΚ
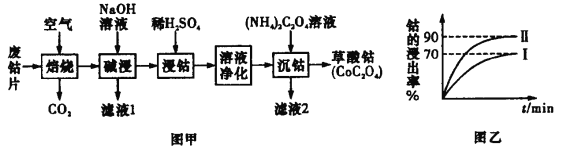
“―÷ΣΘΚΔΌ±Κ…’Κσ Mn ‘ΣΥΊΒΡΜ·ΚœΦέΈΣ+2
ΔΎ
Έο÷ | MgF2 | CaF2 | CoF2 | MgC2O4 | CaC2O4 | CoC2O4 |
»ήΕ»Μΐ | 4ΓΝ10Θ≠9 | 5.3ΓΝ10Θ≠9 | 4ΓΝ10Θ≠3 | 5ΓΝ10Θ≠6 | 6.4ΓΝ10Θ≠9 | 1.7ΓΝ10Θ≠7 |
(1)±Κ…’ ±ΈΣΝΥ ΙΖœΨ…νήΫπ τΤ§≥δΖ÷Ζ¥”ΠΘ§Ω…≤…»ΓΒΡ¥κ © «_____________Θ®»Έ–¥“ΜΧθΘ©ΓΘ
(2)¬Υ“Κ 1 Κ§”–ΒΡ“θάκΉ” « ____________ ΓΘ
(3)ΗΟΝς≥Χ÷–Ϋΰνή ±Θ§νήΒΡΫΰ≥ω¬ ΉνΗΏ÷ΜΡή¥οΒΫ 70ΘΞΘ§Κσά¥ΗΡΫχΖΫΖ®Θ§Φ”»κ Ι”ΟΝρΥαΫχ––ΒΎ“Μ¥ΈΫΰ»ΓΚσΘ§ ‘ΌΦ”»κ Na2SO3 »ή“ΚΫχ––ΒΎΕΰ¥ΈΫΰ»ΓΘ§¥”Εχ ΙνήΒΡΫΰ≥ω¬ ¥ο 90ΘΞ“‘…œΘ§–¥≥ωΒΎΕΰ¥ΈΫΰ≥ωνή ±»ή“Κ÷–ΖΔ…ζΖ¥ ”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ___________________
(4)ΨΜΜ·»ή“ΚΒΡ≤ΌΉς÷–Κ§”–ΕύΗω≤Ϋ÷ηΘ§œ»≥ΐΧζΚσ≥ΐΟΧΓΘ
ΔΌ≥ΐΧζΘΚ≥ΘΈ¬œ¬Θ§ΒςΫΎ»ή“Κ pH ΈΣ 1Θ°5ΓΪ2Θ°0 ΚσΘ§Φ” H2O2Θ§Ζ¥”Π“ΜΕΈ ±ΦδΘ§Φ” 8ΘΞNa2CO3 »ή“ΚΘ§ΫΪ»ή“Κ ΒΡ pH Βς÷Ν 4Θ°0ΓΪ5Θ°0ΓΘ«κ”ΟΜ·―ßΤΫΚβ“ΤΕ·‘≠άμΫβ ΆΦ”»κ Na2CO3 »ή“ΚΡή≥ΐ»Ξ»ή“Κ÷–Χζ‘ΣΥΊΒΡ‘≠“ρ____________ΓΘ
ΔΎ≥ΐΟΧΘΚΦ”»κ NaClO »ή“ΚΓΘ–¥≥ωΗΟάκΉ”ΖΫ≥Χ ΫΘΚ___________________ΓΘ
ΔέΦθΗΤΟΨΘΚΦ”»κ NH4F »ή“ΚΘ§≥ΝΒμ¥σ≤ΩΖ÷ΒΡΗΤΓΔΟΨΒΡάκΉ”ΓΘ ‘Ϋβ ΆΈΣΚΈ≤ίΥαοß»ή“Κ≥Ννή«Α“ΣΦθΗΤΟΨΘΚ_____ΓΘ
(5) ςΒ¬÷–―ßΜ·―ß–Υ»Λ–ΓΉι”ϊΧΫΨΩ CoC2O42H2O ή»»ΚσΒΡΖ÷Ϋβ≤ζΈοΘ§»Γ 5.49gCoC2O42H2OΘ®ΡΠΕϊ÷ ΝΩΈΣ183g/molΘ©”Ύ”≤÷ ≤ΘΝßΙή÷–Φ”»»“ΜΕΈ ±ΦδΘ§ά以ΓΔ≥ΤΝΩΘ§ Θ”ύ―θΜ·ΈοΙΧΧεΒΡ÷ ΝΩΈΣ 2.41gΓΘ ι–¥ CoC2O42H2O ή»»Ζ÷ΫβΒΡΜ·―ßΖΫ≥Χ Ϋ___________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣΡ≥÷÷»ΦΝœΚ§”–ΧΦΓΔ«βΓΔ―θ»ΐ÷÷‘ΣΥΊΓΘΈΣΝΥ≤βΕ®’β÷÷»ΦΝœ÷–ΧΦΚΆ«βΝΫ÷÷‘ΣΥΊΒΡ÷ ΝΩ±»Θ§Ω…ΫΪΤχΧ§»ΦΝœΖ≈»κΉψΝΩΒΡO2÷–»Φ…’Θ§≤ΔΫΪ≤ζ…ζΒΡΤχΧε»Ϊ≤ΩΆ®ΙΐΆΦ ΨΉΑ÷ΟΘ§ΒΟΒΫ»γ±μΥυΝ–ΒΡ Β―ι ΐΨί(≤ζ…ζΒΡΤχΧεΆξ»Ϊ±ΜΈϋ ’)ΓΘ

Β―ι«Α | Β―ιΚσ | |
(Η…‘οΦΝΘΪU–ΈΙή)ΒΡ÷ ΝΩ | 101.1g | 102.9g |
(≥Έ«ε ·Μ“Υ°ΘΪΙψΩΎΤΩ)ΒΡ÷ ΝΩ | 312.0g | 314.2g |
ΗυΨί Β―ι ΐΨίΧνΩ’ΘΚ
Θ®1Θ© Β―ιΆξ±œΚσΘ§…ζ≥…Έο÷–Υ°ΒΡ÷ ΝΩΈΣ____gΘ§ΦΌ…ηΙψΩΎΤΩάο…ζ≥…“Μ÷÷’ΐ―ΈΘ§Τδ÷ ΝΩΈΣ______gΓΘ
Θ®2Θ©…ζ≥…ΒΡΥ°÷–«β‘ΣΥΊΒΡ÷ ΝΩΈΣ________gΓΘ
Θ®3Θ©…ζ≥…ΒΡCO2÷–ΧΦ‘ΣΥΊΒΡ÷ ΝΩΈΣ________gΓΘ
Θ®4Θ©ΗΟ»ΦΝœ÷–ΧΦΓΔ«β‘ΣΥΊ÷ ΝΩ±»ΈΣ________Θ°
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com