
【题目】某种食品的配料标签如图所示:
(1)该配料中,富含蛋白质的物质是_________,富含油脂的物质是________;
(2)该配料中的________有防腐作用。碳酸氢钠受热分解,产生的气体使食品膨松,该过程的化学方程式为_________;
(3)用于包装该食品 的聚乙烯塑料包装属于_________(填字母);
a.有机高分子材料 b.无机非金属材料 c.金属材料

科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为_____________
(2)W与Y 可形成化合物W2Y,该化合物的电子式为________________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_________________________。Y的最高价氧化物是否满足8电子稳定结构______________(填是.否)
(4)比较Y、Z气态氢化物的稳定性由大到小的顺序是________________(用分子式表示)。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是
____________________________________________________。(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol·L-1NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
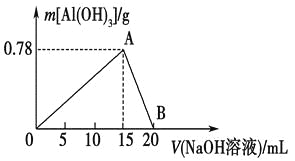
(1)图中A点表示的意义是_________________________。
(2)图中B点表示的意义是_________________________。
(3)上述两步反应用总的离子方程式可表示为:____________________________。
(4)若所得Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱顺序是CH3COOH>H2CO3>C6H5OH。
(1)利用如图所示的仪器可以组装实验装置,则仪器的连接顺序是____接D、E接_____、______接_____。
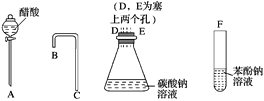
(2)有关反应的化学方程式为________________________________________________。
(3)有的同学认为此装置不能验证H2CO3和C6H5OH的酸性强弱,你认为________(填“有”或“没有”)道理。怎样改进实验才能验证H2CO3和C6H5OH的酸性强弱?
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下:
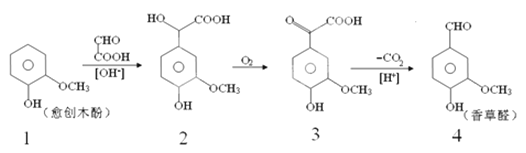
下列说法正确的是( )
A. 反应1→2属于加成反应,且生成的化合物2具有一个手性碳原子
B. 化合物2在一定条件下可发生消去反应
C. 检验制得的香草醛中是否混有化合物3,可用氯化铁溶液
D. 等物质的量四种化合物分别与足量NaOH反应,消耗NaOH物质的量之比为1:3:2:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示(明矾石焙烧后成分不变):
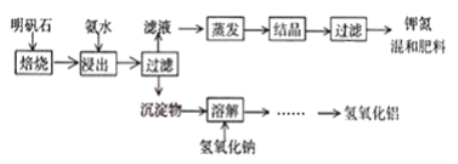
完成下列填空:
(1)“浸出”反应的离子方程式为_______。“浸出”所用稀氨水浓度为39.20g/L,配制500mL该氨水需251.28g/L的浓氨水________mL。
(2)“过滤”所需的玻璃仪器有______________。
(3)写出“溶解”过程中发生反应的化学方程式_________、________。
(4)检验滤液中是否含有SO42-的实验方法__________。
(5)为测定钾氨复合肥K2SO4、(NH4)2SO4中SO42-的质量分数,设计实验步骤如下:
①_____________________。
②溶于水,加入足量BaCl2溶液,待白色沉淀不再产生为止。
③过滤、______、________(依次填写实验操作名称)。
④冷却、称量所得沉淀的质量。
(6)若所取试样和所得沉淀的质量分别为mg、ng,试用含有m、n的代数式表示该钾氮复合肥中SO42-的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA是阿伏加德罗常数的值,下列说法正确的是
A.12gNaHSO4晶体中SO42-数目为0.1NA
B.2.0gD2O中含有的中子数为NA
C.2.24LCl2与足量Na2SO3溶液反应时转移的电子数为0.2NA
D.标准状况下,4.48 LHF所含原子数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸是合成阿司匹林的重要原料。水杨酸的学名邻羟基苯甲酸,结构简式为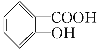 ,请回答下列问题:
,请回答下列问题:
(1)请写出水杨酸中具有的官能团名称________;
(2)能够区分水杨酸和苯酚的试剂_____ ___;
A.浓溴水 B.氢氧化钠溶液 C.氯化铁溶液 D.碳酸氢钠溶液
(3)水杨酸的另一种同分异构体的结构简式为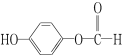 ,1 mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)________;
,1 mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)________;
A.1 mol B.2 mol C.3 mol D.4 mol
(4)已知有机物CH3COOH可以表示为:![]() ,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为:
,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为: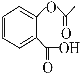 ,则阿司匹林分子式为________;
,则阿司匹林分子式为________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿(主要成分为![]() ,含少量
,含少量![]() 和
和![]() 等杂质)为原料生产铝和氮化铝的一种工艺流程如图[已知:
等杂质)为原料生产铝和氮化铝的一种工艺流程如图[已知:![]() 在“碱溶”时转化为铝硅酸钠(
在“碱溶”时转化为铝硅酸钠(![]() )沉淀]。
)沉淀]。
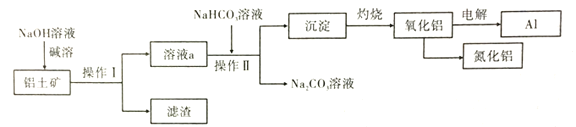
(1)用氧化物的形式表示铝硅酸钠的化学式____。
(2)溶液a中加入![]() 后,生成沉淀的离子方程式为___。
后,生成沉淀的离子方程式为___。
(3)有人考虑用熔融态![]() 电解制备铝,你觉得是否可行?请说明理由:___。
电解制备铝,你觉得是否可行?请说明理由:___。
(4)取一定量的氮化铝样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开![]() ,加入NaOH浓溶液,至不再产生
,加入NaOH浓溶液,至不再产生![]() 。打开
。打开![]() ,通入
,通入![]() 一段时间。
一段时间。
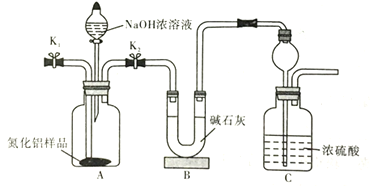
①写出AlN与NaOH溶液反应的化学方程式______。
②实验中需要测定的数据是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com