
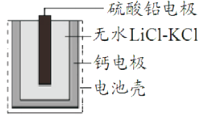
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,无水LiCl-KCl混合物受热熔融后,电池即可瞬间输岀电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法不正确的是
A. 放电时,电子由Ca电极流出
B. 放电时,Li+向PbSO4电极移动
C. 负极反应式:PbSO4+2e-+Li+=Li2SO4+Pb
D. 每转移0.2mol电子,理论上生成还原产物Pb的质量为20.7g
【答案】C
【解析】
由原电池总反应可知,Ca为原电池的负极,被氧化生成CaCl2,电极方程式为Ca+2Cl--2e-=CaCl2,PbSO4为原电池的正极,发生还原反应,电极方程式为PbSO4+2e-+2Li+=Li2SO4+Pb,原电池工作时,阳离子向正极移动,阴离子向负极移动。
A、由原电池总反应可知,Ca为原电池的负极,电子由负极Ca电极流出,故A正确;
B、放电过程中阳离子向正极PbSO4电极移动,故B正确;
C、Ca为原电池的负极,被氧化生成CaCl2,反应的电极方程式为Ca+2Cl--2e-=CaCl2,故C错误;
D、根据电极方程式PbSO4+2e-+2Li+=Li2SO4+Pb可知,每转移0.2mol电子,理论上生成0.1molPb,质量为20.7g,故D正确;
故选:C。


科目:高中化学 来源: 题型:
【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去)。
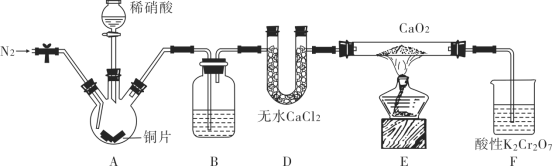
已知:2NO+CaO2=Ca(NO2)2 ;2NO2+CaO2=Ca(NO3)2 。
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因是_____________。
(2)仪器D的名称是______________;B中盛装的试剂是__________。
(3)装置F中,酸性K2Cr2O7溶液可将剩余的NO氧化成NO![]() ,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为____________________________________________________________。
,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式为____________________________________________________________。
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体。设计实验证明E中有亚硝酸钙生成_____________________________________________________________。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,反应原理为Ca(OH)2+NO+NO2=Ca(NO2)2+H2O。
①若n(NO)∶n(NO2)>1∶1,则会导致______________________________________________;
②若n(NO)∶n(NO2)<1∶1,则会导致______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬酸(用H3R表示)可用作酸洗剂。常温下,向0.1mol·L1 H3R溶液中加入少量的NaOH固体(忽略溶液体积的变化),H3R、H2R、HR2和R3的含量与pH的关系如图所示。下列正确的是
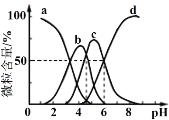
A. 图中b曲线表示HR2的变化
B. HR2的电离常数Ka3=106
C. pH=7时,c(Na+)=c(H2R)+c(HR2)+c(R3)
D. pH=5时,c(H2R)+c(HR2)+c(R3)=0.1mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图表示4个碳原子相互结合的几种方式。小圆球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都与氢结合。

(1)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成________和三键;不仅可以形成碳链,还可以形成碳环。
(2)上图中互为同分异构体的是:A与____;D与____,与B互为同分异构体但不属于同种类的物质的是_____。(填编号)
(3)写出F与溴水加成的反应方程式_________________。
Ⅱ.某有机物气体含碳82.7%,含氢17.3%,在标准状况下它的密度是2.59g/L。则该有机物可能的结构简式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
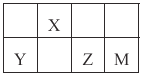
【题目】四种短周期元素X、Y、Z和M在周期表中的位置如图所示,Y原子序数是X的2倍。下列说法不正确的是
A. Z、M、X的简单离子半径依次减小
B. Y和M可形成离子化合物YM4
C. X的简单气态氢化物的稳定性强于Y的
D. M的最高价氧化物对应水化物的酸性比Z的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A是来自石油的重要有机化工原料,A的产量可以用来衡量一个国家石油化工发展水平。E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。
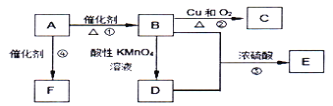
(1)A的结构式为________,F的结构简式为__________。
(2)写出下列反应的反应类型:①________;③_________;
(3)写出反应②的化学方程式____________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H为
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2SO3溶液中混有 NaHSO3,要提纯Na2SO3溶液,可用三室法电解实现,如图所示。下列说法不正确的是
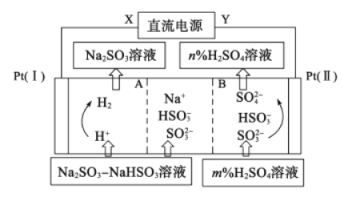
A. A为阳离子交换膜,B为阴离子交换膜
B. X为直流电源的负极,阳极区pH减小
C. 图中的n<m
D. 阴极的电极反应式为2H++2e-=H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com