
| A�� | ��c��CO32-��=0.1 mol•L-1����Һ�У�K+��AlO2-��Cl-��NO3- | |
| B�� | �ڳ�������ˮ�������c��OH-��=1��10-12 mol•L-1����Һ�У�Fe2+��ClO-��Na+��SO42- | |
| C�� | �ڼ��뱽�ӻ�����ɫ����Һ�У�NH4+��Cl-��Na+��SCN- | |
| D�� | ����ʹ��ɫʯ����ֽ������Һ�У�S2O32-��CO32-��Na+��K+ |
���� A����������֮�䲻��Ӧ��
B����������ˮ�������c��OH-��=1��10-12 mol•L-1����Һ��Ϊ������Һ��
C�����뱽�ӻ�����ɫ����Һ���������ӣ�
D����ʹ��ɫʯ����ֽ������Һ�������ԣ�
��� �⣺A����������֮�䲻��Ӧ���ɴ������棬��A��ȷ��
B����������ˮ�������c��OH-��=1��10-12 mol•L-1����Һ��Ϊ������Һ��������Һ�в��ܴ�������Fe2+������Һ��Fe2+��ClO-����������ԭ��Ӧ�����ܹ��棬��B����
C�����뱽�ӻ�����ɫ����Һ���������ӣ���SCN-�������������ӣ����ܹ��棬��C����
D����ʹ��ɫʯ����ֽ������Һ�������ԣ����ܴ�������S2O32-��CO32-����D����
��ѡA��
���� ���⿼�����ӹ��棬Ϊ��Ƶ���㣬����ϰ���е���Ϣ������֮��ķ�ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�⸴�ֽⷴӦ����Ϸ�Ӧ��������ԭ��Ӧ���жϣ���Ŀ�ѶȲ���


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 �����������еĻ�ѧ������Ϊ���Ӽ������ۼ���
�����������еĻ�ѧ������Ϊ���Ӽ������ۼ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����ᣨHNO2����һԪ���ᣬ�����ἰ������ʵ���ҵ����������ҪӦ�ã���ش�
�����ᣨHNO2����һԪ���ᣬ�����ἰ������ʵ���ҵ����������ҪӦ�ã���ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 35.9g | B�� | 30.8g | C�� | 28.1g | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
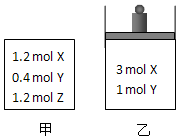 ���¶ȡ���ʼ�ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���ͼ��ʾ�����������·�Ӧ��3X��g��+Y��g��?2Z��g����H��0�������¶Ȳ��䣬���ƽ��ʱ���й��������������˵����ȷ���ǣ�������
���¶ȡ���ʼ�ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���ͼ��ʾ�����������·�Ӧ��3X��g��+Y��g��?2Z��g����H��0�������¶Ȳ��䣬���ƽ��ʱ���й��������������˵����ȷ���ǣ������� | ���������� | ��ѹ������ | |
| X�����ʵ�����mol�� | n1 | n2 |
| Z��������� | ��1 | ��2 |
| A�� | ƽ��ʱ�����ҵ��ݻ�һ���ȷ�ӦǰС | |
| B�� | ƽ��ʱ������ѹǿһ���ȷ�ӦǰС | |
| C�� | n2��n1 | |
| D�� | ��2����1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1 mol NH4NO3����ϡ��ˮ��ʹ��Һ�����ԣ���Һ��NH4+��ĿΪNA | |
| B�� | 60 g SiO2���еĻ�ѧ����ĿΪ4NA | |
| C�� | CO2ͨ��Na2O2ʹ������a gʱ����Ӧ��ת�Ƶĵ�����ΪaNA/56 | |
| D�� | ���³�ѹ�£�14.9 g KCl��NaClO�Ĺ��������������ӵ���ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com