
【题目】如图是铁钉在某溶液中被腐蚀的实验(开始时试管中液面和试管外液面等高). 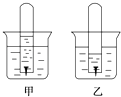
(1)甲、乙两图溶液中呈酸性的是(填“甲”或“乙”).
(2)甲图电极反应式是:正极 , 负极 .
(3)乙图中发生反应的离子方程式是 .
【答案】
(1)乙
(2)O2+2H2O+4e﹣═4OH﹣; Fe﹣2e﹣═Fe2+
(3)Fe+2H+═Fe2++H2↑
【解析】解:从两图中液面的高度可以看出,甲图试管内液面上升,说明气体体积减小,氧气被吸收,发生吸氧腐蚀,乙图试管内液面下降,说明气体体积增大,有氢气生成,发生析氢腐蚀,(1)由以上分析可知乙发生析氢腐蚀,溶液呈酸性,所以答案是:乙;(2)甲发生吸氧腐蚀,正极发生还原反应,电极方程式为O2+2H2O+4e﹣═4OH﹣,负极发生氧化反应,电极方程式为Fe﹣2e﹣═Fe2+,
所以答案是:O2+2H2O+4e﹣═4OH﹣;Fe﹣2e﹣═Fe2+;(3)乙发生析氢腐蚀,铁被氧化,同时生成氢气,离子方程式为Fe+2H+═Fe2++H2↑,所以答案是:Fe+2H+═Fe2++H2↑.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】酮洛芬是一种良好的抗炎镇痛药,可以通过以下方法合成:

(1)化合物D中所含官能团的名称为__________________和_____________________。
(2)化合物E的结构简式为__________________;由B→C的反应类型是____________。
(3)写出C→D的反应方程式____________________________________。
(4)B的同分异构体有多种,其中同时满足下列条件的有_____种。
I.属于芳香族化合物
II.能发生银镜反应
III.其核磁共振氢谱有5组波峰,且面积比为1:1:1:1:3
(5)请写出以甲苯为原料制备化合物![]() 的合成路线流程图____(无机试剂可任选)。合成路线流程图示例如图:
的合成路线流程图____(无机试剂可任选)。合成路线流程图示例如图:![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电动公交车替代燃油公交车是节能减排、控制雾霾的重要举措之一,下图所示电池是一种正在开发的车载电池。有关该电池的说法正确的是
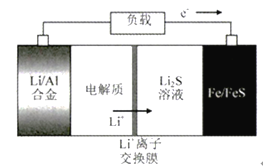
A. 放电时Fe/FeS极是负极
B. 放电时负极反应式为:Al-3e-=Al3+
C. 充电时阳极反应式为:Fe+S2--2e-=FeS
D. 左边电解质可以是LiOH的醇溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜广泛应用于有机合成、石油、油脂、染料等工业。以某种铜矿粉(含Cu2S、CuS及FeS等)为原料制取CuCl的工艺流程如下:
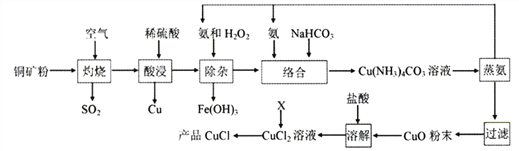
已知:①CuS、Cu2S、FeS灼烧固体产物为Cu2O、FeO;
②Ksp(CuCl)=2×10-7,2Cu+=Cu+Cu2+的平衡常数K1=1×106
回答下列问题:
(1)“灼烧”时,被还原的元素有____________(填元素符号)。
(2)“酸浸”所需H2SO4是用等体积的98%H2SO4和水混合而成。实验室配制该硫酸溶液所需的玻璃仪器除玻璃棒、胶头滴管外,还有_______。“酸浸”时硫酸不宜过多的原因是__________________。
(3)“除杂”的总反应方程式是_____________________。
(4)“络合”反应中的NH3与NaHCO3理论比值是____________________。
(5)加热“蒸氨”在减压条件下进行的原因是________________。
(6)X可以充分利用流程中的产物,若X是SO2时,通入CuCl2溶液中反应的离子方程式是________________;若X是Cu时,反应Cu+Cu2++2Cl-=2CuCl的平衡常数K2=_________。
(7)以铜为阳极电解NaCl溶液也可得到CuCl,写出阳极电极反应式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果、葡萄、西瓜、山楂是人们普遍喜爱的水果,这些水果富含一种有机物 A,又知A的分子式为C4H6O5。为了弄清该有机物的结构,某兴趣小组的同学做了以下实验:
①该化合物与氢氧化钠溶液反应会生成正盐和酸式盐两种产物;
②该化合物既能与羧酸反应产生有香味的物质,又能与醇反应产生有香味的物质;
③1mol该有机物与足量金属钠反应产生1.5 mol H2;
④利用仪器测知A分子中不含有甲基(—CH3)。请回答下列问题:
(1)根据以上实验结果,对A的结构可作出的判断是________。
A.肯定有碳碳双键 B.有两个羧基
C.肯定有羟基 D.有两个“CH2”基团
(2)有机物A的结构简式为__________________________。
(3)写出A与足量氢氧化钠溶液反应的化学方程式:________________________________。
(4)写出A与金属钠反应的化学方程式:____________________________________。
(5) 写出A与乙酸发生酯化反应的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)羟基的电子式;
(2)相对分子质量为72且沸点最低的烷烃的结构简式;
(3)合成高聚物  其单体的结构简式;
其单体的结构简式;
(4)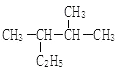 的名称(系统命名法) .
的名称(系统命名法) .
(5)甲烷具有型的空间结构,而乙炔则具有型空间结构.
(6)苯酚遇FeCl3溶液会显色;蛋白质与浓硝酸共热会变色;淀粉遇碘则显色.这些特性常被用于物质的检验或鉴别.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++OH-=H2O来表示的化学反应是( )
A.氢氧化镁和稀盐酸反应
B.Ba(OH)2溶液滴入稀硫酸中
C.澄清石灰水和稀硝酸反应
D.二氧化碳通入澄清石灰水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组探究电解FeCl2溶液的电极反应产物
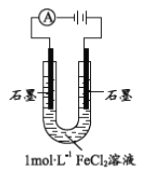
(1)配制1molL-1FeCl2溶液,测得pH=4.91,原因______(用离子方程式表示)。从化合价角度分析, Fe2+具有________。
(2)该小组同学预测电解FeCl2溶液两极的现象:阳极有黄绿色气体产生,阴极有无色气体产生。
该小组同学用右图装置电解1molL-1FeCl2溶液:
①取少量银灰色固体洗涤后,加稀H2SO4有气泡产生,再向溶液中加入________(试剂和现象),证明该固体为Fe。
②该小组同学进一步分析红褐色固体产生的原因,甲同学认为________;乙同学认为2Cl- - 2e- = Cl2↑,Cl2可氧化Fe2+最终生成Fe(OH)3 。
为证实结论,设计方案如下:用实验Ⅰ的装置和1.5v 电压,电解酸化(pH=4.91)的_______,通电5分钟后,阳极无明显现象,证实乙同学的推论不正确。丙同学认为仍不严谨,原因是产生的气体溶于水,继续实验________(操作和现象),进一步证实了乙同学的推论不正确。
(3)该小组同学进一步探究电解1molL-1FeCl2溶液电极产物的影响因素。
实验 | 条件 | 操作及现象 | ||
电压 | pH | 阳极 | 阴极 | |
Ⅰ | 1.5v | 4.91 | 无气泡产生,溶液逐渐变浑浊,5分钟后电极表面析出红褐色固体 | 无气泡产生,4分钟后电极表面有银灰色金属状固体附着 |
Ⅱ | 1.5v | 2.38 | 无气泡产生,溶液出现少量浑浊,滴加KSCN溶液变红色 | 无气泡产生,电极表面有银灰色金属状固体附着 |
Ⅲ | 1.5v | 1.00 | 无气泡产生,溶液无浑浊现象,滴加KSCN溶液变红色 | 有气泡产生,无固体附着 |
Ⅳ | 3.0v | 4.91 | 无气泡产生,溶液逐渐变浑浊,3分钟后电极表面有红褐色固体产生 | 极少量气泡产生,1分钟出现镀层金属 |
Ⅴ | 6.0v | 4.91 | 有气泡产生,遇湿润的淀粉碘化钾试纸变蓝。溶液逐渐变浑浊 | 大量气泡产生,迅速出现镀层金属 |
①对比实验Ⅰ、Ⅱ、Ⅲ可以得出结论:
阳极Fe2+放电时,酸性较强主要生成Fe3+; 酸性较弱主要生成Fe(OH)3 。阴极________。
②对比实验Ⅰ、Ⅳ、Ⅴ可以得出结论:
增大电压,不仅可以改变离子的放电能力,也可以________。
(4)综合分析上述实验,电解过程中电极反应的产物与________有关 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com