
 ����������N2H4���ǵ������ֳ���������ڹ�ũҵ����������Ҫ��Ӧ�ã�
����������N2H4���ǵ������ֳ���������ڹ�ũҵ����������Ҫ��Ӧ�ã� [N2H5•H2O]++H+��������������Һ�е�����Ũ�ȹ�ϵ��ȷ����ac������ţ���
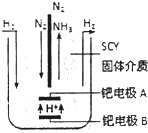
[N2H5•H2O]++H+��������������Һ�е�����Ũ�ȹ�ϵ��ȷ����ac������ţ������� ��1��B�缫������ʧȥ�������������ӣ�����������Ӧ��BΪ������AΪ������������������õ��ӣ���SCY�մɴ��ݵ�H+������ɰ�����
��2���������֪��������������Ӧ����NH2Cl��HCl��������NH2Cl��Ӧ����N2H4��HCl��
��3���⻯���У�Nԭ����=43.0��0.977��14=3��Hԭ����=43.0��0.023��1=1���ʷ���ʽΪHN3��ײ��������Ӧ��2HN3=H2+3N2�����ݷ���ʽ�����������������
��4����ˮ����NH4Cl���ƣ���N2H62+ˮ����H2O�������ɵ�OH-�õ�[N2H5•H2O]+��
a��N2H62+����ˮ����Һ�����ԣ�
b��N2H62+����ˮ����Һ�����ԣ���ˮ��̶�������Һ��������Դ��N2H62+����ˮ�⼰ˮ�ĵ��룻
c�����ݵ���غ��жϣ�
d�����������غ��жϣ�
��� �⣺��1��B�缫������ʧȥ�������������ӣ�����������Ӧ��BΪ���������ӵ�Դ��������AΪ������������������õ��ӣ���SCY�մɴ��ݵ�H+������ɰ����������缫��ӦʽΪ��N2+6e-+6H+=2NH3��
�ʴ�Ϊ������N2+6e-+6H+=2NH3��
��2���������֪��������������Ӧ����NH2Cl��HCl��������NH2Cl��Ӧ����N2H4��HCl����Ӧ����ʽΪ��Cl2+NH3=NH2Cl+HCl��NH3+NH2Cl=N2H4+HCl��
�ʴ�Ϊ��Cl2+NH3=NH2Cl+HCl��NH3+NH2Cl=N2H4+HCl��
��3���⻯���У�Nԭ����=43.0��0.977��14=3��Hԭ����=43.0��0.023��1=1���ʷ���ʽΪHN3��ײ��������Ӧ��2HN3=H2+3N2��4.30g���⻯������ʵ���Ϊn=$\frac{4.3g}{43g/mol}$=0.1mol�����ݷ���ʽ��֪����������������ʵ���Ϊ0.1mol��2=0.2mol�����Ϊ0.2mol��22.4L/mol=4.48L��
�ʴ�Ϊ��HN3��4.48��
��3����ˮ����NH4Cl���ƣ���N2H62+ˮ����H2O�������ɵ�OH-�õ�[N2H5•H2O]+�������µ�һ��ˮ�ⷴӦ�����ӷ���ʽΪ��N2H62++H2O [N2H5•H2O]++H+��
[N2H5•H2O]++H+��
a��N2H62+ˮ�������ԣ�ˮ��ij̶Ⱥ�����������Ũ�ȵĴ�С��ϵΪc��Cl-����c��N2H62+����c��H+����c��OH-������a��ȷ��
b��N2H62+����ˮ����Һ�����ԣ���ˮ��̶�������Һ��������Դ��N2H62+����ˮ�⼰ˮ�ĵ��룬��c��Cl-����c��H+����c��[N2H5•H2O]+����c��OH-������b��ȷ��
c�����ݵ���غ�ɵã�2c��N2H62+��+c��[N2H5•H2O+]��+c��H+��=c��Cl-��+c��OH-������c����
d�����������غ�c��Cl-��=2c��N2H62+��+2c��[N2H5•H2O]+��+2c��[N2H4•2H2O]������d����
�ʴ�Ϊ��N2H62++H2O [N2H5•H2O]++H+��ab��
[N2H5•H2O]++H+��ab��
���� ���⿼����ԭ������ѧ����ʽ���㡢����ˮ��ȣ���Ŀ�ز�İ�������ؿ���ѧ����Ϣ��ȡ��֪ʶ��Ǩ�����ã��Ѷ��еȣ�


 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
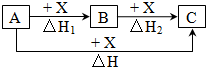 һ��������A��B��C����ͼ��ʾ��ת����ϵ���ҡ�H=��H1+��H2��������ת����ϵ��A��C�����Ǣ�Fe��FeCl3 ��C��CO2 ��AlCl3��NaAlO2 ��NaOH��NaHCO3 ��S��SO3 ��Na2CO3��CO2��������
һ��������A��B��C����ͼ��ʾ��ת����ϵ���ҡ�H=��H1+��H2��������ת����ϵ��A��C�����Ǣ�Fe��FeCl3 ��C��CO2 ��AlCl3��NaAlO2 ��NaOH��NaHCO3 ��S��SO3 ��Na2CO3��CO2��������| A�� | ֻ�Тڢۢܢ� | B�� | ������ | C�� | ������ | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | һ��ʱ���ͭƬ���أ�������K+����CuSO4��Һ | |
| B�� | ������ӦΪ��Zn-2e-�TZn2+ | |
| C�� | ���Ӵ�ͭƬ����������пƬ | |
| D�� | ��ع���ʱZn2+��Cu2+ ��Ũ�ȱ��ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶� | B�� | �ʵ�����ѹǿ | ||
| C�� | ������� | D�� | ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ���ǿ����Һ�ķ�Ӧ������Ƴ�ԭ��� | |
| B�� | ��������п��������ʱ��������Һ�Ӵ���п����ʴ | |
| C�� | �����ڷ����ķ�Ӧ��Ϊ�Է����е�������ԭ��Ӧ | |
| D�� | �ö��Ե缫�����������ʳ��ˮ�ɼ�����ʹ��Һ�ָ���ԭ״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ô���SO2Ư������ | |
| B�� | ��С�մ�NaHCO3�����Ƹ�� | |
| C�� | ��ʳ����ϴ��ˮƿ���ڱڸ��ŵ�ˮ����CaCO3�� | |
| D�� | ������Һ����Ч�ɷ�NaClO���Բ;߽���ɱ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �Լ� | |
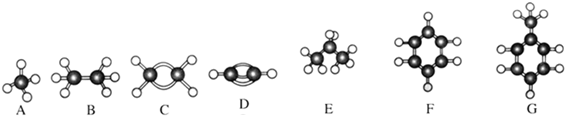
| �������������ϩ | |
| �屽���������嵥�� |
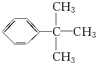 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4 | B�� | Cl2 | C�� | Na2O2 | D�� | SO2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com