
| ||
| ||


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发 | B、分液 | C、过滤 | D、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
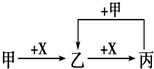 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X(要求甲和X能互换)不可能是[提示:Al3++3AlO2-+6H2O=4Al(OH)3↓]( )
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X(要求甲和X能互换)不可能是[提示:Al3++3AlO2-+6H2O=4Al(OH)3↓]( )| A、C和O2 |
| B、SO2和NaOH溶液 |
| C、Cl2和Fe |
| D、AlCl3溶液和NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
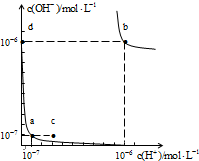
| A、图中对应点的温度关系为:a>b |
| B、水的离子积常数Kw数值大小关系为:b>d |
| C、温度不变,加入少量NaOH可使溶液从a点变到c点 |
| D、在b点对应的温度下,pH=6的溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大压强,使活化分子数目增加,化学反应速率一定增大 |
| B、活化分子间所发生的分子间碰撞均为有效碰撞 |
| C、升高温度,使活化分子百分数增加,化学反应速率一定增大 |
| D、加入反应物,使活化分子百分数增加,化学反应速率一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、Na2O2既是氧化剂又是还原剂 |
| B、3 mol Na2O2发生反应,有6mol电子转移 |
| C、在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌 |
| D、Na2FeO4既是氧化产物又是还原产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com