
正极材料为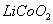
 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
(1) 橄榄石型
橄榄石型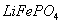 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过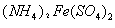 、
、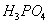 与
与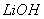 溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成 型而制得。
型而制得。
①共沉淀反应投料时,不将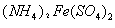 和
和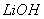 溶液直接混合的原因是 。
溶液直接混合的原因是 。
②共沉淀反应的化学方程式为 。
③高温成型前,常向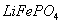 中加入少量活性炭黑,其作用除了可以改善成型后的
中加入少量活性炭黑,其作用除了可以改善成型后的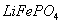 的导电性能外,还能 。
的导电性能外,还能 。
(2)废旧锂离子电池的正极材料试样(主要含有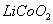 及少量AI、Fe等)可通过下列实验方法回收钴、锂。
及少量AI、Fe等)可通过下列实验方法回收钴、锂。
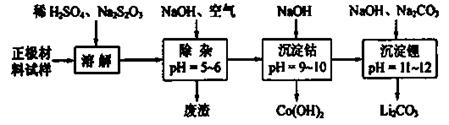
① 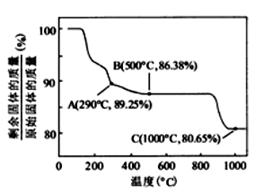 在上述溶解过程中,
在上述溶解过程中,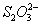 被氧化成
被氧化成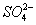 ,
,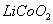 在溶解过程中反应的化学方程式为 。
在溶解过程中反应的化学方程式为 。
② 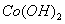 在空气中加热时,固体残留率随温度的变化如右图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为 。(填化学式);在350~400℃范围内,剩余固体的成分为 。(填化学式)。
在空气中加热时,固体残留率随温度的变化如右图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为 。(填化学式);在350~400℃范围内,剩余固体的成分为 。(填化学式)。
【答案】
(1)①Fe2+在碱性条件下更易被氧化(凡合理答案均可)
②(NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4+2NH4HSO4+H2O
③与空气中O2反应,防止LiFePO4中的Fe2+被氧化
(2)
①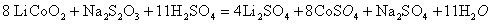
② 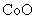
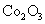 、
、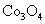
【解析】本题考察的知识比较散,涉及到能源利用,物质性质、化工流程分析,图表分析,覆盖面比较广。(1)①不能直接混合的原因是Fe2+在碱性条件下更容易被氧化;②根据题给的信息,发生的反应为(NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4+2NH4HSO4+H2O③消耗空气中的O2,保护Fe2+,防止Fe2+被氧化;(2)①通过题给信息可知LiCoO2与Na2S2O3发生了氧化还原反应,反应为8 LiCoO2+ Na2S2O3+11H2SO4=4Li SO4+8CoSO4+ Na2SO4+11 H2O②根据质量的变化,在变化过程中,Co的质量没有变,通过题给数据看,在10000C是Co(OH)2完全分解,则产物CoO,在350-4000C时,固体的质量在89.25%-86.38%之间,可以通过极点进行分析,在2920C,n(Cr)n(O)=100/93:(89.25-100*59/93)/16=2:3,其化学式为Co2O3在5000C n(Cr)n(O)= 100/93:(86.38-100*59/93)/16=3:4其化学式为Co3O4 ,所以可以确定在350-4000C时的化学式为Co2O3和Co3O4


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
下列有关同分异构体数目的叙述中,不正确的是( )
A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
B.分子式符合C5H11Cl 的化合物有6种
C.已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种
D.菲的结构简式为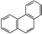 ,它与硝酸反应,可生成5种一硝基取代物
,它与硝酸反应,可生成5种一硝基取代物
查看答案和解析>>
科目:高中化学 来源: 题型:
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
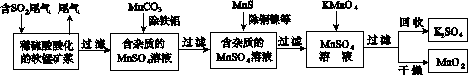
请回答下列问题:
(1)上述流程脱硫实现了____(选填下列字母编号)。
A.废弃物的综合利用
B.白色污染的减少
C.酸雨的减少
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原因是________________________________。
(3)已知:25 ℃、101 kPa时,
Mn(s)+O2(g)===MnO2(s) ΔH=-520 kJ/mol
S(s)+O2(g)===SO2(g) ΔH=-297 kJ/mol
Mn(s)+S(s)+2O2(g)===MnSO4(s)
ΔH=-1065 kJ/mol
SO2与MnO2反应生成无水MnSO4的热化方程式是____________________________________。
(4)MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是________________________________。
(5)MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是________________。
(6)假设脱除的SO2只与软锰矿浆中的MnO2反应。按照图示流程,将a m3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为c kg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
A.2Na2O2+ 2H2O=4NaOH+O2↑ B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
2H2O=4NaOH+O2↑ B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.2F2+2H2O=4HF+O2 D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaOH = ________________.
(2)反应Cl2+Na2SO3+2 NaOH===2NaCl+Na2SO4+H2O中的还原剂为________________.
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl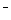 、OH
、OH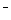 和SO
和SO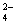 .请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
① 提出合理假设 .
假设1:只存在SO32-;假设2:既不存在SO32-也不存在ClO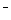 ;假设3:_____________.
;假设3:_____________.
② 设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3moL L-1H2SO4、1moL
L-1H2SO4、1moL L-1NaOH、0.01mol
L-1NaOH、0.01mol L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3 moL |
|
| 步骤2: | |
| 步骤3: |
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是__________________。
(2)已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为__________________。
(3)根据上述反应可推知__________________。
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:

查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示溶液中发生反应的化学方程式错误的是( )
A.2Al+2NaOH+2H2O====2NaAlO2+3H2↑
B.2KMnO4+HCOOK+KOH====2K2MnO4+CO2↑+H2O
C.MnO2+4HCl(浓)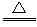 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
D.K2Cr2O7+6FeSO4+7H2SO4====Cr2(SO4)3+3Fe2(SO4)3+K2SO4+7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,氧化剂与还原剂物质的量的关系为1∶2的是
A.O3+2KI+H2O==2KOH+I2+O2
B.2CH3COOH+Ca(ClO)2==2HClO+Ca(CH3COO)2
C.I2+2NaClO3==2NaIO3+Cl2
D.4HCl+MnO2==MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
丁基橡胶可用于制造汽车内胎,合成丁基橡胶的一种单体A的分子式为C4H8,A氢化后得到2—甲基丙烷。完成下列填空:
1)A可以聚合,写出A的两种聚合方式(以反应方程式表示)。
2)A与某烷发生烷基化反应生成分子式为C8H18的物质B,B的一卤代物只有4种,且碳链不对称。写出B 的结构简式。
的结构简式。
3)写出将A通入下列两种溶液后出现的现象。
A通入溴水:
A通入溴的四氯化碳溶液:
4)烯烃和NBS作用,烯烃中与双键碳相邻碳原子上的一个氢原子被溴原子取代。分子式为C4H8的烃和NBS作用,得到的一溴代烯烃有 种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com