
【题目】将4molA气体和2molB气体置于1L的密闭容器中,混合后发生如下反应:2A(g)+B(g)=2C(g)。若经2s后测得C的浓度为1.2mol/L,下列说法正确的是()
A.用物质A表示的反应速率为1.2mol/(L·s)B.2s时物质A的转化率为30%
C.用物质B表示的反应速率为0.6mol/(L·s)D.2s时物质B的浓度为0.6mol/L
【答案】B
【解析】
A.若经2s后测得C的浓度为1.2molL1,则物质C的平均速率为![]() ,用A物质表示的反应速率υ(A)=υ(C)=0.6molL1·s1,故A错误;
,用A物质表示的反应速率υ(A)=υ(C)=0.6molL1·s1,故A错误;
B.根据A选项分析得到υ(A)=υ(C)=0.6molL1·s1,则![]() ,Δn(A)=1.2mol,2s时物质A的转化率
,Δn(A)=1.2mol,2s时物质A的转化率![]() ,故B正确;
,故B正确;
C.若经2s后测得C的浓度为1.2molL1,则物质C的平均速率为![]() ,用物质表示的反应速率υ(B)=
,用物质表示的反应速率υ(B)=![]() υ(C)=
υ(C)=![]() ×0.6molL1·s1=0.3molL1·s1,故C错误;
×0.6molL1·s1=0.3molL1·s1,故C错误;
D.根据B选项分析得到Δn(A)=1.2mol,Δn(B)=![]() Δn(A)=
Δn(A)=![]() ×1.2mol=0.6mol,则2s时物质B的物质的量为2mol0.6mol=1.4mol,物质的量浓度为
×1.2mol=0.6mol,则2s时物质B的物质的量为2mol0.6mol=1.4mol,物质的量浓度为![]() ,故D错误。
,故D错误。
答案为B。


科目:高中化学 来源: 题型:
【题目】元素X形成的气态X2的分子共有三种,其相对分子质量依次为158、160、162,此三种分子的物质的量之比为9:6:1,据此,下列说法中正确的是( )
A.X有三种同位素
B.其中一种同位素的质量数为80
C.X2的平均相对分子质量为159
D.质量数为79的同位素的原子百分数为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究CuSO4分解产物
Ⅰ.甲同学选择下列装置设计实验探究硫酸铜分解的气态产物SO3、SO2和O2,并验证SO2的还原性。

回答下列有关问题
(1)上述装置按气流从左至右排序为A、D、___________E、F(填代号)。
(2)装置D的作用是______________________;能证明有SO3生成的实验现象是______________________。
(3)在实验过程中C装置中红色溶液逐渐变为无色溶液,说明A中分解产物有___________;待C中有明显现象后,F开始收集气体,F装置中集气瓶收集到了少量气体,该气体是___________(填化学式)。
(4)为了验证SO2的还原性,取E装置中反应后的溶液于试管中,设计如下实验:
a.滴加少量的NH4SCN溶液 b.滴加少量的K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加盐酸酸化的BaCl2溶液
其中,方案合理的有___________(填代号),写出E装置中可能发生反应的离子方程式:________________。
Ⅱ.乙同学利用A中残留固体验证固体产物(假设硫酸铜已完全分解)查阅资料知,铜有+2、+1价,且分解产物中不含0价的铜。Cu2O在酸性条件下不稳定,发生反应:Cu2O+2H+=Cu+Cu2++H2O。
(5)为了验证固体产物中是否有Cu2O,设计了下列4种方案,其中能达到实验目的的是___________。
甲:取少量残留固体于试管,滴加足量的稀硝酸,观察溶液颜色是否变为蓝色
乙:取少量残留固体于试管,滴加足量的稀硫酸,观察溶液颜色是否变为蓝色
丙:取少量残留固体于试管,滴加足量的稀盐酸,观察是否有红色固体生成
丁:取少量残留固体于试管,通入氢气,加热,观察是否生成红色固体
(6)经检验CuSO4分解生成CuO、Cu2O、SO3、SO2和O2,且CuO、Cu2O的质量之比为5:9,SO2、O2、SO3的体积之比(同温同压下测定)为4:3:2。写出CuSO4分解的化学方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3),是一种易燃气体。主要作为甲基化试剂和各类气雾推进剂,在制药、染料、农药工业中有许多独特的用途。其制备方法之一可由H2和CO合成:2CO(g) + 4H2(g) ![]() CH3OCH3(g) + H2O(g) ΔH<0
CH3OCH3(g) + H2O(g) ΔH<0
(1)该反应的ΔS_____0(填“>”、“<”或“=”)。
(2)在恒温恒容容器中,不能判断该反应达到化学平衡状态的依据是____(选填字母序号)。
a.二甲醚和水蒸气的体积比等于1︰1 b.容器中压强保持不变
c.υ正(H2)=4υ逆(CH3OCH3) d.容器中一氧化碳的物质的量不再改变
(3)在密闭容器中,反应达到平衡后下列措施能加快反应速率并提高CO转化率的是___(选填字母序号)。
a.将H2O(g)从体系中分离出来 b.缩小容器体积,使体系压强增大
c.加入合适的催化剂 d.升高体系温度
(4)T℃时,在2 L密闭容器中,充入4 molCO和8 molH2发生反应,测得H2的物质的量随时间变化如图中状态Ⅰ(图中实线)所示:

①T℃时,在状态Ⅰ的条件下,反应达到C点时体系处于平衡状态,以H2表示该反应的平均速率υ(H2)=_________, CO的转化率是________,反应的平衡常数KⅠ=_________。
②若仅改变某一条件,测得H2物质的量随时间变化如图状态Ⅱ所示,则KⅠ _____KⅡ(填“>”、“<”或“=”)。
③若仅改变某一条件时,测得H2的物质的量随时间变化如图状态Ⅲ所示,则改变的条件可能是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g) + I2(g) ![]() 2HI(g) △H < 0,有相同容积的密封容器甲和乙,甲中加入H2和I2各0.1mol ,乙中加入0.1mol H2和0.2mol I2,相同温度下分别达到平衡。下列说法不正确的是( )
2HI(g) △H < 0,有相同容积的密封容器甲和乙,甲中加入H2和I2各0.1mol ,乙中加入0.1mol H2和0.2mol I2,相同温度下分别达到平衡。下列说法不正确的是( )
A. 乙中反应速率比甲中反应速率快
B. 平衡时甲、乙两容器中混合物的总物质的量之比为2:3
C. 若平衡时甲中H2的转化率为40%,则乙中H2的转化率大于40%
D. 平衡后,向乙中再加入0.1mol H2,建立新的平衡时,甲和乙中H2的百分含量不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见物质A~K之间存在如图所示的转化关系,其中A、D、E、H为单质,请回答下列问题。
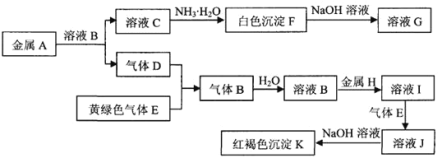
(1)下列物质的化学式是:C______,H______。
(2)反应“I→J”的离子方程式是____。
(3)检验J溶液中的金属离子的方法是(写出操作步骤、现象及结论)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。已知t ℃时AgCl的Ksp=4×10-10,下列说法正确的是( )
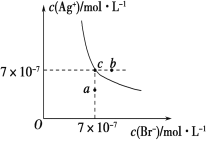
A. 加入NaBr固体,AgBr的溶解度减小,Ksp也减小
B. 在AgBr饱和溶液中加入固体NaBr,可使溶液中c点变到b点
C. 图中a点对应的是有AgBr沉淀生成
D. 在t ℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中有HCHO、H2和O2混合气体共10 g,放入足量Na2O2用电火花引燃,使其完全反应,Na2O2增重4 g,则原混合气体中O2的质量分数是
A.40% B.33.3% C.60% D.36%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研人员提出HCHO(甲醛)与O2在羟基磷灰石(HAP)表面催化生成H2O的历程,该历程示意图如下(图中只画出了 HAP的部分结构):
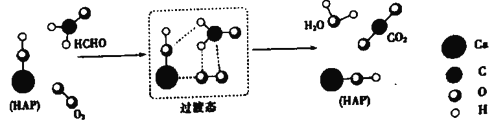
下列说法不正确的是
A. HAP能提高HCHO与O2的反应速率
B. HCHO在反应过程中,有C-H键发生断裂
C. 根据图示信息,CO2分子中的氧原子全部来自O2
D. 该反应可表示为:HCHO+O2![]() CO2+H2O
CO2+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com