
| 编号 | 纯净物 | 混合物 | 弱电解质 | 非电解质 |
| A | 明矾 | 蔗糖 | NaHCO3 | CO2 |
| B | 天然橡胶 | 石膏 | NH3?H2O | CH3CH2OH |
| C | 冰 | 王水 | H2SiO3 | Cl2 |
| D | 胆矾 | 水玻璃 | H2CO3 | SO2 |
| A、A | B、B | C、C | D、D |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| A | B | C | D | |
| X | 稀盐酸 | 偏铝酸钠溶液 | 氨水 | 二氧化碳 |
| Y | 碳酸钠溶液 | 硫酸溶液 | 硝酸银溶液 | 苯酚钠溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③④ | B、②④ | C、①③ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正反应进行的程度大,正反应速率一定大 |
| B、化学反应速率变化时,化学平衡一定发生移动 |
| C、化学平衡发生移动时,化学反应速率一定变化 |
| D、对于正反应为放热的化学反应,升高温度平衡逆向移动,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、油脂是产生能量最高的营养物质 |
| B、植物油通过氢化可以变为脂肪 |
| C、脂肪是有机体组织里储存能量的重要物质 |
| D、利用油脂在碱性条件下的水解,可以制甘油和肥皂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

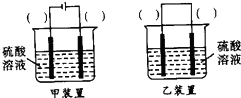
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
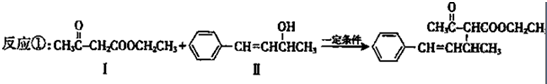
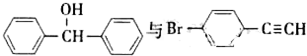 也可以发生类似反应①的反应,有机产物的结构简式为
也可以发生类似反应①的反应,有机产物的结构简式为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com