
| Cl2 |
| 红磷(少量) |



| NaOH/C2H5OH |
| △ |
| 一定条件 |
| 14n+32 |
| 8.8 |
| 22.4 |
| 2.24 |
 ,进而确定A为
,进而确定A为 ,C为
,C为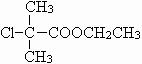 ,F为
,F为 ,由E的结构简式和D的苯环上有两种氢,可以确定D为
,由E的结构简式和D的苯环上有两种氢,可以确定D为 ,结合有机物的结构判断具有的性质.
,结合有机物的结构判断具有的性质.| 14n+32 |
| 8.8 |
| 22.4 |
| 2.24 |
 ,进而确定A为
,进而确定A为 ,C为
,C为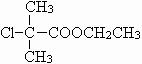 ,F为
,F为 ,由E的结构简式和D的苯环上有两种氢,可以确定D为
,由E的结构简式和D的苯环上有两种氢,可以确定D为 ,
, ,R为丙基,有两种,可为-CH2CH2CH3或-CH(CH3)CH3,所以同分异构体有
,R为丙基,有两种,可为-CH2CH2CH3或-CH(CH3)CH3,所以同分异构体有 两种,
两种, ;
; ,进而确定A为
,进而确定A为 ,故答案为:
,故答案为: ;
; 取代-Cl的反应,方程式为:
取代-Cl的反应,方程式为: ,
, ;取代反应;
;取代反应; ,其中含有的官能团有羟基和氯原子;是苯酚和Cl2反应的产物,与NaOH或Na2CO3溶液反应生成E.
,其中含有的官能团有羟基和氯原子;是苯酚和Cl2反应的产物,与NaOH或Na2CO3溶液反应生成E. (G),故答案为:消去反应;
(G),故答案为:消去反应; ;
; ,
, .
.


科目:高中化学 来源: 题型:
| A、-720kJ/mol |
| B、+430kJ/mol |
| C、-450kJ/mol |
| D、-1220kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
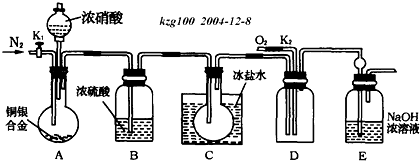
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 5.0 | 10.0 | 15.0 |
| 生成气体的体积/mL(标准状况) | 44.8 | 89.6 | 112 |
| 16n(H2O2) |
| m(样品) |
查看答案和解析>>
科目:高中化学 来源: 题型:
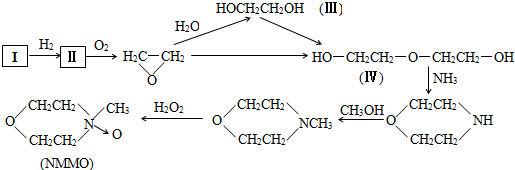
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g按如图所示装置进行实验(铁架台、铁夹等仪器未在图中画出).可供选用的试剂为:浓硫酸、品红溶液、酸性高锰酸钾溶液、碱石灰(可重复使用).
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g按如图所示装置进行实验(铁架台、铁夹等仪器未在图中画出).可供选用的试剂为:浓硫酸、品红溶液、酸性高锰酸钾溶液、碱石灰(可重复使用).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com