
【题目】(1)质量之比为16∶7∶6的三种气体SO2、CO、NO,分子个数之比为__;氧原子个数之比为___。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92g该氧化物的体积为448mL,则该氧化物的摩尔质量为___,R的相对原子质量为__。
(3)常温下,在27.5g水中溶解12.5gCuSO4·5H2O,恰好达到饱和,该溶液的密度为1.21g/cm3,则该溶液中CuSO4的物质的量浓度约为__,从中取出20.0mL该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积是__mL。
【答案】5:4:4 5:2:2 46g/mol 14 1.5mol/L 30
【解析】
(1)质量比为16:7:6的三种气体 SO2、CO、NO物质的量之比为![]() :
:![]() :
:![]() =5:4:4,故三者分子数目之比为5:4:4,含有氧原子数目之比为5×2:4×1:4×1=5:2:2;
=5:4:4,故三者分子数目之比为5:4:4,含有氧原子数目之比为5×2:4×1:4×1=5:2:2;
(2)RO2的物质的量的物质的量为![]() =0.02mol,其摩尔质量为
=0.02mol,其摩尔质量为![]() =46g/mol,R的相对原子质量为46-32=14;
=46g/mol,R的相对原子质量为46-32=14;
(3)12.5g CuSO45H2O的物质的量为![]() =0.05mol,则溶液中硫酸铜的物质的量为0.05mol,溶液的体积为
=0.05mol,则溶液中硫酸铜的物质的量为0.05mol,溶液的体积为![]() mL,故硫酸铜溶液的物质的量浓度为
mL,故硫酸铜溶液的物质的量浓度为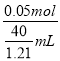 ×103=1.51mol/L,根据稀释定律,稀释前后溶质的物质的量不变,则20.0ml该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积为
×103=1.51mol/L,根据稀释定律,稀释前后溶质的物质的量不变,则20.0ml该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积为![]() =30mL。
=30mL。


科目:高中化学 来源: 题型:
【题目】关于有机物的叙述正确的是( )
A. 丙烷的二卤代物有4种,则其六卤代物是2种
B. 对二甲苯的一氯代物有3种
C. 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种
D. 某烃的同分异构体只能形成一种一氯代物,其分子式可能为C5H12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃酚是合成农药的重要中间体,其合成路线如下:

(1)A在空气中久置会由无色转变为棕褐色,其原因是____________,A在核磁共振氢谱中有___________组峰。
(2)B→C的反应类型是_____________________。
(3)已知X的分子式为C4H7Cl。写出A→B的化学方程式:___________________。
(4)要鉴别化合物C和D,适宜的试剂是__________________________。
(5)B的同分异构体很多,符合下列条件的有______种,写出其中能发生银镜反应的同分异构体的结构简式:__________(任写一种)。
①苯的衍生物 ②有两个互为对位的取代基 ③含有酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、配制960 mL 0.3mol/L NaOH溶液。具体如下:
(1)需__________________________g NaOH。
(2)配制过程中,下列仪器不会用到的是________________,(填序号)尚缺少的主要玻璃仪器是_________。
A.托盘天平 B.250mL容量瓶 C.玻璃棒 D.胶头滴管
II、乙同学用质量分数为98%,密度为1.84g/cm3的浓硫酸配制90mL 2.3 mol/L的稀硫酸。通过计算,用量筒量取_________ml 浓硫酸,选用的量筒________。(选填15mL,25mL, 50mL, 100mL)
III、下列操作会使配制的溶液浓度偏低的是___________(填字母)。
A、配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体
B、配制氢氧化钠溶液时,容量瓶中有少量水
C、发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线
D、定容时俯视容量瓶刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH<0,在低温下获得较高反应速率,反应过程如图:
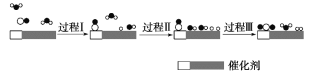
下列说法正确的是
A.若已知CO和H2的标准燃烧热,由此可推算出该反应的ΔH
B.过程Ⅰ、过程Ⅱ均为吸热过程,且吸收的热量相等
C.在该反应过程中,实际有两个H2O参与反应,断裂了三个氢氧键
D.使用催化剂降低了水煤气变换反应的ΔH,提高了反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)苏打属于________晶体,与盐酸反应时需要破坏的化学键有_________。
(2)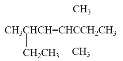 可与H2反应,请用系统命名法对其产物命名_________。
可与H2反应,请用系统命名法对其产物命名_________。
(3)在蔗糖与浓硫酸的黑面包实验中,蔗糖会变黑并膨胀,请用化学方程式解释膨胀的主要原因:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. C(s) + H2O(g)![]() CO(g) + H2(g)在室温下不能自发进行,说明该反应的△H>0
CO(g) + H2(g)在室温下不能自发进行,说明该反应的△H>0
B. 25 ℃,向0.1 mol·L-1的NH4Cl溶液中加水,![]() 会增大
会增大
C. 用pH均为2的盐酸和甲酸中和等物质的量的NaOH溶液,盐酸消耗的体积多
D. 合成氨生产中将氨气液化分离,可加快正反应速率,提高H2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)2CO(g)=2C(s)+O2(g),该反应不能自发进行的原因是_____________________
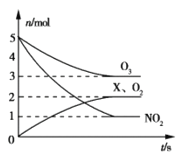
(2)臭氧是一种杀菌消毒剂,还是理想的烟气脱硝剂。一种脱硝反应中,各物质的物质的量随时间的变化如图所示,写出该反应的化学方程式__________________________。
(3)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图I、Ⅱ所示。
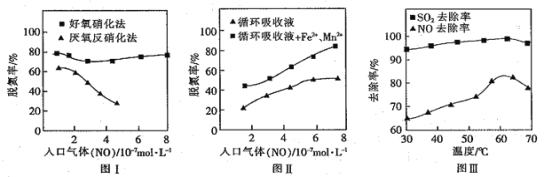
① 由图I知,当废气中的NO含量增加时,宜选用________法提高脱氮的效率。
② 图Ⅱ中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为________。
③研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为________。
(4)氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,涉及的相关反应如下:
反应①:NH3+HClO=NH2Cl+H2O
反应②:NH2Cl+HClO=NHCl2+H2O
反应③:2NHCl2+H2O=N2+HClO+3HCl
已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件一定的情况下,改变![]() (即NaClO溶液的投入量),溶液中次氯酸钠对氨氮去除率及余氯量 (溶液中+1价氯元素的含量) 的影响如图4所示。
(即NaClO溶液的投入量),溶液中次氯酸钠对氨氮去除率及余氯量 (溶液中+1价氯元素的含量) 的影响如图4所示。
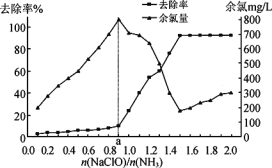
①反应中氨氮去除效果最佳的![]() 值约为_______。
值约为_______。
②a点之前氨氮去除率较低的原因为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学方程式C(s)+H2O(g) ![]() CO(g)+H2(g);△H =+131.3kJ/mol表示( )
CO(g)+H2(g);△H =+131.3kJ/mol表示( )
A. 碳和水反应吸收131.3kJ能量
B. 1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C. 1mol固态碳和1mol水蒸气完全反应生成一氧化碳气体和氢气,并吸热131.3kJ热量
D. 1个固态碳原子和1分子水蒸气反应吸热131.1kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com