
【题目】凯夫拉纤维是生产防弹衣的主要材料之一,其结构片段如下:

下列说法不正确的是
A. 其结构简式为:![]()
B. 凯夫拉纤维在发生水解反应的过程中,![]() 中的C—N键断裂
中的C—N键断裂
C. 完全水解产物的单个分子中,苯环上的氢原子具有相同的化学环境
D. 通过质谱法测定凯夫拉纤维的平均相对分子质量,可得其聚合度
【答案】A
【解析】
A. 该高聚物是通过氨基与羧基脱水缩合而成,其重复结构单元为 ;
;
B. 肽键![]() 可发生水解生成羧基和氨基;
可发生水解生成羧基和氨基;
C. 完全水解后生成的单体为:![]() 、
、![]() ;
;
D. 链节的相对分子质量![]() n = 总的平均相对分子质量。
n = 总的平均相对分子质量。
A. 根据高聚物的结构片段可知,其重复结构单元为: ,故该高聚物的结构简式可表示为:
,故该高聚物的结构简式可表示为: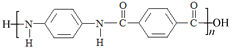 ,故A项错误;
,故A项错误;
B. 凯夫拉纤维在发生水解反应的过程中,![]() 中的C—N键断裂,生成羧基与氨基,故B项正确;
中的C—N键断裂,生成羧基与氨基,故B项正确;
C. 完全水解产物为![]() 、
、![]() ,从结构上可以看出,根据等效氢原理可知,苯环上的氢原子均具有相同的化学环境,故C项正确;
,从结构上可以看出,根据等效氢原理可知,苯环上的氢原子均具有相同的化学环境,故C项正确;
D. 通过质谱法可测定凯夫拉纤维的平均相对分子质量,除去链节( ),即可得出聚合度n的值,故D项正确;
),即可得出聚合度n的值,故D项正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列叙述正确的是

A.Mg(s)所具有的能量高于MgX2(s)所具有的能量
B.MgCl2电解制Mg(s)和Cl2(g)是吸热过程
C.热稳定性:MgI2>MgBr2>MgCl2>MgF2
D.常温下氧化性:F2<Cl2<Br2<I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从有机反应R-H+Cl2R-Cl(液)+HCl(气)制取副产品盐酸的设想已成为现实。高一兴趣小组设计了如图模拟装置图,请回答下列问题:

(1)写出实验室制Cl2 的离子方程式_________。
(2)装置B 中盛放的溶液是_________;作用是_________。
(3)装置C有三种功能:①_________②_________③观察气泡的产生情况,便于控制两种气体的配比。
(4)玻璃管E中放在石棉碎块上的碘化钾的作用是________;导管末端“肚形”装置的作用是________。
(5)从F 中分离出盐酸的最佳方法是________;该套实验装置还存在的缺陷是________。
(6)内江六中高一另一兴趣小组设计Cl2与NH3反应来验证非金属元素氯的氧化性强于和氮,请写出Cl2与足量NH3反应的化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以玉米(主要成分是淀粉)为原料制备乙醇的流程如下:

下列说法中不正确的是
A. C12H22O11属于二糖
B. 1mol葡萄糖分解成3mol乙醇
C. 可用碘水检验淀粉是否完全水解
D. 可采取蒸馏的方法初步分离乙醇和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式不正确的是
A. 次氯酸钙溶液中通入过量二氧化硫:Ca2+ + 2ClO-+ H2O + SO2=CaSO3↓+ 2HClO
B. 硫酸型酸雨放置一段时间溶液的pH下降:2H2SO3+O2=2H2SO4
C. 纯碱液可以清洗油污的原因:CO32+H2O![]() HCO3+OH
HCO3+OH
D. 向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72—+H2O![]() 2CrO42—+2H+
2CrO42—+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。

(1)图中试剂①~⑤溶质的化学式分别是:
①________,②________,③________,④__________,⑤__________。
(2)图中现象c表明检验出的离子是________________。
(3)白色沉淀A若加试剂③而不加试剂②,对实验的影响是____________________。
(4)气体E通入试剂④发生反应的离子方程式是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学对乙醛与新制的Cu(OH)2反应的实验进行探究。
实验Ⅰ:取2mL 10%的氢氧化钠溶液于试管中,加入5滴2%的CuSO4溶液和5滴5%的乙醛溶液,加热时蓝色悬浊液变黑,静置后未发现红色沉淀。
实验小组对影响实验Ⅰ成败的因素进行探究:
(1)探究乙醛溶液浓度对该反应的影响。
编号 | 实验Ⅱ | 实验Ⅲ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变红棕色,静置后底部有大量红色沉淀 | 加热,蓝色悬浊液变红棕色,静置后上层为棕黄色油状液体,底部有少量红色沉淀 |
已知:乙醛在碱性条件下发生缩合反应:CH3CHO+CH3CHO![]() CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
① 能证明乙醛被新制的Cu(OH)2 氧化的实验现象是______。
② 乙醛与新制的Cu(OH)2 发生反应的化学方程式是______。
③ 分析实验Ⅲ产生的红色沉淀少于实验Ⅱ的可能原因:______。
(2)探究NaOH溶液浓度对该反应的影响。
编号 | 实验Ⅳ | 实验Ⅴ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,蓝色悬浊液变红棕色, 静置后底部有红色沉淀 |
依据实验Ⅰ→Ⅴ,得出如下结论:
ⅰ. NaOH溶液浓度一定时,适当增大乙醛溶液浓度有利于生成Cu2O。
ⅱ. 乙醛溶液浓度一定时,______。
(3)探究NaOH溶液浓度与乙醛溶液浓度对该反应影响程度的差异。
编号 | 实验Ⅵ | 实验Ⅶ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,静置后底部有红色沉淀 |
由以上实验得出推论: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某物质X能发生如下转化,下列有关上述转化关系中物质及其反应的叙述不正确的是

A. 若X为N2或NH3,则A为硝酸
B. 若X为S或H2S,则A为硫酸
C. 若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D. 反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.密闭容器中,1molN2和3molH2催化反应后分子总数为2NA
B.100g98%的浓H2 SO4与过量的Cu反应后,电子转移数为NA
C.标准状况下,11.2L氧气和二氧化碳混合物中含氧原子数目为NA
D.1L1mol/LNa2CO3溶液中所含阴离子数目小于NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com