
| A、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| B、Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
| C、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
| D、0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4+AlO2-+2H2O |


 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
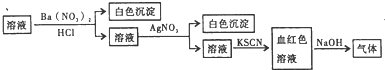
| A、原溶液中一定含有SO42- |
| B、原溶液中不一定含有NH4+ |
| C、原溶液中一定含有Cl- |
| D、原溶液中含Fe2+、Fe3+至少有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| B、向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| C、将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,生成的AgBr沉淀多于AgCl |
| D、测定中和反应的反应热时,将碱缓慢倒入酸中,所测反应热的数值偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Cl2,光照 |
| ① |
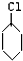
| NaOH、乙醇、△ |
| ② |
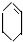
| 溴的CCl4溶液 |
| ③ |
| ④ |
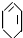
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、②③⑤ |
| C、③④⑤ | D、④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、硫酸与氢氧化钡反应的中和热化学反应方程式为:
| ||||||
| B、向0.1 mol?L-1、pH=1的NaHA溶液中加入NaOH溶液:H++OH-=H2O | ||||||
| C、以金属银为阳极电解饱和硫酸铜溶液:2Cu2++2H2O=2Cu+O2↑+4H+ | ||||||
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、由已知信息可得NA=
| ||
B、W g该原子的物质的量一定是
| ||
C、W g该原子中含有
| ||
| D、该元素的摩尔质量是aNA g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com