
����Ŀ�������ΪV L�ĺ����ܱ�������ʢ��һ����H2��ͨ��Br2(g)������ӦH2(g)+Br2(g)![]() 2HBr(g)����H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ��ͼ��ʾ������˵����ȷ����
2HBr(g)����H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ��ͼ��ʾ������˵����ȷ����

A����b��c�����ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2
B��a��b����ķ�Ӧ���ʣ�b��a
C��Ϊ�����Br2(g)��ת���ʿɲ�ȡ����Br2(g)ͨ�����ķ���
D��b��c�����HBr���������b��c
���𰸡�B
��������
���������A����ͼ��������T2�¶���ƽ��ʱ�������������С��˵��ƽ�������ƶ������¶�ƽ�������ƶ�����T2�¶���T1�ͣ����ȷ�Ӧ�¶�Խ�ͣ�ƽ�ⳣ��Խ������K1<K2����A����B����T1�¶��£����ż�����������ӣ���Ӧ���ʼӿ죬��B��ȷ��C�������壬�����������ת���ʣ���������ת���ʽ��ͣ���C������D��T2�¶���T1�ͣ������¶�ƽ�������ƶ�����HBr���������������b��c�����HBr���������c��b����D��������ѡB��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ���нϸ��۵㣬�����ͻ����
B. SO2��ʹ��ˮ��ɫ��������Ư����
C. �����ǵ���ʣ���Ϊ������ˮ��Һ�ܵ���
D. �ƼغϽ�����ڿ����ӷ�Ӧ�ѵ��Ƚ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ��ж����ڵ�һ���֣�����YԪ�ص�ԭ������ΪM��NԪ��ԭ������֮�͡�����˵����ȷ����
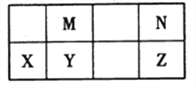
A. �⻯����ȶ��ԣ�N >Z������Ϊ���⻯����ӿ��γ����
B. Ԫ�صķǽ����ԣ�M > Y������Ϊ����M����YN2��Ӧ���ɵ���Y
C. �۷е㣺YN2>MN2������ΪYN2�ķ��Ӽ�������ǿ
D. �����ӵİ뾶��N >X������Ϊ���Ǿ�����ͬ�ĵ��Ӳ�ṹ��X�ĺ˵��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
���ܵĴ洢������Ӧ�õ���Ҫƿ������λ�⻯��������廯������Ŀǰ�����õ���Ҫ������ϡ�
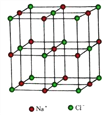
��1��Ti��BH4��2��һ�ֹ���Ԫ�����⻯�ﴢ����ϡ��ڻ�̬Ti�У��۵����Ų�ʽΪ____���۵����Ų�ͼΪ____
��2��Һ���Ǹ������ʣ������ܵ��������壬����N2+3H2![]() 2NH3,ʵ�ִ�������⡣����˵����ȷ����_____��
2NH3,ʵ�ִ�������⡣����˵����ȷ����_____��
a��NH3�����е�ԭ�ӵĹ���ӻ���ʽΪsp2�ӻ�
b��NH+4��PH+4��CH4��BH-4��ClO��4��Ϊ�ȵ�����
c����ͬѹǿʱ��NH3�ķе��PH3�ķе��
d��[Cu��NH3��4]2+�����У�Nԭ������λԭ��
��3���ü۲���ӶԻ��������ƶ�SnBr2�����У�Snԭ�ӵĹ���ӻ���ʽΪ__________��
SnBr2������ Sn-Br�ļ���______120��(�������������=��)��
(4) NiO �ľ���ṹ���Ȼ�����ͬ�� �ھ����������ӵ���λ����_______��
��֪�����ı߳�Ϊ a nm�� NiO ��Ħ������Ϊ b g��mol-1�� NAΪ�����ӵ�������ֵ�� ��NiO ������ܶ�Ϊ_________g��cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƿ������ڸ��Ƶر�ˮ�ʡ��������ؽ������ӷ�ˮ�������ೱ��Ҳ������Ӧ�������ȡ�ʵ���ҿ��ù�ҵ̼���(��MgCO3��FeCO3������)��ȡ������̼��ƣ�Ȼ�����ô���̼�����ȡ�������ƣ�����Ҫ�������£�

��֪��CaO2��8H2O�ʰ�ɫ����ˮ��
(1)д����Ӧ����������ԭ��Ӧ�����ӷ���ʽ�� ______________��
(2)��Ӧ�ٺ����Һ�м�Ũ��ˮ��Ŀ���ǣ� __________________��
(3)��Ӧ�ڳ��ñ�ˮ�����¶���0�����ң������ԭ����(д������)��
��__________________����______________��
(4)�ⶨ��Ʒ��CaO2�ĺ�����ʵ�鲽����
��һ����ȷ��ȡa g��Ʒ��������ƿ�У�������������ˮ������b g KI���壬�ٵ�������2 mol/L��H2SO4��Һ����ַ�Ӧ��
�ڶ�������������ƿ�м��뼸�ε�����Һ��
����������ε���Ũ��Ϊc mol��L��1��Na2S2O3����Һ����Ӧ�յ㣬����Na2S2O3��ҺV mL��
��֪��I2��2S2O![]() ===2I����S4O
===2I����S4O![]() ��
��
�ٵζ��յ������Ϊ____________����Ʒ��CaO2����������Ϊ_________________
��ijͬѧ��һ���͵ڶ����IJ������ܹ淶������������̫����������õ�CaO2��������������________ (�����Ӱ�족��ƫ�͡���ƫ�ߡ�)��ԭ����_____________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʳƷ�м���ɷֲ���Ӫ��ǿ�������� �� ��
A��ʳ�μӵ� B�������м��� C��ʳƷ�м��� D�������м���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�ִ�����Ⱦ״̬��������Դͷ���ֶ�������������β������ҵ�ŷš������ﳾ���������գ�������ɽ�緢�ȡ�
��1������β���е�NO��g����CO��g����һ���¶Ⱥʹ����������¿ɾ�����
����֪���ֻ�ѧ���ļ�������
����ʽ/�ṹʽ | NO/N��O | CO/C��O | CO2/O=C=O | N2/N��N |
��ѧ�� | N��O | C��O | C=O | N��N |
���ܣ�KJ/mol�� | 632 | 1072 | 750 | 946 |
���������β��������NO��g����CO��g��������Ӧ���Ȼ�ѧ����ʽ
2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ��H=_________kJ/mol
N2(g)+2CO2(g) ��H=_________kJ/mol
����������Ӧ�ں��¡����ݵ��ܱ���ϵ�н��У�����t1ʱ�̴ﵽƽ��״̬��������ʾ��ͼ�������������_________����ѡ����ţ�������ͼ��v����K��n��P���ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ�������ѹǿ��
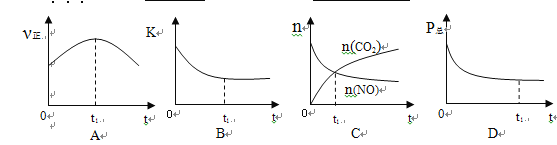 ��2����t1���£������Ϊ10L�ĺ����ܱ�������ͨ��NO��CO , ����˲�ͬʱ��ʱNO��CO�����ʵ������±���
��2����t1���£������Ϊ10L�ĺ����ܱ�������ͨ��NO��CO , ����˲�ͬʱ��ʱNO��CO�����ʵ������±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/��l0-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
n(CO)/��l0-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
t1��ʱ�÷�Ӧ��ƽ�ⳣ��K=__����������Ӧ��������ʹƽ�������ƶ��Ĵ�ʩ��_����д��һ�ּ��ɣ�
��3����ͼ1��ʾ����N2O4Ϊԭ�ϲ��õ�ⷨ���Ʊ�������ɫ��������һ�ֵ������д�����������������������缫��Ӧʽ________________________��
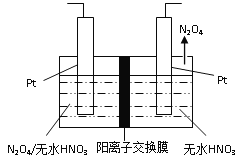
ͼ1 ͼ2
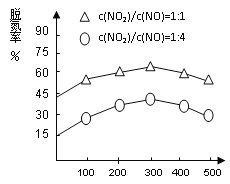
��4��NH3����ԭ��������(SCR)������ĿǰӦ����㷺���������������ѳ��������ڰ�������������£���ͬc(NO2)/c(NO)����ͬ�¶ȶ��ѵ��ʵ�Ӱ����ͼ2��ʾ����֪��������ԭ�������������ӦΪ���ȷ�Ӧ������ش��¶ȶ��ѵ��ʵ�Ӱ��____________________�����������Ľ��ͣ�____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H7N9����������һ�����������У��㽭��2015���������������ۼƱ����˸�ȾH7N9������4�����о��������ò����������У����2�������ϼ���ʧȥ���ԣ����ೣ������ҩ���磺������ء�Ư�ۡ������ȣ�Ҳ�����Խ��ò���ɱ��
��1��������ˮ�к��ж�����������ɫʯ����Һ������ˮ�У���Һ�Ժ�ɫ�����õ�����___________����һ�������Һ��ɫ����ȥ�������õ�����______________��
��д��������ˮ��Ӧ�����ӷ���ʽ_____________________��
��2����ҵ����ȡƯ�۵ķ�Ӧ����ʽΪ��__________________��
��3����֪���������Ũ�������ܲ�����������ѧ��Ӧ����ʽΪ��2KMnO4 + 16HCl ![]() 2MnCl2 + 2KCl + 8H2O + 5Cl2�����÷�Ӧ��������Ϊ____________��
2MnCl2 + 2KCl + 8H2O + 5Cl2�����÷�Ӧ��������Ϊ____________��
��4����Ư����Һ�еμ�̼������Һ���а�ɫ�������ɣ�д��������Ӧ�����ӷ���ʽ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL 0.50 mol/L ��������50 mL 0.55mol/L������������Һʹ��ʹ������װ�ý����к��Ȳⶨʵ����
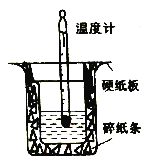
��1��װ����ȱ�ٵ�һ��������_____��װ���л����ڵĴ�����_______�����ִ�����������¶ȶ���_______������ƫ��������ƫС��������Ӱ����) ��
��2���ɷ�ȡ��55mL 0.50mol/L , NaOH ��Һ�ִ�50 mL 0.55m ѵL ������������Һ��____��������������������������
��3����ʵ��С����������ʵ�飬ÿ��ȡ��Һ��50mL������¼����ԭʼ������
ʵ����� | ���� ��ʼ�¶�t1/�� | ��ֹ�¶ȣ�t2���� | �²t2-t1���� | ||
���� | NaOH��Һ | ƽ��ֵ | |||
1 | 25.1 | 24.9 | 28.2 | ||
2 | 25.1 | 25.1 | 28.4 | ||
3 | 25.1 | 25.1 | 28.5 | ||
��֪���ᡢNaOH��Һ�ܶȽ���Ϊ1.0g/cm3���кͺ���Һ�ı����� C=4.2J/(g����)��ʽ��������÷�Ӧ���к���Ϊ��H=_____________________��������������С�����1λ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com