
【题目】乙炔是一种重要的基本有机原料,在一定条件下其衍变关系如下图:
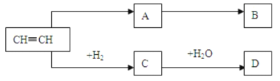
已知:B是一种塑料,75%的D溶液在医药上用作消毒剂。试回答下列问题:
(1)比乙炔多一个碳原子的同系物的结构简式是________________________。
(2).A物质的结构简式是________________________,A→B反应类型是______反应。
(3).写出以下各步反应的化学方程式:
乙炔→A:______________________________________________
乙炔→C:______________________________________________
C→D:_________________________________________________
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置制取氯气,并收集氯气进行实验。
请完成下列问题:
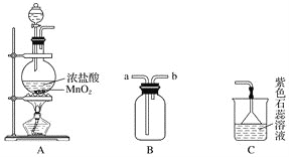
(1)装置A中发生反应的离子方程式为______________________________________。
(2)装置B如图中所示正放,则连接A的接口是________(填序号)。
(3)实验中可观察到装置C中紫色石蕊溶液的现象是__________________,其原因______________________________________________________________________。
(4)取出B中的集气瓶进行氯气与铜的反应实验,应该进行的操作是______________,然后立刻放入充满氯气的集气瓶中。实验中有同学提出应该在集气瓶底先放少量的水或细沙,你认为__________(填“需要”或“不需要”)放,理由是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氮及其化合物说法,不正确的是
A.“雷雨发庄稼”是由于放电条件有利于游离态的氮转化为化合态
B.二氧化氮不仅能形成酸雨,还能在一定条件下促进形成“光化学烟雾”
C.铵态氮肥应保存在阴凉处,硝态氮肥(硝酸盐)则能够耐高温
D.工业上制备硝酸过程中,氨催化氧化放出大量热,能预热新进入设备的氨气和空气,节约能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 == 2Na2CO3 + O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和过氧化钠为原料,制取O2,设计出如下实验装置:

(1)A中制取CO2 的装置,应从下列图①、② 中选哪个图:________。

A装置中发生反应的离子方程式为 ______________________________。
(2)B装置的作用是________________,C装置内可能出现的现象是__________ 。为了检验E中收集到的气体,在取出集气瓶后,__________________________(简要表述操作过程及结论)。
(3)若E中的石灰水出现轻微白色浑浊,请说明原因:_______________ (用离子方程式及简要文字描述)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气还原 NO 的反应为![]() 。
。
(1)![]() 的电子式为________。
的电子式为________。
(2)已知几种共价键的键能如下:
共价键 | H-H |
| N-O | H-O |
键能/( | 436 | 946 |
| 464 |
根据上述数据计算,NO的键能![]() =___________。
=___________。
(3)![]() 的反应速率表达式为
的反应速率表达式为![]() (
(![]() 为正反应速率常数,只与温度有关。
为正反应速率常数,只与温度有关。![]() 和
和![]() 为反应级数,取最简正整数)。
为反应级数,取最简正整数)。
为了探究一定温度下 NO、![]() 的浓度对反应速率的影响,测得实验数据如下:
的浓度对反应速率的影响,测得实验数据如下:
序号 |
|
|
|
Ⅰ | 0.10 | 0.10 | 0.414 |
Ⅱ | 0.10 | 0.20 | 0.828 |
Ⅲ | 0.30 | 0.10 | 3.726 |
①![]() 中,
中,![]() =____,
=____,![]() =______。
=______。
②经研究,有人提出上述反应分两步进行:![]() ;
;![]() 。
。
化学总反应由较慢的一步反应决定。
上述反应中,(a)反应较慢,(a)正反应活化能________(填“大于”“小于”或“等于”)(b)正反应活化能。
③1889年,瑞典化学家阿伦尼乌斯根据实验结果,提出了温度与反应速率常数关系的经验公式:![]() [
[![]() 为反应速率常数,
为反应速率常数,![]() 为比例常数,
为比例常数,![]() 为自然对数的底数,
为自然对数的底数,![]() 为气体摩尔常数,
为气体摩尔常数,![]() 为开尔文温度,
为开尔文温度,![]() 为活化能
为活化能![]() ]。
]。![]() 反应达到平衡后,升高温度,正反应速率常数增大的倍数_____(填“大于”“小于”或“等于”)逆反应速率常数增大的倍数。
反应达到平衡后,升高温度,正反应速率常数增大的倍数_____(填“大于”“小于”或“等于”)逆反应速率常数增大的倍数。
(4)一定温度下,在2 L恒容密闭容器中充入2 mol NO(g)、![]() 发生上述反应,混合气体压强随着时间变化关系如图所示。
发生上述反应,混合气体压强随着时间变化关系如图所示。
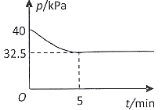
①05 min 内![]() 的平均速率
的平均速率 ![]() =___________________
=___________________![]() 。
。
②该温度下,上述反应的平衡常数![]() =________________
=________________![]() 。
。
③其他条件不变,在10min时向反应体系中再充入1mol NO、![]() ,达到新平衡时NO的平衡转化率 ________________(填“增大”“减小”或“不变”)。
,达到新平衡时NO的平衡转化率 ________________(填“增大”“减小”或“不变”)。
(5)工业上,可以采用电化学方法处理NO。以惰性材料为电极,以硝酸铵溶液为电解质溶液并补充![]() ,电解反应为
,电解反应为![]() 。电解过程中,阳极的电极反应式为_______________________。
。电解过程中,阳极的电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某微生物电池在运行时可同时实现净化有机物污水、净化含![]() 废水(pH约为6)和淡化食盐水,其装置示意图如图所示。图中,D和E为离子交换膜,Z为待淡化食盐水。(已知Cr3+完全沉淀所需的pH为5.6)下列说法不正确的是
废水(pH约为6)和淡化食盐水,其装置示意图如图所示。图中,D和E为离子交换膜,Z为待淡化食盐水。(已知Cr3+完全沉淀所需的pH为5.6)下列说法不正确的是
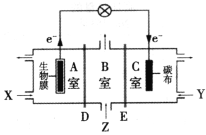
A.E为阴离子交换膜
B.X为有机物污水,Y为含![]() 废水
废水
C.理论上处理1 mol的![]() 的同时可脱除3 mol的NaC1
的同时可脱除3 mol的NaC1
D.C室的电极反应式为![]() +6e-+8H+==2Cr(OH)3↓+H2O
+6e-+8H+==2Cr(OH)3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从废定影液中回收Ag和Br2的主要步骤为:向废定影液中加入Na2S溶液沉淀银离子,过滤、洗涤、干燥,灼烧Ag2S制取金属Ag;制取Cl2并将Cl2通入滤液中氧化Br-,再用苯萃取分液。其中部分实验操作的装置如图所示。下列叙述正确的是
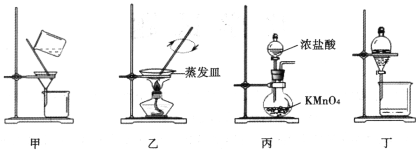
A.用装置甲分离Ag2S时,用玻璃棒不断搅拌
B.用装置乙在通风橱中高温灼烧Ag2S制取Ag
C.用装置丙制备Cl2,其中KMnO4也可用MnO2代替
D.用装置丁分液时,打开分液漏斗塞子,再打开旋塞,使下层液体从分液漏斗下端放出,待两液界面与旋塞上口相切即可关闭旋塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在体积为![]() 的密闭容器中,存在关系
的密闭容器中,存在关系![]() ,反应物和生成物的物质的量随时间变化的关系如图所示。下列说法正确的是( )
,反应物和生成物的物质的量随时间变化的关系如图所示。下列说法正确的是( )

A. ![]()
B. 该温度下,反应的平衡常数为![]()
C. 平衡时混合气体的平均摩尔质量是![]()
D. ![]() 时刻,保持温度不变,再充入
时刻,保持温度不变,再充入![]() ,重新达到平衡时,
,重新达到平衡时,![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3CuO+2NH3![]() 3Cu+N2+3H2O。下列判断正确的是
3Cu+N2+3H2O。下列判断正确的是
A.N元素的化合价降低B.NH3被还原
C.消耗0.3 mol CuO转移0.6 NA个电子D.CuO是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com