
【题目】实验室从废定影液中回收Ag和Br2的主要步骤为:向废定影液中加入Na2S溶液沉淀银离子,过滤、洗涤、干燥,灼烧Ag2S制取金属Ag;制取Cl2并将Cl2通入滤液中氧化Br-,再用苯萃取分液。其中部分实验操作的装置如图所示。下列叙述正确的是
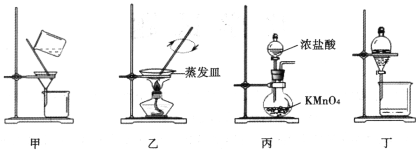
A.用装置甲分离Ag2S时,用玻璃棒不断搅拌
B.用装置乙在通风橱中高温灼烧Ag2S制取Ag
C.用装置丙制备Cl2,其中KMnO4也可用MnO2代替
D.用装置丁分液时,打开分液漏斗塞子,再打开旋塞,使下层液体从分液漏斗下端放出,待两液界面与旋塞上口相切即可关闭旋塞
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】现有短周期元素A、B、C、D。A元素M层上有2对成对电子,D与A在周期表中同一主族。由A、B与D组成的化合物的浓溶液是常见的干燥剂,常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要肥料。
(1)A的原子最外层共有___种不同运动状态的电子,该原子共有___种不同能量的电子,能量最高的电子占有___个轨道,其电子云形状为____。
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该化合物在实验室制备乙酸乙酯时所起的作用:_____。
(3)B与C元素形成带一个单位正电荷的离子,写出该微粒的电子式____。
(4)元素A与元素D相比,非金属性较强的是____(用元素符号表示),下列表述中能表明这一事实的是____。
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
从原子结构分析A和D非金属强弱的原因_____。
(5)C原子的原子结构示意图:_____,C的氢化物固态时属于____晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 K2FeO4 溶于水后,会水解生成多种微粒。下图是0.10 mol·L1 K2FeO4 溶液中各含铁微粒随溶液 pH 的变化图,纵坐标表示其个数百分含量,则下列说法不正确的是
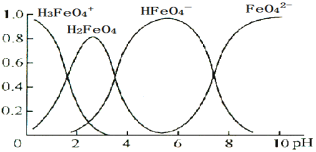
A.K2FeO4 溶于水呈碱性B.![]() 水解强于电离
水解强于电离
C.H2FeO4 既能和强碱反应又能和强酸反应D.0.10 mol·L1 的 K2FeO4 的 pH 近似等于 10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的基本有机原料,在一定条件下其衍变关系如下图:
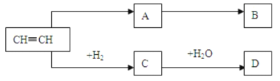
已知:B是一种塑料,75%的D溶液在医药上用作消毒剂。试回答下列问题:
(1)比乙炔多一个碳原子的同系物的结构简式是________________________。
(2).A物质的结构简式是________________________,A→B反应类型是______反应。
(3).写出以下各步反应的化学方程式:
乙炔→A:______________________________________________
乙炔→C:______________________________________________
C→D:_________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)有相同温度和压强下的两种气体12C18O和14N2,若两种气体的质量相同,则两种气体所含的质子数之比为__________,若两种气体的原子数相等,则两种气体所含中子数之比_________,若两种气体的体积相同,则两种气体的密度之比为_________。
(2)10.8 g R2O5中氧原子的数目为3.01×1023,则元素R的相对原子质量为 ________。
(3)将10 mL1.00 mol/L Na2CO3溶液与10 mL1.00 mol/L CaCl2溶液相混和,则混和溶液中Na+的物质的量浓度为___________(忽略混合前后溶液体积的变化)。
(4)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是_________。
(5)在空气中煅烧CoC2O4生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D的单质颜色相同的淡黄色固态化合物。试根据以上叙述回答:
(1)写出AB2的电子式:______________;
(2)用电子式表示C2B的形成过程:__________________________________。
(3)写出淡黄色固态化合物与水反应的化学方程式:_______________________________。
(4)请设计简单实验,比较元素B、D的金属性(或非金属性)强弱:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)以甲醇为原料制取高纯H2具有重要的应用价值。甲醇水蒸气重整制氢主要发生以下两个反应:
主反应:![]() H=+49kJmol-1
H=+49kJmol-1
副反应:![]() H=+41kJmol-1
H=+41kJmol-1
①甲醇蒸气在催化剂作用下裂解可得到H2和CO,则该反应的热化学方程式为_________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是______________。
②分析适当增大水醇比![]() 对甲醇水蒸气重整制氢的好处是__________。
对甲醇水蒸气重整制氢的好处是__________。
③某温度下,将n(H2O):n(CH3OH)=1:1的原料气充入恒容密闭容器中,初始压强为P1,反应达平衡时总压强为P2,则平衡时甲醇的转化率为________________(忽略副反应,用含P1、P2的式子表示)。
(2)工业上用CH4与水蒸气在一定条件下制取H2,原理为:![]() H=+203kJmol-1
H=+203kJmol-1
①该反应逆反应速率表达式为:v逆=k·c(CO)·c3(H2),k为速率常数,在某温度下测得实验数据如下表:
c(CO)/mol·L-1 | c(H2)/mol·L-1 | v逆/mol·L-1·min-1 |
0.05 | c1 | 4.8 |
c2 | c1 | 19.2 |
c2 | 0.15 | 8.1 |
由上述数据可得该温度下,该反应的逆反应速率常数k为_________L3·mol-3·min-1。
②在体积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度关系如图所示:N点v正____________M点v逆(填“大于”或“小于”);Q点对应温度下该反应的平衡常数K=_______________mol2·L-2。平衡后再向容器中加入1molCH4和1molCO,平衡向_____________方向移动(填“正反应”或“逆反应”)。
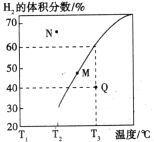
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 A、B、C、D、E、M、N六种短周期主族元素,它们的核电荷数依次增大。A可与D、E形成10电子分子,其中B的最外层电子数等于次外层电子数,C原子最外层电子数是次外层电子数的2倍,M的L层电子数为K层和M层电子数之和,D和M同主族。回答下列问题:
(1)元素B的符号和名称分别是____,______;在周期表中的位置是_________________。
(2)元素C的原子结构示意图为______________________________。
(3)元素C与M可形成CM2,C与N可形成CN4,这两种化合物均可做溶剂,其电子式分别为:________________和____________________。
(4)元素A与D、E形成10电子分子的结构式分别为:_______________和 _________________。
(5)元素D和M相比,非金属性较强的是_____________(用元素符号表示)。
(6)元素D、M的氢化物的沸点高低顺序为:______________________(用化学式表示)。
(7)在一定条件下,A、D的单质和M的最高价氧化物对应水化物的溶液可构成原电池,该电池在放电过程中,电解质溶液的酸性将_____________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的铁、氧化亚铁和氧化铁的混合粉末中,加入100ml2mol/L的盐酸,恰好使混合物完全溶解,并放出448ml的气体(SPT),在所得溶液中加入KSCN溶液无血红色出现.若用相同质量的上述混合物粉末高温下同足量的一氧化碳反应,可得到铁的质量是( )
A.无法计算B.2.8gC.5.6gD.11.2g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com