
【题目】向一定量的铁、氧化亚铁和氧化铁的混合粉末中,加入100ml2mol/L的盐酸,恰好使混合物完全溶解,并放出448ml的气体(SPT),在所得溶液中加入KSCN溶液无血红色出现.若用相同质量的上述混合物粉末高温下同足量的一氧化碳反应,可得到铁的质量是( )
A.无法计算B.2.8gC.5.6gD.11.2g
科目:高中化学 来源: 题型:
【题目】实验室从废定影液中回收Ag和Br2的主要步骤为:向废定影液中加入Na2S溶液沉淀银离子,过滤、洗涤、干燥,灼烧Ag2S制取金属Ag;制取Cl2并将Cl2通入滤液中氧化Br-,再用苯萃取分液。其中部分实验操作的装置如图所示。下列叙述正确的是
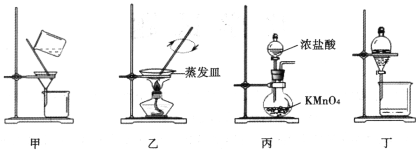
A.用装置甲分离Ag2S时,用玻璃棒不断搅拌
B.用装置乙在通风橱中高温灼烧Ag2S制取Ag
C.用装置丙制备Cl2,其中KMnO4也可用MnO2代替
D.用装置丁分液时,打开分液漏斗塞子,再打开旋塞,使下层液体从分液漏斗下端放出,待两液界面与旋塞上口相切即可关闭旋塞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO,其过程如下:mCeO2 (m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2
(m-x)CeO2·xCe+xO2;(m-x)CeO2·xCe+xH2O+xCO2![]() mCeO2+xH2+xCO
mCeO2+xH2+xCO

下列说法不正确的是( )
A.该过程中CeO2没有消耗B.该过程实现了太阳能向化学能的转化
C.图中ΔH1=ΔH2+ΔH3D.H2(g)+O2(g)=H2O(g)的反应热大于ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3CuO+2NH3![]() 3Cu+N2+3H2O。下列判断正确的是
3Cu+N2+3H2O。下列判断正确的是
A.N元素的化合价降低B.NH3被还原
C.消耗0.3 mol CuO转移0.6 NA个电子D.CuO是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是指导我们系统学习化学的重要工具。(答案都填写化学式)
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图__,自然界中存在的54Fe和56Fe,它们互称为___。将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是__。通常证明某溶液中含Fe2+的化学方法是___。
下表是元素周期表的一部分:
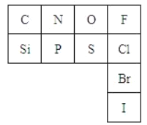
(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的__相同。处于同一列的N和P位于元素周期表的__族。
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为_,其气态氢化物的结构式为__。
②与硅元素处于同一周期,两性金属元素是__,并写出其在元素周期表中的位置:第__周期,__族,该元素的最高价氧化物对应水化物的电离方程式为__。
③第三周期半径最大的金属元素__,该元素形成氢氧化物的电子式_,检验物质中是否含有该元素的方法是:__。
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是__(写化学式)。该元素与硫元素相比,非金属性较强的元素是__(填元素符号),请写出证明该结论的一个实验事实:__。
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是___。
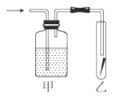
a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第__族,又有人提议可将它放在周期表中第IVA族,这样建议的原因是__。
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的__(选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上已经实现CO2与H2反应合成甲醇。在一恒温、恒容密闭容器中充入2molCO2和6molH2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。请回答:

(1)该密闭容器的容积是___。
(2)达到未平衡状态的时刻是___min(填“3”或“10”)。
(3)在前3min内,用H2浓度的变化表示的反应速率v(H2)=___mol/(L·min)。
(4)10min时体系的压强与开始时压强之比为__。
(5)达平衡后H2O(g)的物质的量分数是___。
(6)已知:①CO(g)+2H2(g)=CH3OH(g) △H=-90.1kJ/mol,②CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.1kJ/mol,则CO2与H2反应合成CH3OH(g)的热化学方程式__,反应在10min内所放出的热量为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明CO与N2O在Fe+作用下发生反应的能量变化及反应历程如图所示,两步反应分別为:①N2O+Fe+=N2+FeO (慢):②FeO++CO=CO2+Fe+ (快)。下列说法正确的是
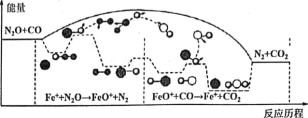
A. 反应①是氧化还原反应,反应②是非氧化还原反应
B. 两步反应均为放热反应,总反应的化学反应速率由反应②决定
C. Fe+使反应的活化能减小,FeO+是中间产物
D. 若转移lmol电子,则消耗II.2LN2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列两个图象:

下列反应中符合上述图象的是( )
A. N2(g)+3H2(g)![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
B. 2SO3(g)![]() 2SO2(g)+O2(g) ΔH>0
2SO2(g)+O2(g) ΔH>0
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
D. H2(g)+CO(g)![]() C(s)+H2O(g) ΔH>0
C(s)+H2O(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤、石油、天然气目前依然是我国的主要能源。它们在氧气不足时会不完全燃烧:2C+O2 ![]() 2CO,烃在氧气不足时也会不完全燃烧。
2CO,烃在氧气不足时也会不完全燃烧。
(1)完成下列方程式:2CxHy +___O2 ![]() aCO +___CO2 +___H2O
aCO +___CO2 +___H2O
(2)H 原子的电子排布式是“1s1”,它未表明电子运动状态的方面是________(填编号)。
a. 电子层 b. 电子亚层 c. 电子云的伸展方向 d. 电子的自旋
(3)上述反应中半径最大的原子核外有______种能量不同的电子,写出其最外层轨道表示式______。
(4)石油和煤的綜合利用中,下列说法错误的是______。
a.近年我国在新疆等地发现的石油矿藏超几十亿吨说明石油取之不尽
b.石油裂解目的是提高汽油的产量和质量
c.煤的液化和煤的气化都属于化学变化、石油的减压分馏属于物理変化
d.石油、煤、天然气都可以通过管道运输节约运输成本
(5)碳元素与氧元素的非金属性强弱的是 C______O(填“>”或“<”)。
(6)写出一个事实比较碳与硫非金属性强弱______。
(7)煤的气化是煤高效洁净利用的方向之一。在一定温度下的恒容密闭容器中建立下列化学平衡:C(s)+H2O(g)CO(g)+H2(g)—Q,该反应的平衡常数表达式______,可认定该可逆反应在一定条件下已达到化学平衡状态的 是______ 。(选填序号)
a. 体系的压强不再发生变化 b. 生成 n mol CO 的同吋生成 n mol H2
c. v 正(CO)=v 逆(H2) d. 1mol H-H 键断裂同吋断裂 1mol H-O 键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com