
【题目】一定温度下,在恒容密闭容器中充入一定量的N2O5,发生反应: 2N2O5(g)![]() 4NO2(g)+O2(g),能判断反应已经达到平衡状态的是
4NO2(g)+O2(g),能判断反应已经达到平衡状态的是
A. NO2和O2的浓度比保持不变B. 容器中的压强不再变化
C. 2υ正(NO2)=υ逆(N2O5)D. 气体的平均相对分子质量为43.2,且保持不变
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】对于反应4NH3+5O2![]() 4NO+6H2O,下列为4种不同情况下测得的反应速率,表明该反应进行最快的是( )
4NO+6H2O,下列为4种不同情况下测得的反应速率,表明该反应进行最快的是( )
A.v(NH3)=0.2mol/(L·s)B.v(O2)=10mol/(L·min)
C.v(H2O)=0.25mol/(L·s)D.v(NO)=8mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据Cd(Hg)+Hg2SO4=3Hg+Cd2++SO42-反应原理,设计出韦斯顿标准电池,其简易装置如图。下列有关该电池的说法正确的是
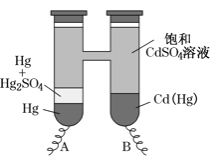
A.电池工作时Cd2+向电极B移动
B.反应中每生成amolHg转移2amol电子
C.电极B上发生的反应:Cd(Hg)-4e-=Hg2++ Cd2+
D.电极A上发生的反应:Hg2SO4+2e-=2Hg+ SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1 mol某烃在足量的氧气中完全燃烧,生成的CO2和水各0.6 mol。
(1)则该烃的分子式为 _________ 。若该烃不能使溴水或高锰酸钾溶液褪色,但在一定条件下,可以和溴蒸汽发生取代反应,其一溴取代物只有一种,则此烃属于_______ 烃,结构简式为 ____________,名称是____________。
(2)若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2,2—二甲基丁烷,则此烃属于______烃,结构简式为__________,名称是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学能与其他能量相互转化的说法错误的是( )
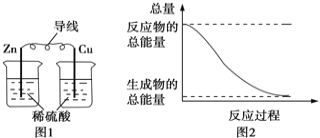
A.图1所示的装置能将化学能转变为电能
B.图2所示的反应为放热反应
C.中和反应中,生成物的总能量比反应物的总能量低
D.化学反应中能量变化的主要原因是化学键的断裂与形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )

编号 | X | Y | Z |
A | Zn | Cu | 稀硫酸 |
B | Ag | Zn | 硝酸银溶液 |
C | Cu | Ag | 硫酸铜溶液 |
D | Cu | Zn | 稀硫酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴(Co)与钛(Ti)是均可与强酸发生反应的金属。利用电解原理电解CoCl2溶液制取钴,工作原理如图所示,其中Ti-Ru为惰性电极。下列说法正确的是
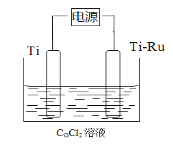
A. 电解时控制CoCl2溶液的pH在0~1范围内
B. 电解过程中Cl在Ti电极放电生成氯气
C. Ti-Ru的作用是作为损耗阳极材料和传递电流
D. 用CoSO4代替CoCl2会使钴的产率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体样品可能含有K+、Ca2+、NH4+、Cl-、CO32-、SO42-中的几种离子。将该固体样品分为等质量的两份,进行如下实验(不考虑盐类的水解及水的电离):(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况)(假设气体全部逸出)。下列说法正确的是
A.该固体中一定含有NH4+、CO32-、SO42-、Cl-
B.该固体中一定没有Ca2+、Cl-,可能含有K+
C.该固体可能由(NH4)2SO4、K2CO3和NH4Cl组成
D.该固体中n(K+)≥0.06mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室以含镍废料(主要成分为NiO,还含有少量 FeO、Fe2O3、CoO、BaO 和SiO2)为原料制备NixOy 和碳酸钴(CoCO3)的工艺流程如图:
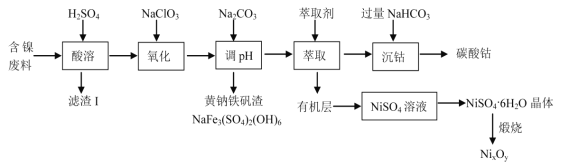
已知有关氢氧化物开始沉淀和沉淀完全的 pH 如表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Ni(OH)2 |
开始沉淀的 pH | 1.5 | 6.5 | 7.2 | 7.7 |
沉淀完全的 pH | 3.7 | 9.7 | 9.4 | 9.2 |
请回答以下问题:
(1)“滤渣Ⅰ”主要成分为(填化学式)_____。
(2)“氧化”时(加入 NaClO3)的离子方程式为_____。
(3)加入 Na2CO3 来“调 pH”的目的是生成黄钠铁钒沉淀而除去铁,也可通过加入MO(对应的金属氧化物)来调节 pH 将铁除去,则 pH 控制的范围为_____。
(4)在实验室萃取操作应该在_____中完成(填仪器名称),向水相中加入NaHCO3 时的离子方程式为_________。
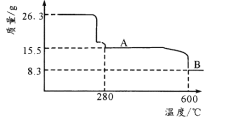
(5)从 NiSO4 溶液获得NiSO4·6H2O 晶体的操作依次是:_____,_________,过滤,洗涤,干燥。“煅烧”时剩余固体质量与温度变化曲线如图,该曲线中 B 段所表示氧化物的名称为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com