
【题目】下表中所列出的物质 , 属于 贴错了标签的是( )
选项 | A | B | C | D |
物质的化学式 | HNO3(浓) | 乙醇 | P4 | CCl4 |
危险警告标签 |
|
|
|
|
A. A B. B C. C D. D
【答案】D
【解析】
A、浓HNO3具有强烈的腐蚀性,应贴腐蚀品的标志,图为腐蚀品标志;
B、乙醇属于易燃物,应贴易燃液体的标志,图为易燃液体标志;
C、P4属于剧毒品,应贴剧毒品的标志,图为剧毒品标志;
D、CCl4常用作灭火材料,它不燃烧,不属于易爆物,图为爆炸品标志;
A、浓HNO3具有强烈的腐蚀性,应贴腐蚀品的标志,图为腐蚀品标志,符合题意,选项A正确;B、乙醇属于易燃物,应贴易燃液体的标志,图为易燃液体标志,符合题意,选项B正确;C、P4属于剧毒品,应贴剧毒品的标志,图为剧毒品标志,符合题意,选项C正确;D、CCl4常用作灭火材料,它不燃烧,不属于易爆物,图为爆炸品标志,不符合题意,选项D错误;答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
A. x的值为2 B. A的转化率为60%
C. B的平衡浓度为0.8 mol/L D. D的体积分数为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述正确的是( )
A. 甲苯与氢气完全加成后产物的一氯代物的种类数是5种
B. 苯与液溴混合后加入铁粉可发生加成反应
C. 1 mol 苹果酸(HOOCCHOHCH2COOH)可与3 mol NaHCO3发生反应
D. 氟利昂-12的结构式为![]() ,该分子是平面型分子
,该分子是平面型分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化铁胶体的制备与其性质检验实验如下,请回答下列问题。
(1)写出制备氢氧化铁胶体的化学方程式______________________。
(2)制备实验操作:取一小烧杯加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL____________,继续煮沸至________________,停止加热。
(3)证明有氢氧化铁胶体生成的实验操作是__________________________________。
(4)氢氧化铁胶体稳定存在的主要原因是____________________________。
(5)氢氧化铁胶体区别于氯化铁溶液最本质的特征是______________________。
(6)若取少量制得的胶体加入试管中,加入硫酸铵溶液,现象是______________,这种现象称为胶体的________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CrSi、Ge-GaAs、ZnGeAs2、聚吡咯、碳化硅和氧化亚铜都是重要的半导体化合物。回答下列问题:
(1)基态铬原子的核外电子排布式为___________,其中未成对电子数为____________。
(2) Ge-GaAs中元素Ge、Ga、As的第一电离能从大到小的顺序为_______________。ZnGeAs2中Zn、Ge、As的电负性从大到小的顺序为________________。
(3)聚吡咯的单体为吡咯(![]() ),该分子中氮原子的杂化轨道类型为__________;分子中σ键与π键的数目之比为________________。
),该分子中氮原子的杂化轨道类型为__________;分子中σ键与π键的数目之比为________________。
(4)碳化硅、晶体硅及金刚石的熔点如下表:
立方碳化硅 | 晶体硅 | 金刚石 | |
熔点/℃ | 2973 | 1410 | 3550~4000 |
分析熔点变化规律及其差异的原因:__________________________________________________。
(5)氧化亚铜的熔点为1235℃,其固态时的单晶胞如下图所示。
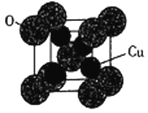
①氧化亚铜属于__________晶体。
②已知Cu2O的晶胞参数a=425.8pm,则其密度为__________ g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在 500 ℃时隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和SO2。
(1)为检验分解产物的成分,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。

①A中固体充分加热较长时间后,通入氮气,目的是__________________________。
②为验证A中残留物是否含有FeO,需要选用的试剂有____________(填字母)。
A.KSCN溶液 B.稀硫酸 C.浓盐酸 D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有________气体生成,若含有该气体,观察到的现象为_______________________________________。
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为b mol,C中沉淀物质的量为a mol,则b________________a(填“大于”“小于”或“等于”)。
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应的离子方程式为______________________
(2)为测定某固体样品中(NH4)2Fe(SO4)2·6H2O的含量,某实验小组做了如下实验:
步骤一:准确称量20.00 g硫酸亚铁铵晶体,配制成100 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,实验测定其与16.00mL 0.1000 mol/L KMnO4溶液恰好完全反应。已知(NH4)2Fe(SO4)2·6H2O的摩尔质量是392g/mol,则产品中(NH4)2Fe(SO4)2·6H2O的质量分数为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用CO与H2反应合成再生能源甲醇,反应如下:CO(g)+ 2H2(g)![]() CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
A. B点的速率比C点的大
B. A、B、C三点的平衡常数KA、KB、KC的大小关系为:KA=KB>KC
C. 若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为2L
D. 合成甲醇的反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是:
A. 将铜丝插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe===2Fe2+
C. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com