
【题目】轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列对该化合物的说法中,正确的是( )

A. 名称是乙醚
B. 只含有一种官能团
C. 链状同分异构体中,属于羧酸的有3种
D. 既能发生加聚反应,又能发生缩聚反应
科目:高中化学 来源: 题型:
【题目】向30 mL 1 mol·L-1的AlCl3溶液中逐渐加入浓度为4 mol·L-1的NaOH溶液,若产生0.78 g白色沉淀,则加入的NaOH溶液的体积可能为( )
A.3 mLB.7.5 mLC.15 mLD.17.5 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,对于①![]()
![]() 溶液②
溶液②![]() 的HCl溶液③
的HCl溶液③![]() 的NaOH溶液④
的NaOH溶液④![]()
![]() 溶液,下列说法正确的是
溶液,下列说法正确的是![]()
A.①和②分别稀释100倍后的pH:②<①
B.水电离出的![]() :④>③>②>①
:④>③>②>①
C.①和③混合后溶液呈中性: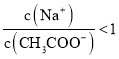
D.①和④混合后溶液呈酸性: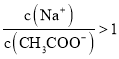
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以N2和H2为反应物,盐酸酸化的NH4Cl溶液为电解质的原电池,工作原理如图所示,下列说法不正确的是

A.b电极为负极
B.反应过程中,溶液中的H+向a电极移动
C.a电极的电极反应式为N2+6e-+8H+=2NH![]()
D.放电一段时间之后,溶液的酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。工业上合成尿素的反应如下:2NH3(g)+CO2(g) ![]() CO(NH2)2(l)+H2O(l) △H<0。回答下列问题:
CO(NH2)2(l)+H2O(l) △H<0。回答下列问题:
(1)已知工业上合成尿素分两步进行,相关反应如下:
反应Ⅰ:2NH3(g)+CO2(g) ![]() NH2COONH4(s) △H1<0
NH2COONH4(s) △H1<0
反应Ⅱ:NH2COONH4(s) ![]() CO(NH2)2(l)+H2O(l) △H2>0
CO(NH2)2(l)+H2O(l) △H2>0
①△H=________________(用△H1、△H2表示)
②下列示意图中[a表示2NH3(g)+CO2(g),b表示NH2COONH4(s),c表示CO(NH2)2(l)+H2O(l)],能正确表示尿素合成过程中能量变化曲线是(填编号)______。
(2)某实验小组模拟工业上合成尿素的条件,在恒定温度下,将氨气和二氧化碳按2:1的物质的量之比充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计),经20min达到平衡,各物质浓度的变化曲线如下图所示。

①可以判断该化合反应已经达到化学平衡的是_________。(填编号)
A.![]() B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中氨气的体积分数不变 D.密闭容器中混合气体的密度不变
②在上述条件下,从反应开始至20min时,二氧化碳的平均反应速率为____________。
③该反应的平衡常数表达式K=____________。
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如下图所示。

阳极室中发生的反应依次为_____________________、____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应。
实验编号 试剂 | A | B | C |
10% H2O2/mL | 20.0 | V1 | V2 |
2 mol·L-1 FeCl3/ mL | 0 | 5.0 | 10.0 |
H2O/ mL | V3 | V4 | 0 |
按要求回答下列问题:
(1)欲用图装置来比较该反应的反应速率快慢,检查该装置气密性的方法是_______。

(2)当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测____________________推(计)算反应速率。
(3)为实现实验目的,则V4=____。
(4)已知Fe3+催化H2O2分解的机理可分两步反应进行,其中第一步反应为:2Fe3+ + H2O2 =2Fe2+ + O2↑+ 2H+,则第二步反应的离子方程式为:___________________。
(5)读数时发现,量气装置左端液面低于右端液面,则测得的气体体积_____填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯(PS)和聚对苯二甲酸乙二醇酯(PET)材料具有高韧性、质轻、耐酸碱等性能,在生产生活中应用广泛。这两种聚合物可按下图路线合成,请回答下列问题:

(1)A的分子式为______,其核磁共振氢谱有______组(个)吸收峰。
(2)含有苯环的B的同分异构体有______种。
(3)D为苯乙烯,其结构简式为______,官能团为______。
(4)F的名称为______,由E→G的反应类型是______(填“缩聚”或“加聚”)反应。
(5)已知:
![]()
![]()
![]()
![]()
![]()
写出由BrCH2CH2Br制备HOOC-CH2CH2-COOH的合成路线:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是( )
A.1mol碳正离子(CH3+)所含的电子总数为9NA
B.25℃,pH=13的Ba(OH)2 溶液中含有OH-的数目为0.1NA
C.常温常压下,过氧化钠与水反应时,生成8g氧气转移的电子数为0.5NA
D.1mol雄黄(As4S4),结构如图:![]() ,含有2NA个S-S键
,含有2NA个S-S键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,请回答下列问题:
常温下,某Na2CO3溶液中滴入酚酞,溶液呈_____色,则该溶液呈 ______ 性,原因是 ______(用离子方程式表示),若在该溶液中再滴入过量的氯化钡溶液,所观察到的现象是_________,
(2)已知在H2S溶液中存在下列平衡:H2S![]() HS- + H+
HS- + H+
①向H2S溶液中加入NaOH固体时(不考虑温度变化),电离平衡向 ______ 移动(填“左”或“右”)![]() ______(填“增大”、“减小”或“不变”)。
______(填“增大”、“减小”或“不变”)。
②向H2S溶液中加入NaHS固体时,电离平衡向______ 移动(填“左”或“右”),pH ______(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com