
【题目】实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应。
实验编号 试剂 | A | B | C |
10% H2O2/mL | 20.0 | V1 | V2 |
2 mol·L-1 FeCl3/ mL | 0 | 5.0 | 10.0 |
H2O/ mL | V3 | V4 | 0 |
按要求回答下列问题:
(1)欲用图装置来比较该反应的反应速率快慢,检查该装置气密性的方法是_______。

(2)当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测____________________推(计)算反应速率。
(3)为实现实验目的,则V4=____。
(4)已知Fe3+催化H2O2分解的机理可分两步反应进行,其中第一步反应为:2Fe3+ + H2O2 =2Fe2+ + O2↑+ 2H+,则第二步反应的离子方程式为:___________________。
(5)读数时发现,量气装置左端液面低于右端液面,则测得的气体体积_____填“偏大”、“偏小”或“无影响”)
【答案】关闭分液漏斗活塞,向量气管中加水至两端产生液面差,记录刻度,静置一段时间后,刻度不变,证明气密性良好 相同时间内收集气体的体积或收集相同体积的气体所需的时间 5 2Fe2++H2O2+2H+=2Fe3++2H2O 偏小
【解析】
(1)检查装置气密性之前必须形成密闭系统,通过改变系统中的压强判断;
(2)由反应速率公式可知,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定相同时间内收集气体的体积或收集相同体积的气体所需的时间来计算化学反应速率;
(3)研究催化剂FeCl3的量对O2生成速率的影响实现实验目的,应使反应物的浓度相同及总体积相同;
(4)总反应减去第一步反应为第二步反应;
(5)由PV=nRT判断可得。
(1)检查装置气密性之前必须形成密闭系统,通过改变系统中的压强判断,则检查装置气密性的方法是关闭分液漏斗活塞,向量气管中加水形成密闭系统,若加水至两端产生液面差后,静置一段时间,液面差不变,证明装置气密性良好,故答案为:关闭分液漏斗活塞,向量气管中加水至两端产生液面差,记录刻度,静置一段时间后,刻度不变,证明气密性良好;
(2)由反应速率公式可知,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定相同时间内收集气体的体积或收集相同体积的气体所需的时间来计算化学反应速率,故答案为:相同时间内收集气体的体积或收集相同体积的气体所需的时间;
(3)研究催化剂FeCl3的量对O2生成速率的影响实现实验目的,应使反应物的浓度相同及总体积相同,则V1=V2=20.0mL,由C可知总体积为30.0mL,则V4=30.0-20.0-5.0=5.0mL,故答案为:5.0;
(4)总反应为2H2O2═2H2O+O2↑,第一步反应为2Fe3++H2O2═2Fe2++O2↑+2H+,则总反应减去第一步反应为第二步反应2Fe2++H2O2+2H+═2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O;
(5)读数时发现,量气装置左端液面低于右端液面,说明装置中压强高于外界大气压,由PV=nRT可知,测得的气体体积偏小,故答案为:偏小。


科目:高中化学 来源: 题型:
【题目】为研究某溶液中溶质R的分解速率的影响因素,分别用三份不同初始浓度的R溶液在不同温度下进行实验,c(R)随时间变化如图。下列说法不正确的是( )

A. 25 ℃时,在0~30 min内,R的分解平均速度为0.033 mol·L-1·min-1
B. 对比30 ℃和10 ℃曲线,在50 min时,R的分解百分率相等
C. 对比30 ℃和25 ℃曲线,在0~50 min内,能说明R的分解平均速度随温度升高而增大
D. 对比30 ℃和10 ℃曲线,在同一时刻,能说明R的分解速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
(1)实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。
序号 | 条件 | 现象 | 结论 | |
温度/℃ | 催化剂 | |||
1 | 40 | FeCl3溶液 | ||
2 | 20 | FeCl3溶液 | ||
3 | 20 | MnO2 | ||
4 | 20 | 无 | ||
试回答:
①实验1、2研究的是_______________对H2O2分解速率的影响。
②实验2、3的目的是_____________________________________________________。
(2)实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在酸性高锰酸钾溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____________________的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是___________。
A、硫酸钾B、硫酸锰C、水D、氯化锰
(3)实验三:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
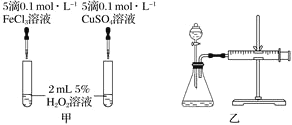
①定性如图甲可通过观察________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是______________________________。
②定量如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为:![]() ,一种工业合成氨,进而合成尿素的简易流程图如下:
,一种工业合成氨,进而合成尿素的简易流程图如下:

(1)步骤II中制氢气原理如下:
![]()
![]()
恒容容器中,对于以上反应,能加快反应速率的是______.
![]() 升高温度
升高温度![]() 充入He
充入He![]() 加入催化剂
加入催化剂![]() 降低压强
降低压强
(2)天然气中的![]() 杂质常用氨水吸收,产物为
杂质常用氨水吸收,产物为![]() ,一定条件下向
,一定条件下向![]() 溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为______.
溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为______.
(3)![]() 和
和![]() 在高温、高压、催化剂条件下可合成
在高温、高压、催化剂条件下可合成![]() ,反应的化学方程式______
,反应的化学方程式______![]() 以
以![]() 、空气、氢氧化钾溶液为原料,石墨为电极可构成然料电池,该电池中负极上的电极反应式是:______.
、空气、氢氧化钾溶液为原料,石墨为电极可构成然料电池,该电池中负极上的电极反应式是:______.
(4)已知![]()
![]() ,若合成尿素的流程中转化率为
,若合成尿素的流程中转化率为![]() 时,100吨甲烷为原料能够合成______吨尿素.
时,100吨甲烷为原料能够合成______吨尿素.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列对该化合物的说法中,正确的是( )

A. 名称是乙醚
B. 只含有一种官能团
C. 链状同分异构体中,属于羧酸的有3种
D. 既能发生加聚反应,又能发生缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.0 g铜与250 mL一定浓度的硝酸恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积为11.2 L。(假定反应前后溶液体积不变,也不考虑N2O4的存在。)
试计算:
(1)硝酸的物质的量浓度是____________ molL-1
(2)若要使此混合气体被水完全吸收,需要通入标准状况下__________L O2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于工业合成氨反应:N2+3H2![]() 2NH3,下列说法错误的是( )
2NH3,下列说法错误的是( )
A.使用合适的催化剂可以加大反应速率B.升高温度可以增大反应速率
C.增大N2浓度可以使H2完全反应D.增大N2浓度可以增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是国际上公认的安全、无毒的绿色消毒剂。常温下二氧化氯为黄绿色气体,其熔点为-59.5℃,沸点为11.0℃,极易溶于水,不与水反应。若温度过高,二氧化氯的水溶液可能会发生爆炸。某研究性学习小组拟用如下图所示装置制取并收集ClO2(加热和夹持装置均省略)。

(1)在圆底烧瓶中先放入一定量的KClO3和草酸H2C2O4),然后再加入足量的稀硫酸,在60~80℃之间反应生成ClO2、CO2和一种硫酸盐,该反应的化学方程式为________。
(2)装置A中使用温度计的目的是____。反应开始后,可以观察到圆底烧瓶内的现象是_____。
(3)装置B的作用是________。
(4)实验过程中装置D中的溶液里除生成Na2CO3外,还生成物质的量之比为1︰1的另外两种盐,一种为NaClO3,另一种为_______。
(5)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:量取ClO2溶液20mL,稀释成100mL试样,量取V1mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,振荡后,静置片刻;
步骤3:加入指示剂X,用 cmol·L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液V2mL。
已知:2ClO2+8H++10I-==5I2+2C1-+4H2O 2Na2S2O3+I2=Na2S4O6+2NaI
请回答:
①配制100mL步骤3中所需的Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要_______。(填仪器名称)
②步骤3中滴定终点的现象为_______。
③原ClO2溶液的浓度为_______g·L-1(用含字母的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.显酸性的溶液是酸溶液,显碱性的溶液是碱溶液
B.盐促进水的电离,酸碱抑制水的电离
C.常温下,某溶液中水电离出的H+浓度为1×10-9 mol/L,该溶液不一定是碱溶液
D.中性溶液即pH=7的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com