
【题目】煤气化的一种方法是在气化炉中给煤炭加氢,发生的主要反应为 C(s)+2H2(g) ![]() CH4(g)。在VL 的容器中投入 amol 碳(足量),同时通入 2amolH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压强及温度的变化关系如图所示。下列说法正确的是( )
CH4(g)。在VL 的容器中投入 amol 碳(足量),同时通入 2amolH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压强及温度的变化关系如图所示。下列说法正确的是( )

A.在 4MPa、1200K 时,图中 X 点 v 正(H2)<v 逆(H2)
B.在 5MPa、800K 时,该反应的平衡常数为![]()
C.上述正反应为吸热反应
D.工业上维持 6MPa、1000K 而不采用 10MPa、1000K,主要是因为前者碳的转化率高
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】工业上一般在恒容密闭容器中采用下列反应合成甲醇:
CO(g)+2H2(g)![]() CH3OH(g)+Q
CH3OH(g)+Q
32、能判断反应达到平衡状态的依据是(填字母序号,下同)________。
A.生成CH3OH的速率与消耗CO的速率相等 | B.混合气体的密度不变 |
C.混合气体的平均相对分子质量不变 | D.CH3OH、CO、H2的浓度都不再发生变化 |
33、下表所列数据是反应在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断该反应Q________(填“>”、“=”或“<”)0;
②某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2 mol/L,则CO的转化率为________,此时的温度为________。
34、要提高CO的转化率,可以采取的措施是________。
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压
e.加入惰性气体加压 f.分离出甲醇
35.寻找合适的催化剂来改善上述合成甲醇的条件一直是研究课题。现分别对X、Y、Z三种催化剂进行如下实验(其他条件均相同):
① X在T1℃时催化效率最高,能使正反应速率加快约3×105倍;
② Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍;
③ Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍;
已知:T1>T2>T3,根据上述信息,你认为在生产中应该选择的适宜催化剂并简述理由:___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用“钯催化交叉偶联反应”合成了有机物丙,合成路线如下:

列下分析判断正确的是( )
A.分离提纯有机物丙宜在NaOH热溶液中进行
B.利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素
C.可用酸性KMnO4溶液检验有机物丙中是否含有机物乙
D.PbCl2的作用是提高反应物的活性,加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象正确的是( )
A. 向 Ca(OH)2和 NaOH的混合溶液中通 入CO2
B. 向 FeCl3 溶液中加入锌粉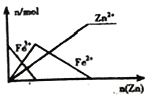
C. 向 NaOH 溶液中通入CO2
D. HCl与Cl2的混合气体通入NaOH溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的镁铝合金与一定量的浓硝酸恰好完全反应,得到溶液A和![]() 、
、![]() 、NO的混合气体,这些气体与
、NO的混合气体,这些气体与![]() 标准状况
标准状况![]() 混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得溶液A中加入
混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得溶液A中加入![]() 溶液至金属离子恰好完全沉淀,则消耗NaOH溶液的体积是
溶液至金属离子恰好完全沉淀,则消耗NaOH溶液的体积是 ![]()
![]()
A.![]() B.80mLC.
B.80mLC.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.酸碱中和滴定曲线是以酸碱滴定过程中滴加碱(或酸)的量或中和百分数为横坐标,以溶液 pH 为纵坐标,绘出溶液 pH 随碱(或酸)的滴加量而变化的曲线。它描述了滴定过程中溶液 pH 的变化情况,特别是滴定终点附近溶液 pH 的突变情况。下图为某浓度的 NaOH 溶液滴定 10.00mL 一定浓度的盐酸的图像

根据图像分析计算:
(1)HCl 溶液的浓度是___________,NaOH 溶液的浓度是____________。
(2)若向 20mL 稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是________(填字母)。
A.  B.
B. 
C.  D.
D. 
Ⅱ.下图为水在 T1℃和 T2℃时(T1<T2)对应的电离平衡曲线,回答下列问题:

(1)在T2℃时,若10体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是________________。
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液,若将二者等体积混合,混合溶液的pH>7,则BOH为_________碱,(填“强”或“弱”),判断的理由是_________。
(3)在曲线A所对应的温度下,向一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,所得混合液的pH=11,则两溶液的体积比V[Ba(OH)2]∶V(NaHSO4)=_________(假定混合液的总体积等于混合前两溶液体积之和)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为5L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g) ![]() Z(g),经20s达到平衡,生成0.1molZ。下列说法正确的是( )
Z(g),经20s达到平衡,生成0.1molZ。下列说法正确的是( )
A.0~20s内,X的反应速率为0.01mol·L-1·s-1
B.将容器体积变为10L,Y的平衡浓度大于原来的![]()
C.其他条件不变,若增大压强,则该反应的平衡常数增大
D.若该反应的△H>0,升高温度,X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是重要的氧化剂。回答下列问题:
(1)实验室常用高锰酸钾制备氧气。
①该反应的还原产物是___(写化学式),每生成1gO2转移___mol电子。
②高锰酸钾完全分解后,将固体生成物溶于水后过滤,向滤液中通入过量的二氧化碳。充分反应后过滤,得到二氧化锰,将滤液再经过重结晶分离,可得到高锰酸钾和碳酸氢钾。写出上述过程发生反应的化学方程式:___。
(2)实验室常用硫酸酸化的草酸(H2C2O4,二元弱酸)溶液滴定KMnO4溶液,测定KMnO4溶液浓度。步骤如下:
I.将-定量的高锰酸钾加入烧杯中,倒入蒸馏水使其溶解;
II.取ag草酸晶体(H2C2O4·2H2O,摩尔质量126g·mol-1)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗VmLKMnO4溶液。
①高锰酸钾溶液盛放在___(填“酸式”或“碱式”)滴定管中。
②滴定到达终点的现象是___。
③该KMnO4溶液的物质的量浓度为___mol·L-1(用相关字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④B.①④⑥C.②③⑤D.③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com