
【题目】KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作是:
(1)称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸1h;
(2)用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;
(3)过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处;
(4)利用氧化还原滴定方法,在70~80 ℃条件下用基准试剂(纯度高、式量较大、稳定性较好的物质)溶液标定其浓度。请回答下列问题:
(1)将溶液加热并保持微沸1 h的目的是_____。
(2)如何保证在70~80 ℃ 条件下进行滴定操作:_____。
(3)准确量取一定体积的KMnO4溶液用_____(填仪器名称)。
(4)在下列物质中,用于标定KMnO4溶液的基准试剂最好选用____(填序号)。
A.H2C2O4·2H2O B.FeSO4
C.浓盐酸 D.Na2SO3
(5)若准确称取Wg你选的基准试剂溶于水配成500 mL水溶液,取25.00 mL置于锥形瓶中,用高锰酸钾溶液滴定至终点,消耗高锰酸钾溶液VmL:
①滴定终点标志是___;
②所配制KMnO4标准溶液的物质的量浓度为__ mol·L-1;
(6)若用放置两周的KMnO4标准溶液去滴定水样中Fe2+含量,测得的浓度值将___(填“偏高”或“偏低”)。
【答案】(1)将水中还原性物质完全氧化;
(2)水浴加热,用温度计控制水温;
(3)酸式滴定管;(4)A;
(5)①滴入最后1滴KMmO4溶液,溶液颜色从无色变成浅红色,且半分钟内不褪色;②![]() ;(6)偏高.
;(6)偏高.
【解析】
(1)由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,所以要除去水中的还原性物质,则将溶液加热并保持微沸1h的目的是将水中还原性物质完全氧化;故答案为:将水中还原性物质完全氧化;
(2)加热温度低于100℃时,一般采用水浴加热,则要保证在70℃~80℃条件下进行滴定操作,应该水浴加热,用温度计控制水温;
(3)KMnO4溶液具有强氧化性能氧化碱式滴定管中的橡胶管,所以不能用碱式滴定管量取,应该用酸式滴定管量取;
(4)A.H2C2O42H2O常温下是稳定的结晶水水化物,溶于水后纯度高、稳定性好,可以用作基准试剂,故A正确;
B.FeSO4在空气中不稳定,亚铁离子容易被氧化成铁离子,不宜用作基准试剂,故B错误;
C.浓盐酸不稳定,易挥发,不宜用作基准试剂,故C错误;
D.Na2SO3具有还原性,在空气中容易被氧化成硫酸钠,不宜用作基准试剂,故D错误;
(5)①滴定时滴入最后一滴,高锰酸钾不完全反应,溶液变成浅红色并保持半分钟不褪色,说明滴定到达终点;
②草酸的物质的量浓度为: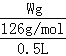 =
=![]() mol/L,根据反应方程式6H+ + 2MnO4﹣ + 5H2C2O42H2O ═ 2Mn2+ + 10CO2↑ + 18H2O中草酸和高锰酸钾之间的关系式得,酸性高锰酸钾的物质的量浓度=
mol/L,根据反应方程式6H+ + 2MnO4﹣ + 5H2C2O42H2O ═ 2Mn2+ + 10CO2↑ + 18H2O中草酸和高锰酸钾之间的关系式得,酸性高锰酸钾的物质的量浓度=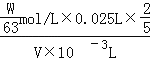 =
=![]() mol/L;
mol/L;
(6)在放置过程中,由于空气中还原性物质的作用,使KMnO4溶液的浓度变小了,再去滴定水样中的Fe2+时,需要消耗KMnO4溶液(标准溶液)的体积会增大,导致计算出来的c(Fe2+)值会增大,测定的结果偏高


科目:高中化学 来源: 题型:
【题目】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(37Rb)同周期。下列说法不正确的是
A. In是第五周期第ⅢA族元素
B. 11549In的中子数与电子数的差值为17
C. 原子半径:In>Al
D. 碱性:In(OH)3>RbOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲醇燃料电池的结构示意图。电池总反应为:2CH3OH+3O2→2CO2+4H2O。下列说法正确的是( )

A. 左电极为电池的负极,a处通入的物质是空气
B. 右电极为电池的负极,b处通入的物质是甲醇
C. 负极反应式为:CH3OH+H2O-6e-= CO2+6H+
D. 正极反应式为:O2+2H2O -4e-= 4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B | C | D |
|
|
|
|
升高温度,正反应方向是放热反应 | 0~3s内,反应速率为:v(NO2)=0.2 mol·L-1·s-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可降解聚合物P的合成路线如下

(1)A的含氧官能团名称是____________。
(2)羧酸a的电离方程是________________。
(3)B→C的化学方程式是_____________。
(4)化合物D苯环上的一氯代物有2种,D的结构简式是___________。
(5)E→F中反应①和②的反应类型分别是___________。
(6)F的结构简式是_____________。
(7)聚合物P的结构简式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中.△H能正确表示物质的燃烧热的是( )
A.CO(g) +![]() O2(g) ==CO2(g); △H=-283.0 kJ/mol
O2(g) ==CO2(g); △H=-283.0 kJ/mol
B.C(s) +![]() O2 ==CO(g); △H=-110.5 kJ/mol
O2 ==CO(g); △H=-110.5 kJ/mol
C.H2(g) +![]() O2(g)==H2O(g); △H=-241.8 kJ/mol
O2(g)==H2O(g); △H=-241.8 kJ/mol
D.2C8H18(l) +25O2(g)==16 CO2(g)+18 H2O(l); △H=-1136 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液导电能力越强,电导率越大。常温下用0.1000 mol/L盐酸分别滴定10.00 mL浓度均为0.1000 mol/L的NaOH溶液和二甲胺[(CH3)2NH]溶液{二甲胺在水中电离与氨相似,已知在常温下Kb[(CH3)2NH·H2O]=1.6×10-4},利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
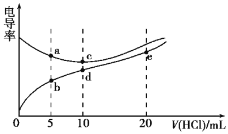
A.盐酸滴定二甲胺实验中选择酚酞作指示剂比选甲基橙误差更小
B.d点溶液中:c(H+)>c(OH-)+c[(CH3)2NH2+]
C.b、c、d、e四点的溶液中,水的电离程度最大的是d点
D.a点溶液与d点的溶液混合后的溶液中: c(OH-) < c(H+) < c[(CH3)2 NH2+] <c(Na+)< c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图其中能量最低的是___________(填字母),电子由状态B到状态C所得原子光谱为___________光谱(填“发射”或“吸收”),状态D是铝的某种激发态,但该电子排布图有错误,主要是不符合__________________________。
A. ![]()
B. ![]()
C. ![]()
D. ![]()
(2)K3[Fe(CN)6]溶液可用于检验Fe2+,生成沉淀的离子方程式为______________________________。与CN- 互为等电子体的化合物是______(写名称)。
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。与铜同一周期的副族元素的基态原子中,最外层电子数与铜原子相同的元素,其原子中未成对电子数为____。实验时形成的深蓝色溶液中的阳离子的结构简式为________。SO42-的立体构型为____,中心原子的杂化轨道类型为____。

(4)某种Al-Fe合金的晶胞如图所示,若合金的密度为ρg·cm-3,则晶胞中Al与Fe的最小距离为___ pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
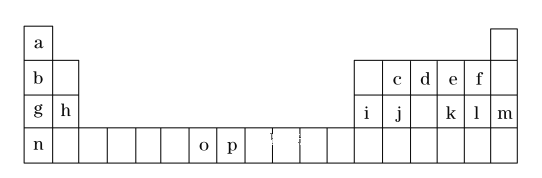
试回答下列问题:
①表中碱性最强的为_______(写出化学式);氢化物稳定性最强的为 ______ ;(写出化学式)
②基态o原子的价电子排布图为______;P3+离子与KSCN反应新生成的化学键为 _____ 键。
③将周期表中g、h、i、j四种元素的第一电离能由大到小排序为_________ (用元素符号表示)。
(二)SiO2晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si之间插入O原子而形成。
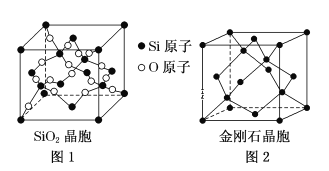
①推测SiO2晶胞中Si采用______杂化,O—Si—O的键角为___________。
②一个SiO2晶胞中,含有_______个Si原子。
③金刚石和晶体硅都是原子晶体,具有相似的结构,则熔点:金刚石_______Si晶体(填“大于”,“等于”或“小于”)
④假设金刚石晶胞的边长为a pm,NA为阿伏伽德罗常数,试计算该晶胞的密度______ g·cm-3(写出表达式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com