
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法正确的是( )
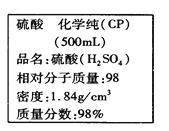
A. 该硫酸的物质的量浓度为9.2 mol·L-1
B. 该硫酸与等体积的水混合所得溶液的质量分数小于49%
C. 配制250mL 4.6 mol·L-1的稀硫酸需取该硫酸62.5mL
D. 该硫酸50.0mL与足量的铜反应可得到标准状况下SO2气体10.304 L
【答案】C
【解析】
A、利用c=![]() =
=![]() =18.4mol·L-1,故A错误;
=18.4mol·L-1,故A错误;
B、令硫酸的体积为VmL,稀释过程中溶质的质量不变,即m(H2SO4)=VmL×1.84g/cm3×98%,水的体积为VmL,则水的质量为Vg,溶液的质量为(VmL×1. 84g/cm3+Vg),稀释后所得溶液的质量分数为![]() ×100%=63.5%>49%,故B错误;
×100%=63.5%>49%,故B错误;
C、根据溶质的物质的量不变,得出250×10-3L×4.6mol·L-1=V(H2SO4)×10-3L×18.4mol·L-1,V(H2SO4)=62.5mL,故C正确;
D、铜是足量的,铜只与浓硫酸反应,不与稀硫酸反应,随着反应的进行,浓硫酸浓度逐渐变稀,反应将会停止,根据所给信息,无法计算出SO2的体积,故D错误;
答案为C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列实验中,所选装置或实验设计合理的是
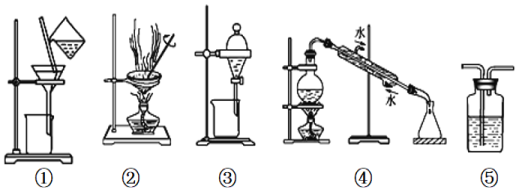
A. 用图①和②所示装置可以除去Na2CO3中的CaCO3杂质,并获得Na2CO3固体
B. 用乙醇提取溴水中的溴选择图③所示装置
C. 用图④所示装置可以分离乙醇水溶液
D. 图⑤所示装置中盛有饱和Na2CO3溶液除去CO2中含有的少量HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出砷的元素符号____________,原子中所有电子占有______个轨道,核外共有________个不同运动状态的电子。
(2)写出Ni的元素名称________,该元素在周期表的位置为第____周期,第____族。
(3)第四周期基态原子中未成对电子数最多的元素是_________,该元素基态原子的价电子轨道表示式为________________。
(4)第三电子层上有____个能级,作为内层最多可容纳___个电子,作为最外层时,最多可含有__个未成对电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组表述中,正确的是
A. 区分晶体和非晶体最可靠的科学方法是对固体进行 X射线衍射
B. 离子键、金属键无方向性和饱和性,而所有共价键都有方向性和饱和性
C. 处于能量最低状态时,外围电子排布为4d15s2的某元素原子,M能层共有8个电子,该元素位于![]() 区第ⅢB族
区第ⅢB族
D. 对充有氖气的霓虹灯管通电,灯管发出红色光.产生这一现象的主要原因是电子由基态向激发态跃迁时以光的形式释放能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A. 常温常压下, 30 g乙烷中所含的极性共价键数为6NA
B. 0.2mol N2和0.6mol H2混合充分反应后,转移的电子数目为1.2 NA
C. 0.1 mol9038Sr原子中含中子数为3.8NA
D. 1L1 mol·L-1 Ca(ClO)2溶液中含ClO-的数目等于2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应的ΔH等于反应物的总键能与生成物的总键能之差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),该反应的反应热ΔH为( )
Si(s)+4HCl(g),该反应的反应热ΔH为( )
A. +412 kJ·mol-1B. -412 kJ·mol-1C. +236 kJ·mol-1D. -236 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④12C、14C
(1)互为同位素的是______(填序号,下同);
(2)互为同素异形体的是_____;
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有___种;
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式____;
(2)用电子式表示二氧化碳分子的形成过程_________;
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是_______(填序号,下同);
(2)含有极性键的离子化合物是_________;
(3)氟化氢水溶液中存在的氢键有________种;
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
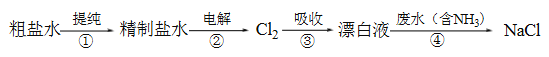
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里,用足量的浓盐酸与一定量的MnO2反应,来制取氯气。MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑ + 2H2O,若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
MnCl2 + Cl2↑ + 2H2O,若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
(1)理论上需要多少克MnO2参加反应?_____________
(2)参加反应的HCl的物质的量为多少?_____________
(3)被氧化的HCl的物质的量为多少?____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com