
【题目】化合物F是一种最新合成的溶瘤药物,可通过以下方法合成:
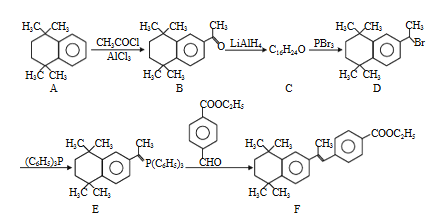
⑴D中所含官能团名称为________。
⑵A→B的反应类型是________。
⑶B的分子式为________。
⑷C的结构简式为________。
⑸A的核磁共振氢谱有_______种类型氢原子的吸收峰。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有机物Ⅰ是有机合成中间体,如可合成J或高聚物等,其合成J的线路图如图:
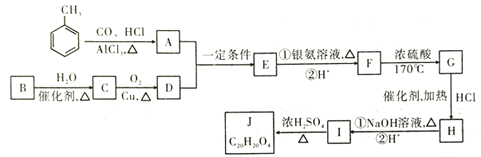
已知:①![]() ,A苯环上的一氯代物只有2种
,A苯环上的一氯代物只有2种
②有机物B是最简单的单烯烃,J为含有3个六元环的酯类
③![]()
![]() (
(![]() 、
、![]() 为烃基或H原子)
为烃基或H原子)
回答以下问题:
(1)A的化学名称为_____;E的化学式为_____。
(2)![]() 的反应类型:____;H分子中官能团的名称是____。
的反应类型:____;H分子中官能团的名称是____。
(3)J的结构简式为____。
(4)写出I在一定条件下生成高聚物的化学反应方程式____。
(5)有机物K是G的一种同系物,相对分子质量比G少14,则符合下列条件的K的同分异构体有___种(不考虑立体异构)。
a.苯环上只有两个取代基
b.既能发生银镜反应也能与![]() 溶液反应
溶液反应
写出其中核磁共振氢谱有6个峰,峰面积之比为2:2:1:1:1:1的结构简式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地菱锰矿的主要成分为MnCO3,还含有少量的FeCO3、CaCO3、Al2O3等杂质。工业上以菱锰矿为原料制备高纯度碳酸锰的流程如图所示:
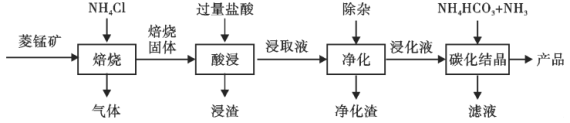
已知:MnCO3+2NH4Cl=MnCl2+CO2↑+2NH3↑+H2O.
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 |
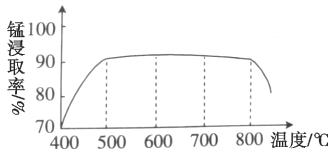
(1)焙烧时温度对锰浸取率的影响如图。焙烧时适宜的温度为___________左右;800℃以上锰的浸取率偏低,可能的原因是___________。
(2)净化包含三步:①加入少量MnO2,添加少量MnO2的作用是____________。发生反应的离子方程式为___________。
②加氨水调pH,溶液的pH范围应调节为___________~8.1之间。生成的沉淀主要是___________。
③加入MnF2,沉淀除去Ca2+,若溶液酸度过高,Ca2+沉淀不完全,原因是___________。
(3)碳化结晶中生成MnCO3的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.天宫二号空间实验室己于2016年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是___________(填化学式),该物质的类别属于_______(填“碱性氧化物”或“酸性氧化物”),实验室中不能用玻璃塞的试剂瓶盛放KOH溶液,原因是___________________(用离子方程式表示)。
(2)太阳能电池帆板是“天宫二号”空间运行的动力。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光太阳能电池,该电池的核心材料是_______,其能量转化方式为____________________。
II.铝和氢氧化钾都是重要的工业产品。
请回答:
(1)铝与氢氧化钾溶液反应的离子方程式是____________________。
(2)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有____________(填序号)。
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,________(填“能”或“不能”)说明固体混合物中无Fe2O3,若能,则不用填写理由,若不能,理由是(用离子方程式说明)___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某学生自己总结的一些规律,其中正确的是( )
A. 氧化物不可能是还原产物,只可能是氧化产物
B. 一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C. 饱和溶液一定比不饱和溶液的浓度大
D. 有些化学反应不属于化合、分解、置换、复分解等类型中的任何一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方案的设计或描述及对应的离子方程式正确的是
A. 用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ = Cu2+ + 2Fe2+
B. 将氯气溶于水制备次氯酸:Cl2 + H2O = 2H+ + Cl- + ClO-
C. 等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合Ca2+ + 2HCO3- +2OH-=CaCO3↓+CO32-+2H2O
D. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO![]() + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氢键,下列说法正确的是
A.分子中有N、O、F原子,分子间就存在氢键
B.因为氢键的缘故,![]() 熔沸点高
熔沸点高
C.NH3的稳定性很强,是因为其分子间能形成氢键
D.“可燃冰” 甲烷水合物(8CH4·46H2O)中CH4与H2O之间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】践行绿水青山就是金山银山的发展理念,就要做好大气污染和水污染防治。
(1)为落实“污水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
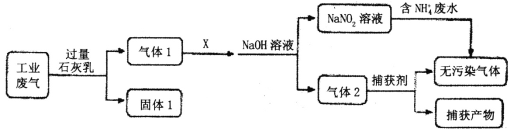
①气体l中主要含有___。
②已知X是空气,通入过量X是否合理__(填是或否),理由是__;NaNO2溶液综合处理含NH4+废水时,发生反应的离子方程式为___;捕获剂所捕获的气体成份主要是___。
(2)为了提高汽车尾气中NOx的去除率,有效降低柴油发动机在空气过量条件下的NOx排放,可以采用NSR(NOx储存还原)处理。其工作原理:NOx的储存和还原在不同时段交替进行,如图a所示。
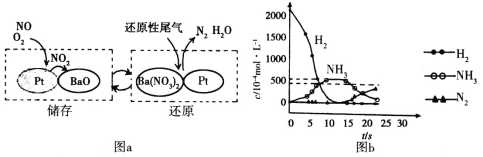
①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是__。
②用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为__。
③有人根据上述模拟过程认为,使用了催化反应器虽然能将NOx转化为N2,但从环保角度汽车仍然需要限行。请简述限行的理由:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是与生命活动密切相关的三种常见化合物,每种物质所含元素种类均不超过三种,甲是单质。它们之间有如下转化关系:
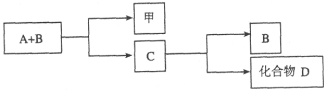
化合物D也是生活中常见的化合物,在一定条件下可发生如下反应:D+3甲![]() 3A+2B
3A+2B
请回答下列问题:
(1)在化合物A、B、C、D中所含元素完全相同的是__________和__________(填字母)。
(2)在常温下,A和B通过__________转化为C。该过程的能量转化关系如何?
____________________。
(3)写出由C生成D的反应的化学方程式____________________。
(4)化合物C是人类生命活动不可缺少的物质之一,它在血液中的正常含量是__________。
(5)目前化合物B在大气中含量呈上升趋势,对环境造成的影响是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com