
【题目】ClO2 与 Cl2 的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小 组通过图1 装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
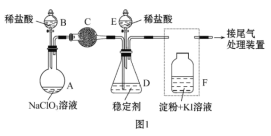
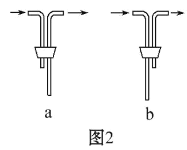
(1)仪器 D 的名称是___________。安装 F 中导管时,应选用图2中的___________。
(2)打开 B 的活塞,A 中发生反应:2NaClO3+4HCl![]() 2ClO2↑+Cl2↑+2NaCl+2H2O。为使 ClO2 在 D 中被稳定剂充 分吸收,滴加稀盐酸的速度宜___________ (填“快”或“慢”)。
2ClO2↑+Cl2↑+2NaCl+2H2O。为使 ClO2 在 D 中被稳定剂充 分吸收,滴加稀盐酸的速度宜___________ (填“快”或“慢”)。
(3)关闭 B 的活塞,ClO2 在 D 中被稳定剂完全吸收生成 NaClO2,此时 F 中溶液的颜色不变,则装置 C 的作用是___________ 。
(4)已知在酸性条件下 NaClO2 可发生反应生成 NaCl 并释放出 ClO2,该反应的离子方程式为___________,在 ClO2 释放实验中,打开 E 的活塞,D 中发生反应,则装置 F的作用是___________ 。
【答案】锥形瓶 b 慢 吸收 Cl2 4H++5ClO2-===Cl-+4ClO2↑+2H2O 验证是否有 ClO2 生成
【解析】
(1)根据仪器特征,仪器D的名称是锥形瓶;根据操作分析,F装置应是氯气和KI 反应,所以应长管进气,短管出气,选b。
(2)为使![]() 在D中被稳定剂充分吸收,滴加稀盐酸的速度要慢。
在D中被稳定剂充分吸收,滴加稀盐酸的速度要慢。
(3)F装置中![]() ,碘遇淀粉变蓝,所以F中溶液的颜色不变,则装置C的作用是吸收Cl2。
,碘遇淀粉变蓝,所以F中溶液的颜色不变,则装置C的作用是吸收Cl2。
(4)在酸性条件下![]() 可发生反应生成NaCl并释放出
可发生反应生成NaCl并释放出![]() ,该反应的离子方程式为4H++5ClO2-===Cl-+4ClO2↑+2H2O; 在
,该反应的离子方程式为4H++5ClO2-===Cl-+4ClO2↑+2H2O; 在![]() 释放实验中,打开E的活塞,D中发生反应,则装置F的作用是验证是否有
释放实验中,打开E的活塞,D中发生反应,则装置F的作用是验证是否有![]() 生成。
生成。


科目:高中化学 来源: 题型:
【题目】已知常温下,HCOOH(甲酸)比NH3H2O电离常数大。向10 mL 0.1mol/L HCOOH中滴加同浓度的氨水,有关叙述正确的是( )
A. 滴加过程中水的电离程度始终增大
B. 当加入10 mL NH3H2O时,c(NH4+) > c(HCOO-)
C. 当两者恰好中和时,溶液pH = 7
D. 滴加过程中n(HCOOH)与n(HCOO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 过量SO2通入到Ba(NO3)2溶液中:3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+
B. Fe(OH)2溶于稀HNO3:Fe(OH)2+2H+=Fe2++2H2O
C. H![]() O2中加入H2SO4酸化的KMnO4:5H
O2中加入H2SO4酸化的KMnO4:5H![]() O2+2MnO4-+6H+=518O2↑+2Mn2++8H2O
O2+2MnO4-+6H+=518O2↑+2Mn2++8H2O
D. 用铜电极电解硫酸铜溶液:2Cu2++2H2O![]() 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置制备溴苯,下列说法错误的是

A. 装置A中长玻璃导管仅起冷凝回流作用,装置B中的实验现象是CCl4由无色变橙色
B. 若装置B后连接装置C,装置C中生成淡黄色沉淀,可证明装置A中发生取代反应
C. 若装置B后连接装置D,则装置D的作用是吸收尾气
D. 向反应后的装置A中加入NaOH溶液,振荡静置,下层为无色油状液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种常用于橡胶硫化、有机物氯化的试剂,甲同学查阅资料:①将干燥的氯气在110~140 ℃ 间与硫反应,即可得S2Cl2粗品;②有关物质的部分性质如表所示:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 | ①一种橙黄色的液体,遇水易水解,有淡黄色固体出现,同时产生能使品红溶液褪色的气体。 ②300 ℃以上完全分解。③S2Cl2+Cl2=2SCl2 |
设计如图所示实验装置在实验室合成S2Cl2:
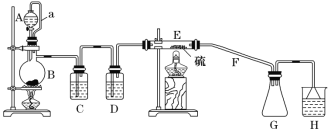
回答以下问题:
(1)仪器A的名称是_______________。
(2)B中所发生反应的离子方程式为___________________________________。
(3)C装置的作用是___________________________________ 。
(4)S2Cl2粗品中可能混有的杂质是_______________ (写其中一种,填化学式)。
(5)乙同学发现,该装置中除了E处的温度不能过高外,还有一处重大缺陷需改进,否则会导致S2Cl2的产率大大降低,原因是______________________________ (用化学方程式表示);请简要提出改进方案:________________________________________________。
(6)H中的溶液可以选择下列试剂中的__________ (填字母)。
A 碳酸钠溶液 B 氯化铁溶液 C 高锰酸钾溶液 D 亚硫酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物的种类很多,现有 H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、 Na2SO4 这 7 种常见的含硫化合物。回答下列问题:
(1)H2SO3 转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数 目:________。
(2)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验 证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于 CuSO4 溶液中,若铁 棒表面__________,则发生了钝化;若铁棒表面__________,则未发生反应。
(3)用 Na2SO3 吸收法作为治理 SO2 污染的一种方法,其原理为(用化学方程式表示):__________。
(4)减少 SO2 的污染并变废为宝,我国正在探索在一定条件下用 CO 还原 SO2 得到单质硫的方法来除去SO2。该反应的化学方程式:______________。
(5)制取硫酸铜有两种方法:方法一:2Cu+O2 ![]() 2CuO,CuO+ H2SO4= CuSO4+H2O,方法二:Cu+2H2SO4(浓)
2CuO,CuO+ H2SO4= CuSO4+H2O,方法二:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:_________________(答任一点)。
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:_________________(答任一点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将图1所示的装置中盐桥换成铜导线与两石墨棒连接得到图2所示装置,并将NaCl溶液换为HCl溶液,发现电流表指针仍然有偏转,下列说法正确的是( )

A. 图1盐桥中的阳离子移向甲装置
B. 两图都是将化学能转变成电能的装置
C. 图2中乙装置总反应的离子方程式:Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
D. 图2中电子流向为Fe→电流计![]() 石墨→石墨b→石墨c→Fe
石墨→石墨b→石墨c→Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。
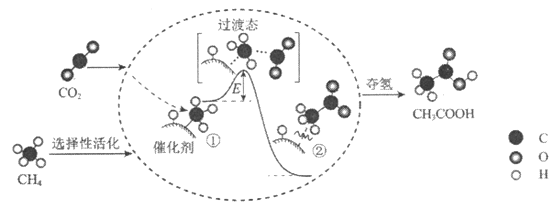
下列说法不正确的是
A. 该反应是化合反应
B. 催化剂参加了化学反应过程
C. CH4→CH3COOH过程中,有C—H键的断裂和形成
D. ①→②过程中,形成了C—C键,断裂的化学键的总键能<形成的化学键的总键能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联合国宣布2019年为“国际化学元素周期表年”。现有四种不同主族短周期元素X、Y、Z、W的原子序数依次递增,X与Y形成的化合物是光合作用的原料之一,Z、W处于同周期且族序数相差6。下列说法正确的是
A. 元素非金属性:![]()
B. Y和Z形成的化合物中只存在离子键
C. Z、W的简单离子半径:![]()
D. 只有W元素的单质可用于杀菌消毒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com