
【题目】下列说法不正确的是
A.镁的氧化物熔点很高,是优质的耐高温材料
B.工业上采用热还原法来冶炼金属铁
C.二氧化硫因具有还原性,可以用来漂白纸浆
D.晶体硅是一种重要的半导体材料,是手机芯片中的主要成分
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,某科研小组采用如下方案由铬铁矿(主要成分为FeO·Cr2O3,还含有SiO2、Al2O3 等杂质)制备重铬酸钾。
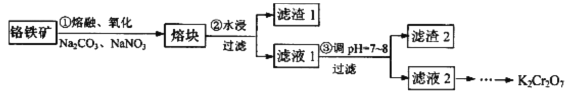
己知:①铬铁矿在熔融、氧化过程中发生的主要反应:
FeO·Cr2O3+Na2CO3+ NaNO3![]() Na2CrO4+ Fe2O3+ CO2↑+NaNO2
Na2CrO4+ Fe2O3+ CO2↑+NaNO2
Na2CO3+Al2O3![]() NaA1O2+CO2↑
NaA1O2+CO2↑
②2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
③有关物质的溶解度如图所示。

(1)步骤①中反应物NaNO3的作用是_______,熔融时所用的仪器为________(填字母)。
A瓷坩埚 B.铁坩埚 C.氧化铝坩埚
(2)步骤②所得的滤渣1中含量最多的金属元素是___________。
(3)步骤③可用醋酸调节滤液1的pH至7~8,可用__________(填仪器或用品名称)测定溶液的pH,写出步骤③加醋酸生成Al(OH)3 的离子方程式____________________________________。
(4)请设计从滤液2(主要溶质为Na2CrO4)制取K2Cr2O7固体的实验方案:__________(实验中须使用的试剂有: KC1固体、1mol/L硫酸溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中除含有Ca2+、Mg2+、SO![]() 等可溶性杂质外,还含有泥砂等不溶性杂质。
等可溶性杂质外,还含有泥砂等不溶性杂质。
(1)检验溶液中含有SO![]() 的方法是_________________________________________________。
的方法是_________________________________________________。
(2)将粗盐溶解过滤除去不溶性杂质后,在滤液中依次滴加过量NaOH溶液、BaCl2溶液和Na2CO3溶液,直至不再产生沉淀。其中加入Na2CO3溶液的目的是___________________,滴加Na2CO3溶液时发生反应的化学方程式为________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是__________,装置B中玻璃棒的作用是__________,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①的名称是__________,①中加入沸石的作用是______________,冷却水的方向是_________。装置D在分液时为使液体顺利滴下,应进行的具体操作是_________。
(3)从氯化钠溶液中得到氯化钠固体,选择装置__________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置__________。检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加________,不产生白色沉淀表明Cl-已除净。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是生物体内四种有机物的组成与功能关系图,请据图回答下列问题:

(1)物质F的元素组成是____________。
(2)生物体内C的种类有__________种,其种类不同是由____________决定。现有一抗体G,它由4条肽链构成,共有764个氨基酸,则该抗体分子中至少含有游离的氨基______个。
(3)小麦种子细胞中,物质E主要是指________。相同质量的E和F彻底氧化分解,耗氧量较多的是________(填字母)。
(4)组成SARS病毒的小分子D是__________,是由____________、______________和____________构成的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,分析细胞内4种重要有机物的组成及功能,E、G、H都是生物大分子,回答下列问题:

(1)A一般是指_______;E在动物细胞中是指_______,在植物细胞中主要是_______。
(2)F是指_______,它是由B(甘油和脂肪酸)组成的。除F之外,脂质还包括_______和_______。
(3)C是________________
(4)D是指_______,生物体内的H分为_______和_______两大类。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极)。下列分析正确的是)

A. 电子流动方向为a→导线→b
B. H+经质子交换膜由右向左移动
C. 放电一段时间b极附近pH不变
D. a电极发生反应:H2N(CH2)2NH2+16e-+4H2O==2CO2↑+N2↑+16H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有m克某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为________mol。
②该气体所含原子总数为________个。
③该气体在标准状况下的体积为________L。
(2)将质量比为14:15的N2和NO混合,则混合气体中N2和NO的物质的量之比为______,氮原子和氧原子的个数比为_______,该混合气体的平均摩尔质量为_________。
(3)同温同压下,质量相同的五种气体:① CO2 ② H2 ③ O2 ④ CH4 ⑤ SO2。
所占的体积由大到小的顺序是(填序号,下同)_________________;所含原子数由多到少的顺序是__________________________;密度由大到小的顺序是__________________。
(4)在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,该混合气体中,CO的质量是__g,CO2的体积是_____升。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com