
【题目】侯氏制碱法又称联合制碱法,是我国化学工程专家侯德榜于1943年发明的。此方法具有食盐利用率高、对环境的污染少、生产成本低等优点。其制备中涉及如下两个反应:NaC1+H2O+CO2+NH3===NaHCO3↓+NH4Cl、2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
(1)基态氯原子的电子排布式为______,C、N、O三种元素第一电离能由大到小的顺序为____。
(2)①H2O、CO2、NH3三种分子中属于V形分子的是_______。
②在常温常压下,1体积水可溶解700体积NH3、可溶解0.8体积CO2,试解释其原因:_________。
(3)Cu(NH3)2Cl2有两种同分异构体,其中一种可溶于水,则此种化合物是________(填“极性”或“非极性”)分子,由此推知[Cu(NH3)4]2+的空间构型是________。
(4)①要确定Na2CO3固体是晶体还是非晶体,最可靠的方法是_____。
②下列事实不能支持Na2CO3的晶体类型为离子晶体的是______(填字母)。
a.熔点为851℃ b.晶体中存在Na+、CO![]()
c.可溶于水 d.晶体中存在离子键,共价键
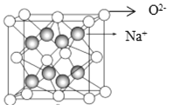
(5)钠、氧两元素可形成两种常见化合物,其中一种的晶胞如下图所示,则该氧化物的化学式为________,若晶胞参数为d pm,晶胞的密度为![]() ,则阿伏加德罗常数NA=______(用含d、ρ的代数式表示)。
,则阿伏加德罗常数NA=______(用含d、ρ的代数式表示)。
【答案】1s22s22p63s23p5或[Ne]3s23p5 N>O>C H2O CO2是非极性分子而水是极性分子,故CO2在水中溶解度较小,NH3是极性分子且能与水分子形成分子间氢键,故NH3在水中溶解度很大 极性 平面正方形 X-射线衍射法 c Na2O ![]()
【解析】
(1)氯原子核外有17个电子,根据能量最低原理,基态氯原子的电子排布式为1s22s22p63s23p5或[Ne]3s23p5;N原子2p轨道上的电子处于半充满状态,第一电离能大于O,元素的第一电离能由大到小的顺序为N>O>C;
(2)①H2O、CO2、NH3三种分子中,中心原子的价层电子对数分别为![]() 4个、
4个、![]() 2个、
2个、![]() 4个,其中水分子含有2对孤电子对,所以水分子是V形分子;
4个,其中水分子含有2对孤电子对,所以水分子是V形分子;
②CO2是非极性分子而水是极性分子,故CO2在水中溶解度较小,NH3是极性分子且能与水分子形成分子间氢键,故NH3在水中溶解度很大;
(3)Cu(NH3)2Cl2有两种同分异构体,其中一种可溶于水,根据相似相溶原理可知该物质应为极性分子;Cu(NH3)2Cl2有两种同分异构体,参考甲烷的二氯代物只有一种,可知[Cu(NH3)4]2+的空间构型应为平面正方形;
(4)①判断固体是晶体还是非晶体最可靠的方法是X-射线衍射法。
②离子晶体熔点较高,由离子构成,含有离子键;而许多分子晶体也可溶于水,故c项符合题意;
(5)由图及均摊原理知,晶胞中氧离子数是![]() ,钠离子的数目是8,故化学式为Na2O;一个晶胞中含有4个“Na2O”组成微粒,则晶胞的质量为
,钠离子的数目是8,故化学式为Na2O;一个晶胞中含有4个“Na2O”组成微粒,则晶胞的质量为![]() ,晶胞的体积为d3
,晶胞的体积为d3![]() 10-30 cm3,则晶胞的密度
10-30 cm3,则晶胞的密度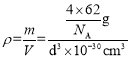 ,解得
,解得![]()


科目:高中化学 来源: 题型:
【题目】实验室利用下图所示装置测定水中氢氧元素之比。下列说法错误的是

A.①、③、④中依次盛装无水CaCl2、碱石灰、碱石灰
B.需测定实验前后装置②和装置③的质量差
C.结束反应时,应先移走酒精灯,待装置②的玻璃管冷至室温,再关闭活塞K
D.实验后装置②的玻璃管中CuO未全部变红,对实验结果无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰单质及其化合物应用十分广泛。回答下列问题:
(1)Mn在元素周期表中的位置为__,基态Mn原子的价电子排布式为__。
(2)MnCl2可与NH3反应生成[Mn(NH3)6]Cl2,新生成的化学键为__键。NH3分子的空间构型为__,其中N原子的杂化轨道类型为__。
(3)金属锰有多种晶型,其中δMn的结构为体心立方堆积,晶胞参数为αpm。δMn中锰的原子半径为__pm。已知阿伏加德罗常数的值为NA,δMn的理论密度ρ=__gcm3。(列出计算式)
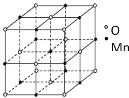
(4)已知锰的某种氧化物的晶胞如图所示,该氧化物的化学式为__,锰离子的配位数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型电池的工作原理如图所示。该电池工作时,下列说法错误的是
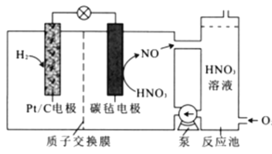
A.Pt/C电极为负极,质子通过交换膜从负极区移向正极区
B.理论上,当消耗22.4L(标准状况下)H2时,会消耗1molO2
C.反应池中发生总反应4NO+3O2+2H2O=4HNO3,实现HNO3再生
D.正极的电极反应为NO3-+4H++3e-=NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的有( )个
①可以用Cu(OH)2悬浊液用一种试剂鉴别甲酸、乙酸、乙醛、乙醇。
②可用酸性K2Cr2O7溶液检验是否酒后驾车,该应用利用了乙醇的还原性和低沸点的性质。
③向银氨溶液中加入几滴乙醛后用酒精灯加热至沸腾制可得银镜。
④向足量的浓苯酚溶液中滴入少量溴水,可观察到有白色沉淀生成,该沉淀为2,4,6-三溴苯酚。
⑤该分子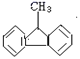 中的碳原子可能都在同一平面。
中的碳原子可能都在同一平面。
⑥做过银镜反应实验后的试管,用氨水洗涤。
A.5B.4C.3D.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
(配制KMnO4标准溶液)如图是配制50 mL KMnO4标准溶液的过程示意图。
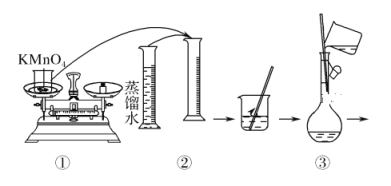
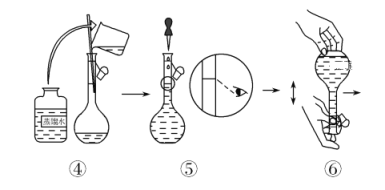
(1)请你观察图示判断,其中不正确的操作有(填序号)________。
(2)其中确定50 mL溶液体积的容器是(填名称)________。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将________(填“偏大”或“偏小”)。
(测定血液样品中Ca2+的浓度)抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)已知草酸跟KMnO4溶液反应的离子方程式为:
2MnO4-+5H2C2O4+6H+===2Mnx++10CO2↑+8H2O则方程式中的x=________。
(5)经过计算,血液样品中Ca2+的浓度为________mg/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒素是辣椒的活性成分,可在口腔中产生灼烧感,能够起到降血压和胆固醇的功效,进而在很大程度上预防心脏病,也能缓解肌肉关节疼痛。辣椒素酯类化合物的通式可以表示为![]() (R为烃基),其中一种辣椒素酯类化合物J的合成路线如图所示:
(R为烃基),其中一种辣椒素酯类化合物J的合成路线如图所示:
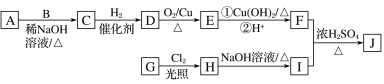
已知:①A、B、E互为同系物,其中A的分子式为C5H10O,B的相对分子质量为44,A和B的核磁共振氢谱显示都有两组峰。
②J的分子式为C15H22O4。
③R1CHO+R2CH2CHO![]()
![]() 。
。
回答下列问题:
(1)G中所含官能团的名称为__________。
(2)由A和B生成C的化学方程式为__________。
(3)由C生成D的反应类型为________,D的化学名称为_________。
(4)由H生成I的化学方程式为________。
(5)在G的同分异构体中,苯环上的一氯代物只有一种的共有_____种(不含立体异构),其中核磁共振氢谱显示两组峰的是_______(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、环境密切相关,下列说法错误的是
A.生活中钢铁制品生锈主要是由于发生吸氧腐蚀所致
B.石油的裂化、裂解和煤的干馏都属于化学变化
C.焚烧废旧塑料可有效防止“白色污染”
D.工业废水中的![]() 、
、![]() 等重金属阳离子可以通过加入
等重金属阳离子可以通过加入![]() 除去
除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了如图所示的装置研究金属的腐蚀和电化学防护。下列相关说法错误的是
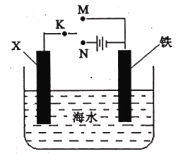
A.若X是碳棒,将开关K置于M处,铁棒的腐蚀加快
B.若X是铜棒,将开关K置于N处,铁棒难以被腐蚀
C.若X是碳棒,将开关K 置于N处,铁棒的腐蚀加快
D.若X是锌棒,将开关K置于M处,铁棒上发生的反应为:O2+ 2 H2O + 4e- = 4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com