
【题目】硫酸亚铁煅烧反应为2FeSO4(s)![]() X(g)+Fe2O3(s)+SO3(g),有关说法正确的是
X(g)+Fe2O3(s)+SO3(g),有关说法正确的是
A. 该反应中X为还原产物
B. X能使溴水退色,说明X具有漂白性
C. 该反应中每生成1 mol Fe2O3转移电子数约为6.02×1023
D. 该反应生成的气体通入足量Ba(NO3)2溶液中,可得到两种沉淀
科目:高中化学 来源: 题型:
【题目】用饱和硫酸亚铁、浓硫酸和硝酸钾反应可以制得纯度为98%的NO,其反应为FeSO4+KNO3+H2SO4(浓)![]() Fe2(SO4)3+NO↑+K2SO4+H2O(未配平)。下列有关说法不正确的是
Fe2(SO4)3+NO↑+K2SO4+H2O(未配平)。下列有关说法不正确的是
A. 该反应的氧化剂是KNO3
B. 氧化产物与还原产物的物质的量之比为2∶3
C. Fe2(SO4)3、K2SO4、H2O均为电解质
D. 该反应中生成144gH2O,转移电子的物质的量为12mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基本知识填空
(1)在一定条件下,当一个可逆反应的_____与____相等时,反应物的浓度与生成物的浓度不再改变,即达到化学平衡状态。
(2)化学平衡状态的特征:_____、____、_____、_____、_____。
(3)对于可逆化学反应mA+nBpC+qD在一定温度下达到化学平衡时,其平衡常数表达式为:______。
(4)强电解质包括的范围:____、____、____。弱电解质包括的范围:____、_____、____、_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的基本化工原料。结合以下合成路线,回答下列问题。
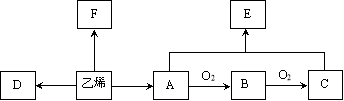
(1)乙烯的结构简式是______,A(乙醇)所含官能团的名称是__________。
(2)制备F(CH3-CH2Cl)有以下两种方案:
方案一 乙烷和氯气的取代反应 ;方案二 乙烯和氯化氢的加成反应
方案二优于方案一的原因是:_____________________________________ 。
(3)以乙烯为原料合成有机高分子化合物D(聚乙烯)的化学方程式为: 。
(4)以乙烯为原料可以合成一种有香味的物质E,实验室可通过下图所示装置来实现,请写出以下变化的化学方程式:
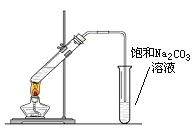
已知:B转化为C的化学方程式为:2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
① A→B的化学方程: 。
② A+C→E的化学方程式: 。
(5)装置中导管末端不能插入饱和碳酸钠溶液中,是为了 。
(6)试管中饱和碳酸钠溶液的作用为:
(7)饱和碳酸钠溶液的试管中可看到的实验现象为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在工业上可用含SiO2、CeO2和Fe2O3的废料作原料来获得硫酸铁铵晶体(Fe2(SO4)3·2(NH4)2 SO4·3H2O),同时可回收CeO2,工艺流程设计如下
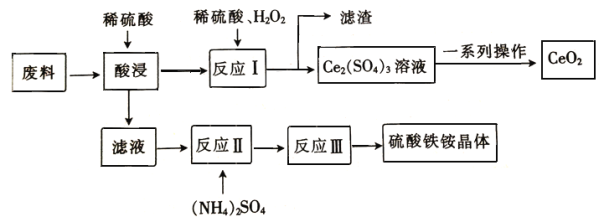
已知: ①SiO2、CeO2不溶于稀硫酸;②酸性条件下,CeO2可与H2O2反应;③“反应Ⅰ”所得溶液中含有Ce3+;④碱性条件下,NH4+与OH-结合生成NH3·H2O。
请回答下列问题
(1)“酸浸”时未发生的反应 物质是__________________(填化学式)。
(2)“滤液”中含有的阳离子有___________________(填离子符号)。
(3)写出“反应Ⅰ”的化学方程式:________________________________________。
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是__________________(填化学式)。
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置(夹持装置略)制取和收集纯净、干燥的氨气,并探究氨气的性质。
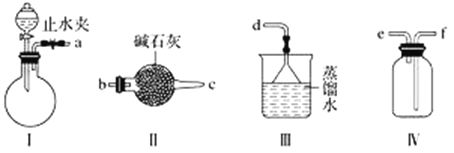
(1)关闭装置Ⅰ中的止水夹,向分液漏斗中加适量水,打开活塞,说明Ⅰ气密性良好的现象是______________________。
(2)利用装置Ⅰ制取氨气,不能选用的试剂为浓氨水和________(填字母)。
A.氢氧化钠 B.碱石灰 C.硝酸钾 D.生石灰
(3)根据实验要求,仪器连接的顺序(用字母编号表示):a接________、________接________、______接______。______
(4)收集氨气,按如图装置进行NH3性质的探究实验。
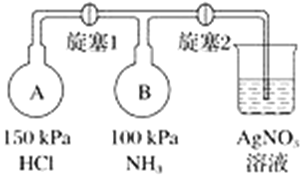
①打开旋塞1,B瓶中的现象是_________________________________________,原因是_____________________________________________,稳定后,关闭旋塞1;
②再打开旋塞2,B瓶中的现象是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为有机物,其中A是常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如下转化关系。请回答下列问题:
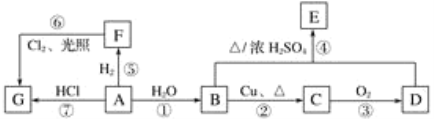
(1)写出A、D、G的结构简式:A________;D________;G________。
(2)A、B中官能团的名称:A________;B_________。
(3)在F的同系物中最简单的有机物的空间构型为____________。
(4)与F互为同系物且含有5个碳原子的同分异构体共有______种。
(5)写出下列编号对应反应的化学反应方程式,并注明反应类型:
①____________、________反应;
②___________________________________________、________反应;
④_________________________________________、________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10L密闭容器里发生4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的速率可表示为( )
4NO(g)+6H2O(g)反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的速率可表示为( )
A. v(O2)=0.0010mol·L-1·s-1B. v(NH3)=0.00125mol·L-1·s-1
C. v(H2O)=0.0010mol·L-1·s-1D. v(NO)=0.0010mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在下坡时,电池处于充电状态。
(1)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。镍氢电池充放电原理如图1所示,其总反应式为H2+2NiOOH![]() 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH___ (填“增大”、“减小”或“不变”),该电极的电极反应式为___。
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH___ (填“增大”、“减小”或“不变”),该电极的电极反应式为___。
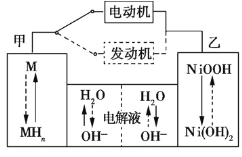
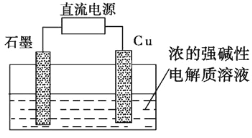
图1 图2
(2)Cu2O是一种半导体材料,可通过如图2所示的电解装置制取,电解总反应式为2Cu+H2O![]() Cu2O+H2↑,阴极的电极反应式是________。用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为___g。
Cu2O+H2↑,阴极的电极反应式是________。用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为___g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com