
【题目】某密闭容器中充入一定量SO2、O2发生反应2SO2(g)+O2(g)![]() 2SO3(g), 测得SO3浓度与反应温度关系如图.下列说法正确的是
2SO3(g), 测得SO3浓度与反应温度关系如图.下列说法正确的是
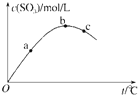
A. 该反应△H>0 B. SO2转化率:a>b>c
C. 化学反应速率:c>b>a D. 平衡常数K:b>c>a
科目:高中化学 来源: 题型:
【题目】在100℃时,把0.5molN2O4气体通入体积为5L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L-1。在60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法不正确的是
A.平衡时,体系内含NO2为0.04mol·L-1
B.平衡时,N2O4的转化率为60%
C.前2s,N2O4的平均反应速率为0.005mol·L-1·s-1
D.在2s时,体系内压强为反应前的1.1倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分难溶物的颜色和常温下的Ksp如下表所示:
Cu(OH)2 | CuOH | CuCl | Cu2O | |
颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
Ksp(25 ℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | — |
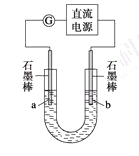
某研究性学习小组对电解食盐水进行了如下探究:
实验Ⅰ装置如图所示,接通电源后,发现a、b电极上均有气泡产生。
(1)电解过程中的总离子反应方程式为_________________________________________。
(2)为了确定电源的正、负极,下列操作一定行之有效的是_______。
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示。
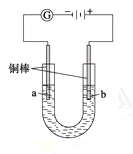
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5 min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10 min后,最靠近a极的白色沉淀开始变成红色;
④12 min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色。
(3) a极发生的电极反应方程式为________________________________________________________。
(4) 电解5 min后,b极发生的电极反应方程式为___________________________________________。
(5)12 min后,b极附近出现的橙黄色沉淀的成分是_____,原因是___________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(金刚石)=C(石墨)![]() <0,可知,金刚石比石墨稳定
<0,可知,金刚石比石墨稳定
C.在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ![]() = -571.6kJ/mol
= -571.6kJ/mol
D.在稀溶液中,若将含0.5mol H2SO4的浓溶液与含1mol NaOH的溶液混合,放出的热量大于57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金是建造航空母舰的主体材料.
(1)航母升降机可由铝合金制造.
①铝元素在周期表中的位置为 ______ ![]() 工业用铝土矿冶炼铝的化学方程式 ______ .
工业用铝土矿冶炼铝的化学方程式 ______ .
②![]() 合金焊接前用NaOH溶液处理
合金焊接前用NaOH溶液处理![]() 膜,其化学方程式为 ______ .
膜,其化学方程式为 ______ .
(2)![]() 也是重要的铝盐,其无水
也是重要的铝盐,其无水![]() 升华
升华![]() 遇潮湿空气即产生大量白雾,实验室可用下列装置制备.
遇潮湿空气即产生大量白雾,实验室可用下列装置制备.
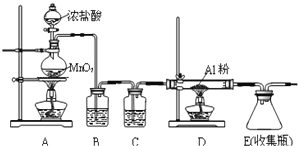
①装置在实验开始前应 ______ ,操作方法是: ______ .
②装置B中盛放饱和NaCl溶液,该装置的主要作用是 ______ ![]() 装置C中盛放 ______ .
装置C中盛放 ______ .
③装置A中发生的离子反应 ______ .
④该装置缺少尾气处理装置,尾气处理装置用的仪器是 ______ 装碱石灰.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是

A. 图甲表示反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
B. 图乙表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,乙的压强比甲的压强大
3C(g)+D(g)的影响,乙的压强比甲的压强大
C. 图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
D. 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某纯碱试样中含有NaCl杂质,有多种方法测定试样中纯碱的质量分数。
![]() 气体法
气体法
可用图中的装置进行实验:

主要实验步骤如下:
![]() 按图组装仪器,并检查装置的气密性;
按图组装仪器,并检查装置的气密性;
![]() 将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
![]() 从A处导管缓缓鼓入一定量的空气;
从A处导管缓缓鼓入一定量的空气;
![]() 称量盛有碱石灰的U型管的质量,得到b克;
称量盛有碱石灰的U型管的质量,得到b克;
![]() 从分液漏斗滴入
从分液漏斗滴入![]() 的盐酸,直到不再产生气体时为止;
的盐酸,直到不再产生气体时为止;
![]() 再从A处导管缓缓鼓入一定量的空气;
再从A处导管缓缓鼓入一定量的空气;
![]() 再次称量盛有碱石灰的U型管的质量,得到c克;
再次称量盛有碱石灰的U型管的质量,得到c克;
![]() 重复步骤
重复步骤![]() 和
和![]() 的操作,直到U型管的质量基本不变,为d克;
的操作,直到U型管的质量基本不变,为d克;
请填空和回答问题:
![]() 、D两装置中分别装什么试剂C: ______ D: ______
、D两装置中分别装什么试剂C: ______ D: ______
![]() 装置中干燥管F的作用是 ______
装置中干燥管F的作用是 ______
![]() 该试样中纯碱的质量分数的计算式为 ______
该试样中纯碱的质量分数的计算式为 ______
![]() 沉淀法
沉淀法
称取![]() 克样品完全溶于水后加足量的
克样品完全溶于水后加足量的![]() 溶液,然后过滤、洗涤、干燥称重得
溶液,然后过滤、洗涤、干燥称重得![]() 克固体,在该实验洗涤操作中如何检验固体已洗干净 ______ 。
克固体,在该实验洗涤操作中如何检验固体已洗干净 ______ 。
![]() 滴定法
滴定法
准确称取![]() 克样品,溶于水配成250mL溶液,量取25.00mL溶液于锥形瓶中,加入几滴酚酞作指示剂,用
克样品,溶于水配成250mL溶液,量取25.00mL溶液于锥形瓶中,加入几滴酚酞作指示剂,用![]() 的盐酸溶液进行滴定,到达终点时共消耗20.00mL盐酸,则样品中纯碱的质量分数为 ______ ,以下实验操作导致测量结果偏低的是 ______
的盐酸溶液进行滴定,到达终点时共消耗20.00mL盐酸,则样品中纯碱的质量分数为 ______ ,以下实验操作导致测量结果偏低的是 ______
A.配制样品溶液定容时俯视容量瓶刻度线
B.配制样品溶液定容后摇匀,发现液面低于容量瓶刻度线,于是又加水至刻度线
C.用盐酸滴定时滴定前仰视刻度线读数,滴定终点时俯视刻度线读数
D.滴定前锥形瓶中有水
E.酸式滴定管滴定前有气泡,而滴定后气泡消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸亚铁((C6H11O7)2Fe)是常用的补铁剂,易溶于水,几乎不溶于乙醇。用下图装置制备FeCO3,并利用FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:
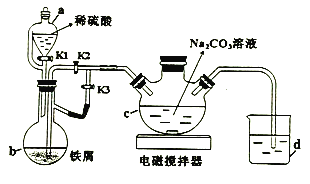
(1)a的名称为_________。
(2)打开a中K1、K3,关闭K2,一段时间后,关闭K3,打开K2。在_________(填仪器标号)中制得碳酸亚铁。实验过程中产生的H2作用有_________、____________。(写2条)
(3)将制得的碳酸亚铁浊液过滤、洗涤。如过滤时间过长会发现产品部分变为红褐色。用化学方程式说明原因____________。
(4)将葡萄糖酸与碳酸亚铁混合,加入乙醇、过滤、洗涤、干燥。加入乙醇的目的是_________________。
(5)用 NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时有气体产生,离子方程式为______________,此法产品纯度更高,原因是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com