
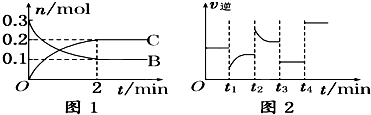
| A、反应开始2分钟内,v(B)=0.05mol/(L?min) |
| B、t1时改变的条件可能是减小了反应物的浓度 |
| C、t2时可能升高了温度 |
| D、t3时改变的条件可能是降压,此时c(B)减小 |
| ||
| △t |
| ||
| 2min |


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
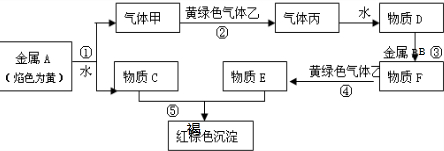
| A、全部 | B、⑤④⑥ |
| C、②④⑥ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝基苯是由苯与浓硝酸在浓硫酸作用下发生取代反应制取的 |
| B、苯可以发生取代反应也可以发生加成反应,但不可被氧化 |
| C、硝基苯有毒,密度比水小,可从水面上“捞出” |
| D、苯与硝基苯都属于芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同温度下,1 mol/L氨水溶液与0.5 mol/L氨水溶液中c(OH-) 之比为2:1 |
| B、NH4Cl 溶液中,c(NH4+)=c(Cl -) |
| C、向0.1 mol/L NaNO3溶液中滴加稀盐酸,使溶液pH=5,此时混合液中c(Na+)=c(NO3-) |
| D、向醋酸钠溶液中加入适量醋酸,使混合液的pH=7,此时混合液中c(Na+)=c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 3 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com