
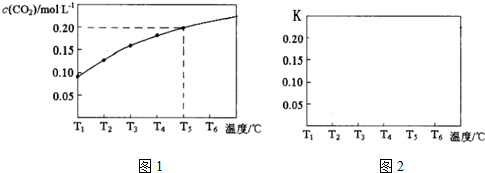
���� ��1����ͼ��֪���¶�Խ�ߣ�������̼�����ʵ���Ũ��Խ��˵���˷�ӦΪ���ȷ�Ӧ��T5��ʱ������̼�����ʵ���Ũ��Ϊ0.2mol/L���ݴ˼��㷴Ӧ���ʼ��ɣ�
��2��CaCO3��s��?CaO ��s��+CO2��g�����˷�Ӧ�ص�Ϊ���ȷ�Ӧ��K���¶ȵĺ������ݴ˽�ɣ�
��3������CaCO3��s��?CaO ��s��+CO2��g����дƽ�ⳣ��K�ı���ʽ�����岻��д��ƽ�ⳣ������ʽ��
��4���¶�Խ�ߣ�ƽ�ⳣ��Խ�ݴ˽�ɣ�
��� �⣺��1���¶�Խ�ߣ�������̼�����ʵ���Ũ��Խ�˷�ӦΪ���ȷ�Ӧ��T5��ʱ������̼�����ʵ���Ũ��Ϊ0.2mol/L��v��CO2��=$\frac{��c��C{O}_{2}��}{��t}$=0.005mol/��L•s�����ʴ�Ϊ������0.005mol/��L•s����
��2��CaCO3��s��?CaO ��s��+CO2��g�����˷�Ӧ�ص�Ϊ���ȵķ�Ӧ��Kֻ���¶��йأ������¶ȣ�ƽ�����ƣ�Kֵ����
�ʴ�Ϊ��d��
��3����֪CaCO3��s��?CaO ��s��+CO2��g������ƽ�ⳣ���ı���ʽK=c��CO2����
�ʴ�Ϊ��K=c��CO2����
��4���¶�Խ�ߣ�ƽ�ⳣ��Խ����ƽ�ⳣ����Ϊ������̼��Ũ�ȣ���ͼ������Ϊ��������ͼ�� ��
��
�ʴ�Ϊ�� ��
��
���� ������Ҫ������Ӱ��ƽ�ⳣ�������ء�Ӱ��ƽ���ƶ������ء���ѧƽ�ⳣ���ı���ʽ����Ŀ�ѶȲ�����ʱע��ѧ���ͼ�л�ȡ��Ϣ����ע���ƽ�ⳣ����������⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���ӻ���� | Ҫ �� |
| A | K+��SO42-��Cl-��HS- | c��K+����c��SO42-�� |
| B | Fe3+��Na+��NO3-��ClO- | ��ҺpH=1 |
| C | Na+��Al3+��Cl-��SO42- | �μӰ�ˮ�����г������� |
| D | NH4+��Ba2+��NO3-��CH3COOH | �μ�NaOH��Һ���������ݲ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ���� | �¶�/�� | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | |
| n��X�� | n��Y�� | n��M�� | ||
| �� | 700 | 0.40 | 0.10 | 0.090 |
| �� | 800 | 0.10 | 0.40 | 0.080 |
| �� | 800 | 0.20 | 0.20 | a |
| �� | 800 | 0.10 | 0.10 | b |
| A�� | ʵ����У���5minʱ���n��M��=0.050mol����0��5minʱ���ڣ���N��ʾ��ƽ����Ӧ���ʦԣ�N��=1.0��10-2mol/��L•min�� | |
| B�� | ʵ����У��÷�Ӧ��ƽ�ⳣ��K=2.0 | |
| C�� | ʵ����У��ﵽƽ��ʱ��X��ת����Ϊ50% | |
| D�� | ʵ����У��ﵽƽ��ʱ��b��0.05 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
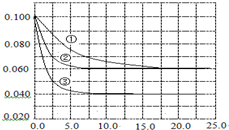 ����Һ�У���ӦA+2B?C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc��A��=0.100mol•L-1��c��B��=0.200mol•L-1��c��C��=0mol•L-1����Ӧ��A��Ũ����ʱ��ı仯��ͼ��ʾ������˵����ȷ���ǣ�������
����Һ�У���ӦA+2B?C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc��A��=0.100mol•L-1��c��B��=0.200mol•L-1��c��C��=0mol•L-1����Ӧ��A��Ũ����ʱ��ı仯��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ��ӦA+2B?C�ġ�H��0 | |
| B�� | ����Ӧ�١��ڵ�ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2 | |
| C�� | ʵ���ƽ��ʱB��ת����Ϊ60% | |
| D�� | ��С��Ӧ�۵�ѹǿ������ʹƽ��ʱc��A��=0.060 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
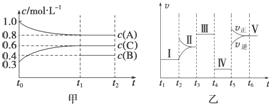 ��ij�ܱ������м��� 4mol A��1.2mol C ��һ������ B �������壬һ������ �·�����Ӧ�������ʵ�Ũ����ʱ��仯���ͼ��ʾ[��֪ t0��t1 �α��ֺ��¡����ݣ��� c��B��δ����]����ͼΪ t2 ʱ�̺�ı䷴Ӧ��������Ӧ������ʱ��ı仯�������֪ �� t2��t3��t4��t5 ʱ�̸��ı�һ�ֲ�ͬ������������ t3 ʱ��Ϊʹ�ô�����
��ij�ܱ������м��� 4mol A��1.2mol C ��һ������ B �������壬һ������ �·�����Ӧ�������ʵ�Ũ����ʱ��仯���ͼ��ʾ[��֪ t0��t1 �α��ֺ��¡����ݣ��� c��B��δ����]����ͼΪ t2 ʱ�̺�ı䷴Ӧ��������Ӧ������ʱ��ı仯�������֪ �� t2��t3��t4��t5 ʱ�̸��ı�һ�ֲ�ͬ������������ t3 ʱ��Ϊʹ�ô������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ�еĻ�ԭ����S2O32- | |
| B�� | �÷�Ӧ������������Cl- | |
| C�� | ������Ӧ�У�ÿ����1 mol SO42-������ȥ2 mol Cl2 | |
| D�� | ���ݸ÷�Ӧ���ж������ԣ�Cl2��SO42- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com