
����Ŀ����(Ti)����Ϊ21���ͽ�����ұ���ѵ���Ҫԭ���Ǻ�Fe2O3��������(FeTiO3)����������
����ͼ��

��֪��TiOSO4������ˮ����ˮ�⣬H2TiO3������ˮ���Իش��������⣺
��1������������Ҫʵ���������ȴ���ᾧ��_________����������ƣ�����������ʵ�����г����Լ�����___________�����������ƣ��м�ǿ�ȡ�
��2���������м�����ˮ��������__________________________________��
��3����������������������(FeSO47H2O)�ڿ����������������졢ˮ����������д���÷�Ӧ�Ļ�ѧ����ʽ______________________________________________________________��
��4�����������õ���������������(FeSO47H2O)��Ŀǰ��ҵ�ϴ��������ж���ˮ���õĻ�ѧ�Լ������߷�Ӧ��(Cr��+6��ת��Ϊ+3��)����ת��Ϊ����Ҫ��ҵ��ֵ�������帴��������(����FeOFeyCrxO3��ʾ)�����Ʊ��������帴����������������Եĺ�����ˮ�У�����FeSO47H2O�����ʵ���ӦΪ��ˮ�����۸�(�൱��CrO3)�����ʵ�����__________����
���𰸡� ���� ���� ���ȡ�ϡ�������ڴ�ʹTiO2+ˮ������H2TiO3 4FeSO47H2O+O2����2Fe2O3+4SO3+28H2O 5
�������������������1���ᾧ���������壬����Ϊ���ˣ����վ���ʧȥ�ᾧˮ�������н��У�
��2��TiO2+����H2TiO3�����ӷ���ʽΪTiO2++2H2O��H2TiO3��+2H+��
��3����������ԭԭ������Ӧ������������Ӧ�Ļ�ѧ����ʽΪ4FeSO4��7H2O+O2![]() 2Fe2O3+4SO3+28H2O��
2Fe2O3+4SO3+28H2O��
��4��FeOFeyCrxO3�У�CrΪ+3�ۣ�FeΪ+3�ۣ���x+y��2�����ݵ��ӵ�ʧ�غ���Fe��Cr��3��1��������x��0.5��y��1.5�����Եó����Ĺ�ϵΪ2.5FeSO47H2O��0.5CrO3�������ʵ���֮�ȱ�Ϊ5��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�����������ڵĺ�����Ȼ���٣�����ά������������в���ȱ�١�����˵����ͨ���������һʵ���õ�֤ʵ��������
A.ֲ��ȱþʱҶƬ���
B.�Ͳ�ȱ��ʱֻ���������
C.����ѪҺ�и��εĺ���̫�ͣ��������鴤
D.ȱ��ʱ��Ӱ��ATP�ĺϳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼΪ���ڱ��ж����ڵ�һ���֣���֪aԭ�ӵ�������ϵĵ�����Ŀ�Ǵ���������Ŀ��һ�룬����˵���в���ȷ���ǣ� �� ![]()
A.Ԫ��a������������ˮ��������Ա�b��
B.Ԫ��a��ԭ�Ӱ뾶��d�Ĵ�
C.Ԫ��a�ĵ����ڿ�����ȼ�ջᵼ�¡�����ЧӦ��
D.Ԫ��a������һ�����õİ뵼�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˫��A�Ľṹ��ʽ����ͼ��ʾ�������йش����ʵ�˵����ȷ����(����)

A. 1 mol��������������ˮ��Ӧ����2 mol Br2
B. ����������̼��������Һ��Ӧ�ų�CO2
C. �����ʵ�����̼ԭ�ӿ�����ͬһƽ��
D. ���������������������ӳɷ�Ӧ���������ʵĻ�ѧʽΪC15H28O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15�֣�Na2O2������Ư���ͺ�������еĹ�������
��1��ijѧϰС�鷢�֣���ʢ��Na2O2���Թ��м�������ˮ�����������������ݣ���������ʧ�������е���1~2�η�̪��Һ����Һ��죻���Թ���������ɫ�ܿ���ȥ����ʱ�����Թ��м�������MnO2��ĩ���������ݲ�����
��ʹ��̪��Һ�������Ϊ ����ɫ��ȥ�Ŀ���ԭ���� ��
������MnO2��Ӧ�Ļ�ѧ����ʽΪ ��
��2��Na2O2��ǿ�����ԣ�H2���л�ԭ�ԣ���ͬѧ����Na2O2��H2�ܷ�Ӧ��Ϊ����֤�˲��룬��С��ͬѧ��������ʵ�飬ʵ�鲽����������¡�
����1����ͼʾ��װ������ͼ�мг�����ʡ�ԣ�����������ԣ�װ��ҩƷ��
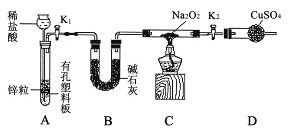
����2����K1��K2����������������װ��Na2O2��Ӳ�ʲ����ܣ�һ��ʱ���û���κ�����
����3������H2�Ĵ��Ⱥ�ʼ���ȣ��۲쵽Ӳ�ʲ�������Na2O2��ʼ�ۻ�������ɫ�ķ�ĩ����˰�ɫ���壬�����������ͭδ����ɫ��
����4����Ӧ��ȥ�ƾ��ƣ���Ӳ�ʲ�������ȴ��ر�K1��
��ʢװϡ������������� ��Bװ�õ������� ��
����������������ȵ�ԭ���� ��
������װ��D��Ŀ���� ��
����õ��Ľ����� �����ܷ�Ӧ���û�ѧ����ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���Na+��NH4+��Cl����SO42����NO3����CO32�� �� �ֽ�������ʵ�飺
��I��ȡһ��������Һ���Թ��У����������Ba��NO3��2��Һ�а�ɫ�������ɣ����˳��ij�����������ϡHNO3 �� ���ų�5.6L������£���ɫ��ζ�����壬ʣ�����4.66g��
��II��ȡ������Һ�����������NaOH��Һ�����ȣ�����13.6g��ɫ�д̼�����ζ�����壬��������ʹʪ��ĺ�ɫʯ����ֽ������
��III����ȡ������Һ������AgNO3��Һ������������
���������������жϣ�
����Һ�п϶����ڵ������� ��
����Һ�п϶������ڵ������� ��
����Һ�п��ܴ��ڵ������� ��
��д��ʵ�飨I���г�����������ϡHNO3���ų���ɫ��ζ��������ӷ���ʽ��
��ʵ�飨II���в�����������ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4 g NaOH�ܽ���ˮ���1L��Һ������ȡ��10mL����10mL��Һ�����ʵ���Ũ���ǣ� ��
A.1 mol/L
B.0.1 mol/L
C.0.01 mol/L
D.10 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˱������������������Դ��ij�о�С��ͨ�����¼����̣�����ҵ�����������������������Ҫ��![]() ���ڣ�ת�����Ҫ�Ĺ�ҵԭ��
���ڣ�ת�����Ҫ�Ĺ�ҵԭ��![]() ����Ӧ�����ԣ�
����Ӧ�����ԣ�
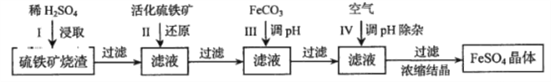
�������ԭFe2������Ҫ��ӦΪ��FeS2��7Fe2(SO4)3��8H2O=15FeSO4��8H2SO4��������������Ӧ����ش��������⣺
��1���ڢ�H2SO4��Fe2O3��Ӧ�����ӷ���ʽ��___________________________��
��2������ڢ���Fe3+�Ƿ���ȫ��ԭ��Ӧѡ��________��������ĸ��ţ���
A.KMnO4��Һ B.����-KI��Һ C.KSCN��Һ
��3���ڢ�FeCO3����ҺpH��5.8���ң�Ȼ���ٵ�VI��ͨ�����ʹ��ҺpH����5.2����ʱFe2������������Һ�����������ʳ�����ͨ�����������ҺpH���͵�ԭ����________________��
��4��FeSO4��ת��ΪFeCO3��FeCO3�ڿ����м��ȷ�Ӧ���Ƶ���ϵ��������ϡ�
��֪25�棬101kPaʱ��
4Fe(s)��3O2(g)=2Fe2O3(s) ��H=-1648kJ/mol
C(s)��O2(g)=CO2(g) ��H=-393kJ/mol
2Fe(s)��2C(s)��3O2(g)=2FeCO3(s) ��H=-1480kJ/mol
FeCO3�ڿ����м��ȷ�Ӧ����Fe2O3���Ȼ�ѧ����ʽ��______________��
��5��FeSO4��һ�������¿��Ƶ�FeS2(��������)���ײ��ϡ��ò��Ͽ��������������﮵�أ���طŵ�ʱ���ܷ�ӦΪ4Li+FeS2=Fe+2Li2S��������Ӧʽ��________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��̽��������ʴ��װ��ͼ�����ֿ�ʼʱU�ι���˺�īˮˮ���½���һ��ʱ���U�ι���˺�īˮˮ��������������˵������ȷ����

A. ���ָ�ʴ�����ĵ缫��Ӧʽ��ΪFe-2e-=Fe2+
B. ��ʼʱ�����������ⸯʴ
C. һ��ʱ���������������ʴ
D. ���ⷴӦ���ܷ�ӦʽΪ2Fe+O2+2H2O=2Fe(OH)2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com