
【题目】粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
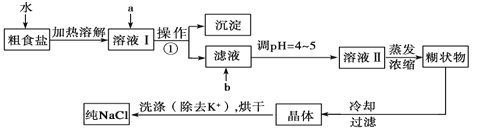
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳、稀盐酸。
(1)欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为___________(只填化学式)。
(2)如何检验SO42-是否沉淀完全_____________。
(3)调节pH的目的是_____________,试剂b是________(填名称)。
(4)洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为______________,使用该试剂的目的是除去晶体表面的杂质,减少晶体的损耗。
【答案】
(1)BaCl2、NaOH、Na2CO3(或NaOH、BaCl2、Na2CO3或BaCl2、Na2CO3、NaOH);
(2)静置,向少量上层清液中(或取少量上层清液)继续滴加BaCl2溶液,无沉淀产生,说明已沉淀完全,反之,则未沉淀完全。
(3)中和溶液中过量的OH- 和CO32-,稀盐酸;
(4)75%乙醇
【解析】
试题分析:(1)除去粗盐中的可溶性杂质:Ca2+、Mg2+、Fe3+、SO42-时,可以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,故答案为:BaCl2、NaOH、Na2CO3(或NaOH、BaCl2、Na2CO3或BaCl2、Na2CO3、NaOH);
(2)钡离子遇到硫酸根离子会生成白色沉淀,因此可以取上层清液少许于试管中,滴加BaCl2溶液,如无沉淀生成,则表明SO42-已沉淀完全;如有沉淀生成,则表明SO42-未沉淀完全,故答案为:静置一段时间后,取少量上层清液再滴加BaCl2溶液,若无沉淀生成,说明SO42-沉淀完全,反之未沉淀完全;
(3)加适量盐酸,可以少引入杂质,并且盐酸与过量NaOH溶液和过量Na2CO3溶液发生反应,离子方程式为:H++OH-═H2O,CO32-+2H+═H2O+CO2↑,从而除掉过量的OH-、CO32-;故答案为:除掉过量的OH-、CO32-;稀盐酸;
(4)粗盐中含有钾离子,所以氯化钠晶体中混有氯化钾,必须进行洗涤,氯化钠不溶于乙醇,可用乙醇冲洗固体表面的氯化钾,这样可以减少晶体的损失,故答案为:75%乙醇。


科目:高中化学 来源: 题型:
【题目】生物大分子在生物体的生命活动中具有重要的作用。碳原子本身的化学性质,使它能够通过化学键连接成链或环,从而形成各种生物大分子。可以说,地球上的生命是在碳元素的基础上建立起来的。以上事实说明( )
A. C元素能组成所有的化合物
B. C元素是构成细胞的最基本的元素
C. C元素是各种大分子中含量最多的元素
D. C元素比其他元素重要
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应方程式正确的是()
A.向AlCl3溶液中加入过量氨水:Al3++4NH3·H2O=4NH4++AlO2-+2H2O
B.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:
2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
C.NO2与水的反应:3NO2+H2O=2HNO3+NO
D.工业冶炼金属钠:2NaCl![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,甲容器中充满35Cl2,乙容器中充满37Cl2,下列叙述不正确的是( )
A.若两种气体体积相等,甲、乙两容器中气体的密度之比为35∶37
B.若两种气体体积相等,甲、乙两容器中气体分子数之比为35∶37
C.若两种气体质量相等,甲、乙两容器中气体所含质子数之比为37∶35
D.若两种气体体积相等,甲、乙两容器中气体所含中子数之比为9∶10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇(CH3OH)是一种重要的化工原料。已知
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H =-566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = + 44.00 kJ·mol-1
①试写出能表示CH3OH(1)燃烧热的热化学方程式: 。试利用热化学方程式计算,完全燃烧16g甲醇生成CO2和H2O(l)时,放出的热量为 kJ
②科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池。据此回答下列问题:氧气在 极反应;通入甲醇的电极反应式为_________________
(2)如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图像,回答问题:
①该反应的方程式为 。
②2min内,用B表示的反应速率为 。
③在其他条件下,测得A的反应速率为0.05mol/(L·s),此时的反应与800℃时相比, 。
A.比800℃时快 B.比800℃时慢
C.和800℃时速率一样 D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号中的试剂除去各组中的杂质,不正确的是( )
A. 苯中的甲苯(溴水) B. 乙醇中的水(新制CaO)
C. 乙醛中的乙酸(NaOH) D. 乙酸乙酯中的乙酸(饱和Na2CO3溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,mg气体A与ng气体B的分子数相同,下列说法中不正确的是( )
A.两种气体A与B的相对分子质量之比为m:n
B.同质量气体A与B的分子数之比为n:m
C.同温同压下,A、B两气体的密度之比为n:m
D.相同状况下,同体积A、B两气体的质量之比为m:n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.催化剂不影响反应活化能,但能增大单位体积内活化分子百分数,从而增大反应速率
B.化学反应速率为0.8 mol/(L·s)是指1 s时某物质的浓度为0.8 mol/L
C.根据化学反应速率的大小可以判断化学反应进行的快慢
D.对于化学反应来说,反应速率越大,反应现象越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是

A.电流从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电极A极反应式为2NH3-6e-=N2+6H+
D.当有4.48LNO2(标准状况)被处理时,转移电子为0.8mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com