
����Ŀ���������п�ͼ��ϵ��գ���֪��Ӧ�١������ҹ���ҵ�����е���Ҫ��Ӧ��X������Ϊ��ɫ��ζ��Һ�壻C��ɫ��Ӧ����ʻ�ɫ��JΪ���ɫ������D��E������Ϊ���壬��E��ʹƷ����Һ��ɫ��A�����н�������Ԫ�أ����н���Ԫ�ص���������ԼΪ46.7%�� 
��1��A�Ļ�ѧʽΪ�� F�Ļ�ѧʽΪ��
��2����Ӧ�۵Ļ�ѧ����ʽ����
��3����Ӧ�ڵ����ӷ���ʽ����
��4����Ӧ�ܵ����ӷ���ʽ����
��5����֪ÿ����16g E���ų�106.5kJ��������Ӧ�ٵ��Ȼ�ѧ����ʽΪ�� ��
���𰸡�
��1��FeS2��Fe2O3
��2��2SO2+O2 ![]() 2SO3
2SO3
��3��2Na2O2+2H2O�T4Na++4OH��+O2��
��4��Fe2O3+6H+�T2Fe3++3H2O
��5��FeS2��s��+ ![]() O2��g���T
O2��g���T ![]() Fe2O3��s��+2SO2��g����H=��852 kJ/mol
Fe2O3��s��+2SO2��g����H=��852 kJ/mol
���������⣺�������п�ͼ��ϵ��գ���֪��Ӧ�١������ҹ���ҵ�����е���Ҫ��Ӧ��X������Ϊ��ɫ��ζ��Һ���ƶ�Ϊˮ��C��ɫ��Ӧ����ʻ�ɫ˵������Ԫ�أ�JΪ���ɫ����Ϊ����������FΪFe2O3��D��E������Ϊ���壬��E��ʹƷ����Һ��ɫ˵��EΪSO2��GΪSO3��HΪH2SO4��IΪ��������˼· 1��3������Ӧ����D����1�Ǹ��������·�Ӧ�ģ���������DΪ������������Ӧ��������BΪ�������ƣ�CΪ�������ƣ�DΪ������A��D�ڸ����·�Ӧ���ɶ�������ͺ��������Ļ������ҵ�ϳ��õ������������е���Ҫ��Ӧ������Ĺ�ҵ����������Ĺ�ҵ����������Ĺ�ҵ����ԭ�϶�Ϊ������ͻ��������������ǻ���������AΪFeS2����AΪFeS2����BΪNa2O2��CΪNaOH��xΪH2O����DΪ������EΪSO2��FΪFe2O3 �� GΪSO3��HΪ���ᣬIΪ��������JΪ������������1�����ݷ����жϽ����AΪ��FeS2 �� FΪ Fe2O3 �� ���Դ��ǣ�FeS2��Fe2O3����2����Ӧ���Ƕ�������������ķ�Ӧ����Ӧ����ʽΪ2SO2+O2 ![]() 2 SO3�����Դ��ǣ�2SO2+O2
2 SO3�����Դ��ǣ�2SO2+O2 ![]() 2 SO3����3����Ӧ���ǹ���������ˮ��Ӧ����Ӧ�����ӷ���ʽΪ��2Na2O2+2H2O=4Na++4OH��+O2�������Դ��ǣ�2Na2O2+2H2O=4Na++4OH��+O2������4����Ӧ�������������������ᷴӦ����Ӧ�����ӷ���ʽΪ��Fe2O3+6H+=2Fe3++3H2O����5����֪ÿ����16g EΪSO2 �� ���ʵ���Ϊ0.25mol���ų�106.5kJ���������ݻ�ѧ����ʽ4FeS2��s��+11O2��g��=2Fe2O3��s��+8SO2��g��������8molSO2 �� ����Ϊ��
2 SO3����3����Ӧ���ǹ���������ˮ��Ӧ����Ӧ�����ӷ���ʽΪ��2Na2O2+2H2O=4Na++4OH��+O2�������Դ��ǣ�2Na2O2+2H2O=4Na++4OH��+O2������4����Ӧ�������������������ᷴӦ����Ӧ�����ӷ���ʽΪ��Fe2O3+6H+=2Fe3++3H2O����5����֪ÿ����16g EΪSO2 �� ���ʵ���Ϊ0.25mol���ų�106.5kJ���������ݻ�ѧ����ʽ4FeS2��s��+11O2��g��=2Fe2O3��s��+8SO2��g��������8molSO2 �� ����Ϊ�� ![]() =3408KJ����Ӧ���Ƕ���������������Ӧ���������������Ͷ�������Ӧ���Ȼ�ѧ����ʽΪ��4FeS2��s��+11O2��g��=2Fe2O3��s��+8SO2��g������H=��3408 kJ/mol��FeS2��s��+
=3408KJ����Ӧ���Ƕ���������������Ӧ���������������Ͷ�������Ӧ���Ȼ�ѧ����ʽΪ��4FeS2��s��+11O2��g��=2Fe2O3��s��+8SO2��g������H=��3408 kJ/mol��FeS2��s��+ ![]() O2��g���T
O2��g���T ![]() Fe2O3��s��+2SO2��g����H=��852 kJ/mol�����Դ��ǣ�FeS2��s��+
Fe2O3��s��+2SO2��g����H=��852 kJ/mol�����Դ��ǣ�FeS2��s��+ ![]() O2��g���T
O2��g���T ![]() Fe2O3��s��+2SO2��g����H=��852 kJ/mol��
Fe2O3��s��+2SO2��g����H=��852 kJ/mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��N��W����Ԫ�������ڱ��е�λ����ͼ��ʾ������˵������ȷ����
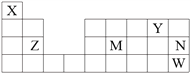
A. ԭ�Ӱ뾶��r(Z)��r(M)��r(Y)
B. ����������Ӧˮ�������ԣ�M��N
C. N�ĵ�������Z��W�γɵĻ�������û���Ӧ
D. X����������Ԫ���γɻ������X�Ļ��ϼ۲���ȫ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2C2O4�Ƕ�Ԫ���ᣬ��������ijŨ�ȵIJ�����Һ����μ���KOH��Һ��������Һ��H2C2O4��HC2O4-��C2O42-����ɰٷ�����pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
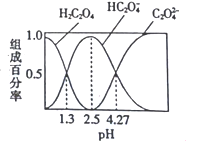
A. pH=4.27����Һ�У�c(K+)+c(H+)=c(OH-)+3c(C2O42-)
B. ��ӦHC2O4-+H2O![]() H2C2O4+OH-��ƽ�ⳣ��Ϊ10-4.27
H2C2O4+OH-��ƽ�ⳣ��Ϊ10-4.27
C. ����Һ�м���KOH��Һ��pH��1.3����4.27�Ĺ�����ˮ�ĵ���̶���������С
D. pH=2.5����Һ�У�c(H+)+2c(H2C2O4)=c(OH-)+c(C2O42-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ǧ�ĵ��ʡ�����������ִ���ҵ��������Ҫ��;��
��.��1��Ǧ���γɶ����������������������PbO������������PbO2������Fe3O4��Pb3O4��Pb3O4��HNO3������������ԭ��Ӧ����һ���κ�һ��Ǧ���������䷴Ӧ�Ļ�ѧ����ʽΪ_____________��
��.�Ժ�Ǧ����(��Ҫ��Pb��PbO��PbO2��PbSO4)Ϊԭ���Ʊ��ߴ�PbO������Ҫ����������

��2�� ��������ʱ����Fe2+������Pb��PbO2��Ӧ����PbSO4����1molPbSO4ת�Ƶ��ӵ����ʵ���Ϊ____________mol��
��3����֪����PbO�ܽ���NaOH��Һ��������ƽ����PbO(s)+NaOH(aq)![]() NaHPbO2(aq)�����ܽ��������ͼ��ʾ��
NaHPbO2(aq)�����ܽ��������ͼ��ʾ��

����ƷPbO���������ʲ�����NaOH��Һ��
���������Ϣ������ɴ�ƷPbO�õ��ߴ�PbO�IJ���������ƷPbO�ܽ���һ����__________(����35%������10%��)��NaOH��Һ����������110��������ܽ����___________(�������ȹ�����������Ũ����)������Һ��ȴ�ᾧ�����ˡ�ϴ�Ӳ�����õ��ߴ�PbO���塣
��4����PbO��Ʒ�ܽ���HCl��NaCl�Ļ����Һ�����õ���Na2PbCl2�ĵ��Һ�����Na2PbCl4��Һ����Pb��װ����ͼ��ʾ��

�������ĵ缫��ӦʽΪ_______________________��
�����һ��ʱ�����Na2PbCl4Ũ�ȼ����С��Ϊ�˻ָ���Ũ����ʵ�����ʵ�ѭ�����ã���������ȡ�ķ�����_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��CΪ������Ԫ�أ������ڱ���������λ����ͼ��ʾ�� ![]()
A��C����Ԫ�ص�ԭ�Ӻ��������֮�͵���Bԭ�ӵ���������B2���Ľṹʾ��ͼΪ�� ![]()
��ش��������⣺
��1��д��A��B��C����Ԫ�صķ��ţ�A �� B �� C ��
��2��Bλ�����ڱ��е������壮
��3��C���⻯��ĵ���ʽΪ��A������������Ӧˮ����Ļ�ѧʽΪ ��
��4��BC6�������������������Գ�������ȫû���ƻ����ã���һ�ֺ��з�չDZ�������������֪BC6���¶ȸ���45��ʱΪ��̬��BC6����������ӡ����ۡ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Fe��Ӧ������������KSCN��Һ����ʹ��Һ���ɫ����
A. Cl2 B. ���� C. CuSO4��Һ D. ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��B��C�����ɶ�����Ԫ����ɵĵ��ʣ��������ʾ�Ϊ�����F�ڳ��³�ѹ��ΪҺ̬��IΪ���д��Եĺ�ɫ���壮��������ͼ��ʾ��ת����ϵ�� 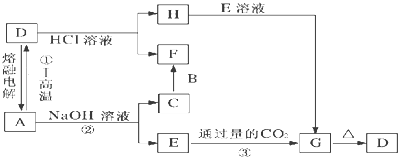
��������ת����ϵ�ش�
��1��д����Ӧ�ٵĻ�ѧ����ʽ����
��2��д����Ӧ�ڵ����ӷ���ʽ����д��H+E��Ӧ�����ӷ���ʽ����
��3����I�����������ᣬ��ֱ�д����Ӧ������Һ�д��ڵ������ӡ����������Լ�����Ӧ���ɲ���������
������ | �����Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����жԻ�ѧ��������⣬��ȷ���ǣ� ��
A. �ṹʽ��A=B=A���ȿ��Ա�ʾCO2��Ҳ���Ա�ʾSiO2
B. ����ʽ![]() ���Ա�ʾ�ǻ���Ҳ���Ա�ʾ����������
���Ա�ʾ�ǻ���Ҳ���Ա�ʾ����������
C. ����ģ��![]() �����Ա�ʾ������ӣ�Ҳ���Ա�ʾ���Ȼ�̼����
�����Ա�ʾ������ӣ�Ҳ���Ա�ʾ���Ȼ�̼����
D. ���ӽṹʾ��ͼ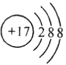 �����Ա�ʾ35Cl-,Ҳ���Ա�ʾ37Cl-
�����Ա�ʾ35Cl-,Ҳ���Ա�ʾ37Cl-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com