
【题目】Mg与Br2反应可生成具有强吸水性的MgBr2,该反应剧烈且放出大量的热。实验室采用如图装置制备无水MgBr2。下列说法错误的是
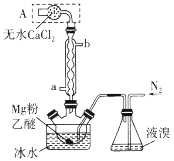
A.a为冷却水进水口
B.装置A的作用是吸收水蒸气和挥发出的溴蒸气
C.实验时需缓慢通入N2,防止反应过于剧烈
D.不能用干燥空气代替N2,因为副产物MgO会阻碍反应的进行
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列化学用语或命名正确的是( )
A.含有10个中子的氧原子的符号:![]() B.乙烯的结构简式:CH2CH2
B.乙烯的结构简式:CH2CH2
C.S2的结构示意图:![]() D.NH4Cl的电子式:
D.NH4Cl的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质属于同素异形体________;属于同位素是________;属于同一种物质是________;属于同系物是________。(写序号)
①红磷与白磷;②12C与14C;③S2与S8;④235U与238U;⑤干冰与二氧化碳;⑥CH4与CH3CH3;⑦ ![]() 与
与 ![]() ;⑧CH3CH=CH2和CH2=CH2。
;⑧CH3CH=CH2和CH2=CH2。
(2)已知A的产量可以用来衡量一个国家的石油化工发展水平,请写出工业上用A制备酒精的化学方程式________。
(3)在一定体积的 18 mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为 0.9 mol。则浓硫酸的实际体积________ (填“大于”“小于”或“等于”)100 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如 KNO3溶液),则该反应的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃A,B组成的混合气体完全燃烧后得到CO2和H2O(g)的物质的量随混合烃的总物质的量的变化如图,则下列说法正确的是( )
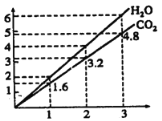
A.混合烃中n(C):n(H) = 2:5B.混合烃中一定不含有乙烯
C.若混合烃为CH4、C4H4,则体积比为4:1D.若混合烃为CH4、C3H4,则体积比为3:7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组设计的糖厂甘蔗渣利用方案如下图所示:其中:A是植物生长调节剂,B是高分子化合物,D是具有水果香味的物质。请回答以下问题:
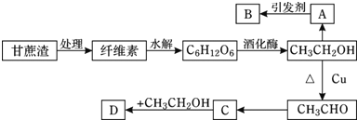
(1)纤维素的化学式为________,是________(填“纯净物”或“混合物”)。
(2)B的结构简式为________,C中官能团的名称为________。
(3)写出下列转化的化学方程式:CH3CH2OH→CH3CHO:_______,反应类型为________。
(4)化学式为C5H10O2的同分异构体中是C的同系物的有______种,其中在核磁共振氢谱上只有2个峰,且峰面积之比为1:9的结构简式为_______。
(5)下列说法正确的是________(填字母)。
A.生产A的主要方法是石油裂解,其产量是衡量一个国家石油化工水平的标志之一
B.分馏石油得到的各个馏分为纯净物
C.B可用于制造食品包装袋
D.塑料、合成纤维、合成橡胶等都是合成有机高分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是

A. 电流由O2所在的铂电极经外电路流向另一电极
B. O2所在的铂电极处发生还原反应
C. 该电池的负极反应式为:CH3CH2OH+3H2O-12e-="=" 2CO2↑+12H+
D. 微处理器通过检测电流大小而计算出被测气体中酒精的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙均为1L的恒容密闭容器,向甲中充入1molCH4和1molCO2,乙中充入1molCH4和nmolCO2,在催化剂存在下发生反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
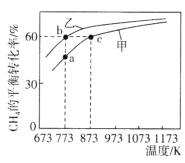
A.该反应的正反应是吸热反应
B.773K时,该反应的平衡常数小于12.96
C.H2的体积分数:![]()
D.873K时,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,平衡不发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸铁铵[(NH4)3Fe(C2O4)3]是一种常用的金属着色剂,易溶于水,常温下其水溶液的pH介于4.0~5.0之间。某兴趣小组设计实验制备草酸铁铵并测其纯度。
(1)甲组设计由硝酸氧化葡萄糖制取草酸,其实验装置(夹持及加热装置略去)如图所示。
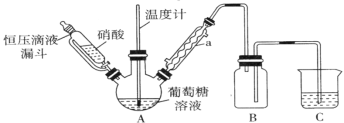
①仪器a的名称是________________。
②55~60℃下,装置A中生成H2C2O4,同时生成NO2和NO且物质的量之比为3:1,该反应的化学方程式为__________________________。
③装置B的作用是______________________;装置C中盛装的试剂是______________。
(2)乙组利用甲组提纯后的草酸溶液制备草酸铁铵。
将Fe2O3在搅拌条件下溶于热的草酸溶液;滴加氨水至__________,然后将溶液________、过滤、洗涤并干燥,制得草酸铁铵产品。
(3)丙组设计实验测定乙组产品的纯度。
准确称量5.000g产品配成100mL溶液,取10.00mL于锥形瓶中,加入足量0.1000mol·L-1稀硫酸酸化后,再用0.1000mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液的体积为12.00mL。
①滴定终点的现象是_______________________。
②滴定过程中发现褪色速率开始缓慢后迅速加快,其主要原因是____________________。
③产品中(NH4)3Fe(C2O4)3的质量分数为____________%。[已知:(NH4)3Fe(C2O4)3的摩尔质量为374g·mol-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环保部门检测到某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,要求该工厂从该废水中回收硫酸亚铁和金属铜。该工厂设计了如下流程图,完成回收硫酸亚铁和铜的简单实验方案。
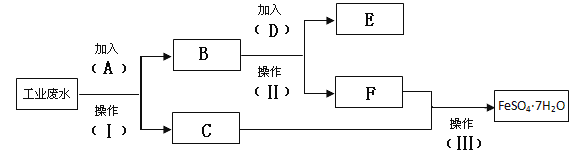
回答下列问题
(1)填写试剂A的化学式 _______________
(2)假如加入2mol D刚好完全反应,此步转移的电子的物质的量为 __________
(3)写出加入A的离子方程式: _________________
(4)操作Ⅱ和III 的名称分别是 ___________、 ____________、________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com