
【题目】甲醇的用途广泛,摩托罗拉公司也开发出一种由甲醇、氧气以及强碱做电解质溶液的新型手机电池,容量达氢镍电池或锂电池的10倍,可连续使用一个月才充一次电、请完成以下与甲醇有关的问题:
(1)工业上有一种生产甲醇的反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g);ΔH=-49kJ·mol-1。在温度和容积相同的A、B两个容器中,按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:
CH3OH(g)+H2O(g);ΔH=-49kJ·mol-1。在温度和容积相同的A、B两个容器中,按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:

①从反应开始到达到平衡时,A中用CO2来表示的平均反应速率为___。
②A中达到平衡时CO2的转化率为___。
③a=___。
(2)某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图:

①写出甲中通入甲醇这一极的电极反应式___。
②理论上乙中两极所得气体的体积随时间变化的关系如图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式___;在t2时所得溶液的pH约为___。

【答案】0.1c1mol/(L·s) 60% 19.6 CH3OH-6e-+80H-=CO32-+6H2O 4OH--4e-=O2↑+2H2O 1
【解析】
(1)①根据甲醇的浓度计算二氧化碳的浓度变化量再根据速率公式计算CO2 的反应速率;
②根据反应放出的热量计算参加反应的二氧化碳的物质的量,再利用转化率定义计算;
③恒温恒容下,容器A与容器B为等效平衡,平衡时对应组分的物质的量、浓度相等,二者起始物质的量等于各物质的化学计量数,放出热量与吸收热量之和等于反应热数值;
(2)①甲醇发生氧化反应,在碱性条件下生成碳酸根离子与水;
②原电池通入甲醇的为负极,乙中石墨电极为阳极、铁电极为阴极,开始Cl-在阳极放电生成氯气,阴极Cu2+放电生成Cu,故图丙中I表示阴极产生的气体,II表示阳极产生的气体,t1前电极反应式为:阳极2Cl--4e-=Cl2↑,阴极2Cu2++4e-=2Cu,t1~t2电极反应式为: 阳极4OH--4e-=O2↑+2H2O,阴极4H++4e-=2H2↑,在根据氧气的量计算氢氧根离子的物质的量,水电离出等物质的量的氢离子和氢氧根离子,根据公式计算得出c(H+)从而得出溶液的pH。
(1) ①根据表格可知A反应中甲醇的反应速率为v=![]() =
=![]() =0.1c1mol/(L·s),根据CO2(g)+3H2(g)
=0.1c1mol/(L·s),根据CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),所以A中CO2的平均反应速率为0.1c1mol/(L·s);
CH3OH(g)+H2O(g),所以A中CO2的平均反应速率为0.1c1mol/(L·s);
②根据CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g);ΔH=-49kJ·mol-1,由表中数据可知,反应达到平衡时放出的热量为29.4kJ,所以参加反应的CO2的物质的量为0.6mol,所以A中达到平衡时CO2的转化率为=
CH3OH(g)+H2O(g);ΔH=-49kJ·mol-1,由表中数据可知,反应达到平衡时放出的热量为29.4kJ,所以参加反应的CO2的物质的量为0.6mol,所以A中达到平衡时CO2的转化率为=![]() ;故答案为:60%;
;故答案为:60%;
③恒温恒容下,容器A与容器B为等效平衡,平衡时对应组分的物质的量、浓度相等,二者起始物质的量等于各物质的化学计量数,放出热量与吸收热量之和等于反应热数值,则吸收的热量a=反应热-放出的热量=49.0kJ-29.4kJ=19.6kJ,故答案为:19.6;
(2)①由图象可知左图为甲醇燃料电池,在碱性条件下甲醇失电子生成碳酸根离子和水,电极反应式为:CH3OH-6e-+80H-=CO32-+6H2O,故答案为:CH3OH-6e-+80H-=CO32-+6H2O;
②乙中石墨电极为阳极、铁电极为阴极,开始Cl-在阳极放电生成氯气,阴极Cu2+放电生成Cu,当Cu2+反应完了,水中的H+放电,故图丙中I表示阴极产生的气体,II表示阳极产生的气体,t1前电极反应式为:阳极2Cl--2e-=Cl2↑,t1~t2电极反应放出的气体速率减小了,说明Cl-反应完了,所以t1~t2电极反应式为:阳极4OH--4e-=O2↑+2H2O,t2点后相当于电解水,电极反应式为:阳极4OH--4e-=O2↑+2H2O,阴极4H++4e-=2H2↑,所以在t1后,石墨电极上的电极反应式为4OH--4e-=O2↑+2H2O;t1前电极反应式为:阳极2Cl--2e-=Cl2↑,产生的Cl2为224mL,t2点时阴极2Cu2++4e~=2Cu,Cu2+刚好反应完,阳极4OH--4e-=O2↑+2H2O中O2的体积为336mL-224mL=112mL,消耗OH-为0.02mol,水电离出等物质的量的氢离子和氢氧根离子,所以n(H+)=0.02mol,c(H+)=![]() =0.1mol/L,所以溶液的pH=1;答案:4OH--4e-=O2↑+2H2O;1。
=0.1mol/L,所以溶液的pH=1;答案:4OH--4e-=O2↑+2H2O;1。


科目:高中化学 来源: 题型:
【题目】25℃时,向一定浓度的Na2C2O4溶液中滴加盐酸,混合溶液的pH与离子浓度变化关系如图所示。已知H2C2O4是二元弱酸,X表示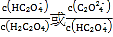 ,下列叙述错误的是
,下列叙述错误的是
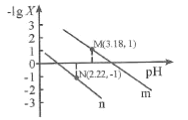
A.从M点到N点的过程中,c(H2C2O4)逐渐增大
B.直线n表示pH与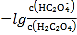 的关系
的关系
C.由N点可知Ka1 (H2C2O4)的数量级为10 -2
D.pH=4.18的混合溶液中:c(Na+)>c(HC2O4-)= c(C2O42-) =c(Cl-)> c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常把原子总数和价电子总数相同的分子或离子称为等电子体,等电子体具有相似的化学结构,则下列有关说法中正确的是( )
A.CH4和NH4+是等电子体,化学键类型完全相同
B.NO3-和CO32-是等电子体,均为平面正三角形结构
C.H3O+和PCl3是等电子体,均为三角锥形结构
D.SO2和O3是等电子体,SO2和O3具有相同的化学性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种兴奋剂的结构如图所示,下列说法正确的是( )

A. 该物质遇FeCl3溶液显紫色,属于苯酚的同系物
B. 1mol该物质分别与浓溴水和NaOH溶液反应时最多消耗Br2和NaOH均为4mol
C. 滴入酸性KMnO4溶液振荡,紫色褪去即证明该物质结构中存在碳碳双键
D. 该分子中所有碳原子均可能位于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、R均是第三周期主族元素。25℃时,各元素最高价氧化物对应水化物的 pH 与原子半径的关系如图,其中 X、N、W、R 测定的是浓度均为0.01 mol/L溶液的pH,Y、Z测定的是其饱和溶液的pH。下列说法正确的是

A.R、N分别与X形成二元化合物的水溶液均呈碱性
B.N、Z、X三种元素的最高价氧化物均不与水反应
C.单质与 H2化合由易到难的顺序是:R、N、M
D.金属单质与冷水反应由易到难的顺序是:Y、X、Z
查看答案和解析>>
科目:高中化学 来源: 题型:
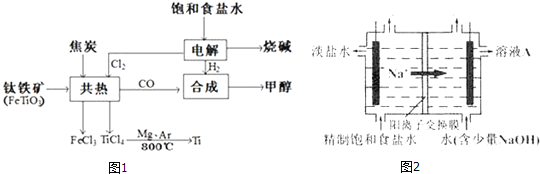
【题目】我国钛资源丰富,攀枝花和西昌已探明钛矿储量就有几十亿吨,其重要的矿石有金红石![]() 、钛铁矿
、钛铁矿![]() 以及钒钛铁矿.如图1所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率.
以及钒钛铁矿.如图1所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率.
![]() 常温下为无色液体,具有刺激性气味,极易水解,其化学键类型为 ______ ,写出
常温下为无色液体,具有刺激性气味,极易水解,其化学键类型为 ______ ,写出![]() 水解的方程式 ______
水解的方程式 ______
![]() 写出钛铁矿与焦炭、
写出钛铁矿与焦炭、![]() 共热得到
共热得到![]() 的化学方程式: ______
的化学方程式: ______
![]() ①
① ![]()
②![]()
请写出上图中![]() 生成Ti的热化学反应方程式: ______
生成Ti的热化学反应方程式: ______
![]() 海绵钛可用碘提纯,原理为
海绵钛可用碘提纯,原理为![]()
![]() 下列说法正确的是 ______
下列说法正确的是 ______
A 该反应正反应的![]()
B 在不同温度区域,![]() 的量保持不变
的量保持不变
C 在提纯过程中,![]() 的作用是将粗钛从低温区转移到高温区
的作用是将粗钛从低温区转移到高温区
D 在提纯过程中,![]() 可循环利用
可循环利用
![]() 钛网做阳极电解饱和食盐水常用隔膜电解槽.图2为阳离子交换膜电解槽示意图.
钛网做阳极电解饱和食盐水常用隔膜电解槽.图2为阳离子交换膜电解槽示意图.
①该电解装置阳极在 ______ ![]() 填左室、右室
填左室、右室![]() 氯碱工业电解槽一般采用Ti网作阳极而不用Fe网,其原因是 ______ .
氯碱工业电解槽一般采用Ti网作阳极而不用Fe网,其原因是 ______ .
②右室中加入少量NaOH的原因是 ______ .
![]() 在上述产业链中合成112t甲醇理论上能生产Ti ______
在上述产业链中合成112t甲醇理论上能生产Ti ______ 不考虑生产过程中物质的任何损失
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重要的化工原料F(C5H8O4)有特殊的香味,可通过如图所示的流程合成:

已知:①X是石油裂解气主要成分之一,与乙烯互为同系物;
② ;
;
③C、E、F均能与NaHCO3生成气体
(1)D中所含官能团的名称是_______________。
(2)反应②的化学方程式为_____________,反应类型是________;反应⑥的化学方程式为______________。
(3)F的同分异构体很多,其中一种同分异构体只含有一种官能团,在酸性或碱性条件下都能水解生成两种有机物,该同分异构体的结构简式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各溶液中,一定能大量共存的离子组是
A.常温下水电离的c(H+)为1×10-12mol/L的溶液中:Fe2+、Na+、SO42-、NO3-
B.滴加石蕊后呈蓝色的溶液中:K+、AlO2-、Cl-、HCO3-
C.使石蕊呈红色的溶液:NH4+、NO3﹣、AlO2﹣、I﹣
D.常温下![]() =1014的溶液中:K+、Ba2+、Cl-、Br-
=1014的溶液中:K+、Ba2+、Cl-、Br-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com